
10.有X、Y、Z三种同主族元素,已知最高价氧化物的水化物的酸性强弱顺序是:
H3XO4<H3YO4<H3ZO4。下列推断正确的是 ( )
A.元素的非金属性:X>Y>Z B.原子序数:X>Y>Z
C.气态氢化物的稳定性:XH3>YH3>ZH3
D.气态氢化物的还原性:XH3<YH3<ZH3
9.在元素周期表中,从左到右共有18个纵行。第1纵行(氢除外)为碱金属元素,稀有气体是第18纵行。下列说法中正确的是 ( )
A.铝元素位于第3纵行 B.过渡元素在周期表中占10个纵行
C.第17纵行所有元素的化合价都有+7价
D.第16纵行元素都是非金属元素
8.X、Y、Z为短周期元素,X的最外层电子数是Y原子最外层电子数的2倍,Y的原子序数比X的原子序数多5,Z原子的最外层电子数比Y多3。下列叙述正确的是( )
A.原子半径的大小顺序:X >Y>Z
B.Z单质与X单质直接反应可生成两种化合物
C.工业上,电解X和Y形成的化合物制取Y单质
D.Y、Z元素的最高价氧化物对应的水化物不能互相反应
7.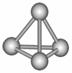 最近意大利罗马大学的FuNvio Cacace等人获得了极具理论研究意义的
最近意大利罗马大学的FuNvio Cacace等人获得了极具理论研究意义的
N4分子。N4分子结构如右图所示,已知断裂1molN-N吸收167kJ热量,
生成1molN≡N放出942kJ热量。根据以上信息和数据,下列说法正确
的是 ( )
A.N4属于一种新型的化合物
B.14N原子核内的中子数为14
C.N4沸点比P4(白磷)低 D.1molN4气体转变为N2吸收882kJ热量
6.俄、美科学家同时宣称合成了元素周期表上的第113号和第115号元素,第115号元素的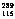 X原子在生成数秒后会衰变成
X原子在生成数秒后会衰变成 Y。下列有关叙述中,正确的是 ( )
Y。下列有关叙述中,正确的是 ( )
A.115号元素变成113号元素是化学变化 B.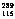 X 和
X 和 Y是两种核素
Y是两种核素
C.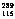 X 的中子数与质子数之差为174 D.113号元素位于周期表第8周期
X 的中子数与质子数之差为174 D.113号元素位于周期表第8周期
5.某合作学习小组讨论辨析以下说法:①粗盐和酸雨都是混合物;②沼气和水煤气都是可再生能源;③冰和干冰既是纯净物又是化合物;④不锈钢和目前流通的硬币都是合金;⑤盐酸和食醋既是化合物又是酸;⑥纯碱和熟石灰都是碱;⑦豆浆和雾都是胶体。上述说法正确的是 ................ ( )
A.①②③④ B.①②⑤⑥ C.③⑤⑥⑦ D.①③④⑦
4.下列条件下,两瓶气体所含原子数一定相等的是 ( )
A.同质量的C2H4和CO B.同体积、同密度的C2H4和C3H6
C.同温度、同体积的H2和N2 D.同压强、同体积的N2O和CO2
3.下列实验操作中,正确的是 ( )
①用托盘天平称取5.2 g NaCl;
②用50 mL量筒量取5.2mL盐酸;
③用蒸发皿加热NaCl溶液可以得到NaCl晶体;
④用 100 mL容量瓶配制50 mL 0.1mol·L-1H2SO4溶液;
⑤用带玻璃塞的棕色试剂瓶存放浓HNO3;
⑥中和热测定的实验中使用的玻璃仪器只有2种
A.①③⑤ B.②④⑥ C.①③④ D.③⑤⑥
2.物质的颗粒达到纳米级时,具有特殊的性质。如将单质铜制成“纳米铜”时,“纳米铜”具有非常强的化学活性,在空气中可以燃烧。下列叙述中正确的是 ( )
A.常温下,“纳米铜”比铜片的金属性强
B.常温下,“纳米铜”比铜片更易失电子
C.常温下,“纳米铜”与铜片的还原性相同
D.常温下,“纳米铜”比铜片的氧化性强
1.2002年由德、法、美及波兰等多国科学家组成的科研小组合成了非常罕见的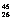 Fe原子,有关
Fe原子,有关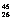 Fe的说法正确的是 ( )
Fe的说法正确的是 ( )
A.它是一种新元素
B.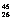 Fe与
Fe与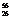 Fe互为同素异形体
Fe互为同素异形体
C.它是一种新核素
D.这种铁原子发生衰变放出两个质子后变成 Fe
Fe
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com