
1.若集合 =( )
=( )
A.[0,1] B. C.
C. D.
D.
23.有机物A是常用的食用油抗氧化剂,分子式为C10H12O5,可发生如下转化:
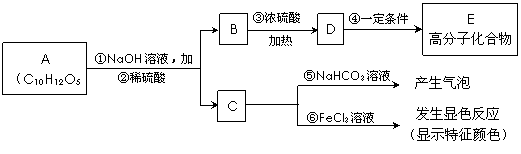
 已知B的相对分子质量为60,分子中只含一个甲基。C的结构可表示为:
已知B的相对分子质量为60,分子中只含一个甲基。C的结构可表示为:
(其中:-X、-Y均为官能团)。
请回答下列问题:
(1)根据系统命名法,B的名称为 。 (2)高聚物E的链节为 。
 (3)A的结构简式为
。
(3)A的结构简式为
。
 (4)
(4) )C有多种同分异构体,写出其中1种符合下列要求的同分异构体的结构简式
。
)C有多种同分异构体,写出其中1种符合下列要求的同分异构体的结构简式
。
 i.含有苯环
ii.能发生银镜反应 iii.不能发生水解反应
i.含有苯环
ii.能发生银镜反应 iii.不能发生水解反应
 (5)从分子结构上看,A具有抗氧化作用的主要原因是
(填序号)。
(5)从分子结构上看,A具有抗氧化作用的主要原因是
(填序号)。
 a.含有苯环
b.含有羰基
c.含有酚羟基
a.含有苯环
b.含有羰基
c.含有酚羟基

21.有关物质存在如图所示的转化关系(部分产物已省略)。通常C为气体单质,G为紫黑色固体单质。实验室中,常用固体E在B的催化下加热制取气体单质H。

请回答下列问题:
(1)反应①的化学方程式为
(2)反应②的离子方程式为
(3)D溶液与Pb(NO3)2溶液混合可形成沉淀,此沉淀的Ksp=7.0×10-9。将等体积的D溶液与Pb(NO3)2溶液混合,若D的浓度为1×10-2mo1/L ,则生成沉淀所需Pb(NO3)2溶液的最小浓度为 。22.海水是巨大的资源宝库,从海水中提取食盐和溴的过程如下:
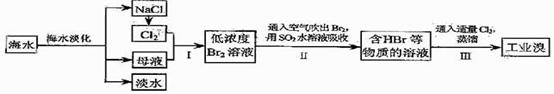
(1)请列举海水淡化的两种方法: 、 。
(2)步骤Ⅰ中已获得Br2,步骤Ⅱ中又将Br2还原为Br,其目的为 。
(3)步骤Ⅱ用SO2水溶液吸收Br2,吸收率可达95%,有关反应的离子方程式为 ,
(4)某化学研究性学习小组为了解从工业溴中提纯溴的方法,查阅了有关资料,Br2的沸点为59℃。微溶于水,有毒性和强腐蚀性。他们参观生产过程后,设计了如下装置简图:
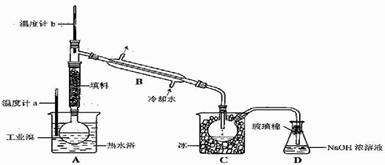
请你参与分析讨论:
①图中仪器B的名称: 。
②为除去该产物中仍残留的少量Cl2,可向其中加入NaBr溶液,充分反应后,再进行的分离操作是 。
③整套实验装置中仪器连接均不能用橡胶塞和橡胶管,其原因是 。
20. 短周期元素Q、R、T、W在元素周期表中的位置如右图所示,其中T所处的周期序数与主族序数相等,。请回答下列问题:
短周期元素Q、R、T、W在元素周期表中的位置如右图所示,其中T所处的周期序数与主族序数相等,。请回答下列问题:
(1)T的原子结构示意图为_______。
(2)元素的非金属性为(原子的得电子能力):Q______W(填“强于”或“弱于”)。
(3) W的单质与其最高价氧化物的水化物浓溶液共热能发生反应,生成两种物质,其中一种是气体,反应的化学方程式为_____ 。
(4)原子序数比R多1的元素,它的一种氢化物能分解为它的另一种氢化物,写出原子序数比R多1的元素的两种氢化物的电子式__________; 。
(5)R有多种氧化物,其中甲的相对分子质量最小。在一定条件下,2L的甲气体与0.5L的氧气相混合,若该混合气体被足量的NaOH溶液完全吸收后没有气体残留,所生成的R的含氧酸盐的化学式是__________。
19.目前世界各国在抗击甲型H1N1流感,达菲(Tamiflu)被世界卫生组织推荐作为治疗和预防甲型H1N1流感的有效药物之一,它是由我国特有中药材八角的提取物--莽草酸(shikimicacid)为原料经过十多步反应合成的。已知莽草酸和达菲的结构式如下:
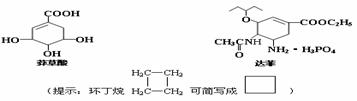
请完成:
(1)写出莽草酸分子中含氧官能团名称 ;
(2)达菲可能发生的反应类型有
A. 氧化反应 B. 水解反应 C. 银镜反应 D. 消去反应
(3)莽草酸通过消去反应可以得到B(B的结构简式为: ),B在浓硫酸加热作用下可得到缩聚物C,C的结构简式是
;
),B在浓硫酸加热作用下可得到缩聚物C,C的结构简式是
;
水杨酸是一种与B具有相同官能团的同分异构体,请写出水杨酸与乙酸酐合成阿司匹林(乙酰水杨酸)的化学方程式(有机物用结构简式表示): ;
B的同分异构体中既含有酚羟基又含有酯基的共有3种,写出其中一种同分异构体的结构简式 ;
18.铁溶于一定浓度的硝酸溶液时,发生反应的离子方程式为:
a Fe+b NO3-+c H+=d Fe2++f Fe3++g NO↑+h NO2↑+k H2O
下列有关推断中,不正确的是( )
A.2d+3f = 3g+h B.反应中每消耗5.6 g Fe,转移0.2mol-0.3mol e-
C.HNO3的氧化性大于Fe3+ D.当a不变时,d随着b的增大而增大
17.下列化合物的核磁共振氢谱中出现三组峰的是( )
A.2,2,3,3一四甲基丁烷 B.2,3,4一三甲基戊烷
 C.3,4一二甲基己烷 D.2,5一二甲基己烷
C.3,4一二甲基己烷 D.2,5一二甲基己烷
16.有关下图所示化合物的说法不正确的是( )
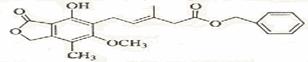
A.既可以与Br2的CCl4溶液发生加成反应,又可以在光照下与Br2发生取代反应
B.1 mol 该化合物最多可以与3 mol NaOH反应
C.既可以催化加氢,又可以使酸性KMnO4溶液褪色
D.既可以与FeCl3溶液发生显色反应,又可以与NaHCO3溶液反应放出CO2气体
15.下列离子方程式正确的是( )
A.H2SO4与Ba(OH)2溶液反应:Ba2++OH-+H++SO42-=BaSO4↓+H2O
B.CuSO4溶液吸收H2S气体:Cu2++S2- =CuS↓
C.AlCl3溶液中加入过量的浓氨水:Al3++4NH3·H2O=AlO2-+4NH4++2H2O
 D.等体积、等浓度的Ba(OH)2稀溶液与NH4HCO3稀溶液混合:
D.等体积、等浓度的Ba(OH)2稀溶液与NH4HCO3稀溶液混合:
 Ba2++2OH-+NH4++HCO3
- =BaCO3↓+NH3·H2O+H2O
Ba2++2OH-+NH4++HCO3
- =BaCO3↓+NH3·H2O+H2O
14. 物质的量之比为2:5的锌与稀硝酸反应,若硝酸被还原的产物为N2O,反应结束后锌没有剩余,则该反应中被还原的硝酸与未被还原的硝酸的物质的量之比是( )
 A. 1:4 B.1:5 C. 2:3 D.2:5
A. 1:4 B.1:5 C. 2:3 D.2:5
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com