
9.将amol H2S和1mol O2置于一个容积可变的容器内进行反应。维持容器内气体的压强不变(101KPa),在120℃下测得反应前后容器内气体的密度分别为d1和d2。若a的取值不同,则H2S的氧化产物可能有如下三种情况:
(1)全部是SO2此时a的取值范围是 。
(2)全部是S,此时a的取值范围是 ,并且d1 d2(填“小于”、“大于”或“等于”)。
(3)部分是SO2,部分是S,此时a的取值范围是 。反应所生成SO2的物质的量为 mol。容器内气体的物质的量之和为 mol(以含a的代数式表示)。
8.有一瓶亚硫酸钠溶液已部分氧化变质:2Na2SO3+O2 2Na2SO4,某学生设计了下列实验,确定Na2SO3的纯度:
2Na2SO4,某学生设计了下列实验,确定Na2SO3的纯度:
①称取ag样品。称量时所用主要仪器的名称是
②样品的溶解。溶解过程中使用玻璃棒搅拌的目的
③在溶液中加入过量的BaCl2溶液且用盐酸酸化。
(1)为什么要用盐酸酸化?
(2)BaCl2为什么要过量?
(3)怎样检验BaCl2溶液是否过量?
(4)为什么要洗涤沉淀?
(5)怎样洗涤沉淀?
(6)怎样判断沉淀是否洗净?
(7)烘干沉淀并计算。烘干后称量沉淀质量为bg,列出计算Na2SO3纯度的计算式。
5. 氯酸钾和亚硫酸氢钠间氧化还原反应生成Cl-和S+6的速度,如右图所示,又已知这个反应的速度随着溶液中氢离子浓度增大而加快。
氯酸钾和亚硫酸氢钠间氧化还原反应生成Cl-和S+6的速度,如右图所示,又已知这个反应的速度随着溶液中氢离子浓度增大而加快。
(1)为什么反应开始时反应速度加快?
(2)为什么后期反应速度下降?
3.亚硫酸钠中有+4价的硫,它既有氧化性又有还原性。现有试剂:溴水、硫化钠溶液、亚 硫酸钠溶液、稀硫酸、烧碱溶液、氨水。
①要证明Na2SO3具有还原性,应选用的试剂有 ,看到的现象 ,反应的离子方程式为 。
②要证明Na2SO3具有氧化性,应选用的试剂有 、 看到的现象 ,反应的离子方程 式为
2.已知四种物质在水中、液氨中的溶解度(g溶质/100g溶剂)。
AgNO3 Ba(NO3)2 AgCl BaCl2
水 170 9.3 1.5×10-4?33.3
液氨 86 97.2 0.8 0
这几种化合物在两溶剂中能发生复分解反应的方向分别是:
11.下列各组离子在水溶液中能大量共存的是( )
A.CO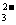 、HCO
、HCO 、OH-、Na+ B.K+、Cl-、S2-、CO
、OH-、Na+ B.K+、Cl-、S2-、CO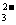 C.H+、Br-、Na+、SO
C.H+、Br-、Na+、SO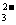 D.Ba2+、Cu2+、NO
D.Ba2+、Cu2+、NO 、SO
、SO
课外作业
10.只能表示一个化学方程式的离子方程式为( )
A.Ba2++2OH-+2H++SO
 BaSO4+2H2O
B.CO
BaSO4+2H2O
B.CO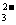 +2H+
+2H+ H2O+CO2
H2O+CO2
C.2Br-+Cl2 2Cl-+Br2
D.SO2+Cl2+2H2O
2Cl-+Br2
D.SO2+Cl2+2H2O 4H++2Cl-+SO
4H++2Cl-+SO
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com