
25.(10分)同学们从山上采集到一种石灰石,他们取80克该样品进行煅烧实验(所含杂质
在煅烧过程中不发生变化),测得反应后固体的质量(m)与反应时间(t)的关系如下表:
|
反应时间t∕s |
t0 |
t1 |
t2 |
t3 |
t4 |
t5 |
t6 |
|
反应后固体的质量m∕g |
80 |
75 |
70 |
66 |
62 |
58 |
58 |
请回答下列问题:
(1)当石灰石完全反应后,生成CO2的质量为 g。
(2)求该石灰石中CaCO3的质量分数,写出计算过程。
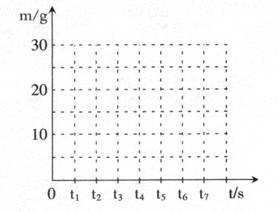
(3)请在下面坐标图中,画出煅烧时生成气体的质量(m)随时间(t)变化的曲线。
2009年广东省汕头市初中毕业生学业考试
24.(7分)莽草酸(化学式:C7H10O5)是制取抗“H1N1流感”药物“达菲”的原料。
请回答:
(1)莽草酸分子中C、H、O原子个数比为 。
(2)174g莽草酸含氢元素质量为 g。
(3)对1岁以上的儿童推荐按照下列“体重-剂量表”服用“达菲”:
|
体重 |
小于等于15千克 |
15-23千克 |
23-40千克 |
大于40千克 |
|
每次用量 |
30mg |
45mg |
60mg |
60mg |
假如患病儿童的体重是35千克,在治疗过程中,需每天服用“达菲”胶囊(每颗胶囊含“达菲”75mg)2次,一个疗程5天,那么该患儿一个疗程共需服用 颗。
23.(13分)为确定木炭还原氧化铜后的固体成份,请你与兴趣小组的同学完成以下探究
[对固体猜想]
猜想I:全部是金属铜; 猜想Ⅱ:除铜外,还含有氧化铜;
猜想Ⅲ:除铜外,还含有木炭; 猜想Ⅳ:除铜外,还含有氧化铜、 。
[进行实验]实验流程见下图:
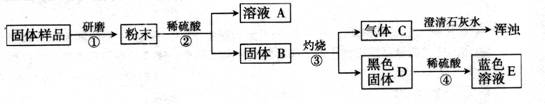
[问题与讨论]
(1)步骤②包括溶解、 两步操作,它们共同用到的玻璃仪器是烧杯、 。
(2)C的化学式为 ,D的化学式为 ,由此推出固体B中含有
(写化学式),步骤④发生反应的化学方程式为 。
(3)结合(2)的结论推断:如果溶液A显蓝色,则溶液A的溶质的化学式为 ,说明样品中含有 ,则证明猜想 成立;如果溶液A无
色,则证明猜想 成立。
22.(14分)下列图( I )是部分常用化学仪器或装置,图(Ⅱ)是部分“微型”化学仪器或装置(用“微型”仪器做实验,其试剂用量和废物排放量是通常用量的l/10或更少,符合绿色化学的理念)。对比图(I)图(Ⅱ)回答以下问题:
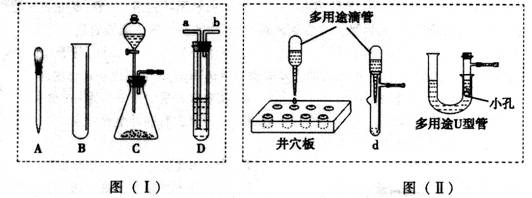
(1) 图( I )中A、B的名称分别是 、 ;若用D装置除去O2 中的水蒸气,则D中应装入的液体是 ,气体应从 口通入(填字母)。
(2)用图(Ⅱ)中的“微型”仪器做实验,固体只需极少量、液体用量也很少(或只需1-2小滴),相对用图(I)仪器做实验的优点是 (填序号):
①节约药品用量 ②能完全消除实验污染
③方便个人或家庭实验 ④若需加热也能节约燃料
(3)图( I )中的C装置的作用相当于图(II)中的装置 (填字母),它们在实验操作上的共同优点是通过控制 来控制反应速度。
(4)图( I )中的C装置和图(II)中的“多用途U型管”(是在U型管中套人一个底部有小孔的具支试管)都可用做“固一液”反应制取气体。若在反应进行中分别将两装置的橡胶管中部夹上铁夹,可能出现的现象是:C装置 ;
“多用途U型管” 。
21.(9分)近年来有人提出了利用海水(含氯化钠)处理含二氧化硫的废气,该方法的流程
如下:
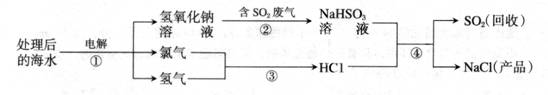
(1) 上图中从海水最终得到“NaCl(产品)”的过程属于 (填“物理变化”
或“化学变化”)。
(2) 图中反应①、③、④属于化合反应的是 (填序号)。
(3) ①中的反应物是氯化钠和 ,该反应的化学方程式为 。
(4)反应④的化学方程式为 。
20.(9分)元素周期律和周期表是学习化学的重要工具,下表是元素周期表的部分信息。
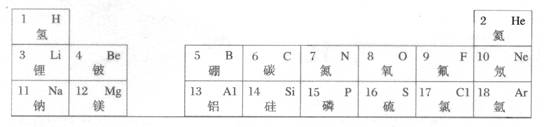 请认真分析表中信息,回答下列问题:
请认真分析表中信息,回答下列问题:
(1)地壳中含量仅次于氧的非金属元素名称是 ,该元素原子的质子数为
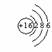
(2) 所表示的粒子符号为 ,它的晟外层电子数为 。
(3)由原子序数为8和13的两种元素组成的化合物是 (写化学式)。
(4)元素周期表同一横行元素的排列规律是:从左至右
19. (6分)Na2CO3俗称纯碱,是一种白色粉末,可以跟CO2和H2O反应生成NaHCO3,该
(6分)Na2CO3俗称纯碱,是一种白色粉末,可以跟CO2和H2O反应生成NaHCO3,该
反应的化学方程式为 ;Na2CO3与稀盐酸反应放出CO2,但实验室却不用这个反应制备CO2,其主要原因可能是
;已知Na2CO3的溶解度比NaHCO3大,那么在饱和的Na2CO3溶液中连续通人CO2,可观察到的现象是 。
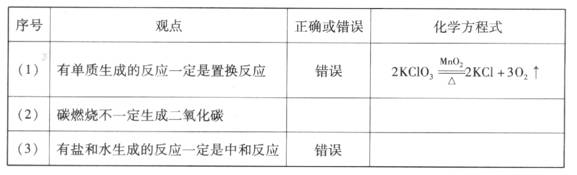
18.(5分)判断下列观点是否正确,用化学方程式证明你的结论
17.(4分)下表是氯化钠和硝酸钾在不同温度时的溶解度,根据此表回答
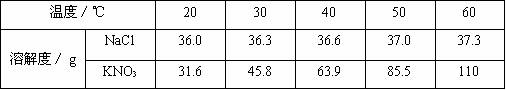
(1)60℃时,氯化钠的溶解度为 g。
(2)在30℃时,100g水中加入50g硝酸钾,充分搅拌后得到的溶液质量为 g。
(3)欲从海水中获得氯化钠晶体,应采取 方法。
(4)由表中数据分析可知,硝酸钾和氯化钠在某一温度时具有相同的溶解度x,则x的
取值范围是 g。
16.(4分)人们的日常生活离不开金属,高科技新材料的开发和应用也需要金属。
(1)现代社会使用大量的钢铁,钢铁与 接触容易生锈造成损失,在钢铁表面采用 方法可以防止钢铁生锈。
(2)波尔多液是由硫酸铜和熟石灰加水配制而成,不能用铁制容器配制的原因是(用化
学方程式表示) 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com