
4.[答案]C
[命题立意]考查NO2的实验室制法及性质
[解析]根据题目提示信息可知A、B分别为NO2、NO。这两种分子是含有氮氧极性键的极性分子,A、B正确;NO2、NO都不是酸酐,C错;NO2比NO多一个O原子,故D正确。
3. [答案]B
[命题立意]考查元素周期表及元素周期律
[解析]同周期中,第ⅠA族元素的金属性一定比第ⅡA族元素的金属性强;第ⅥA族元素中,氢化物稳定性最好的是H2O,常温下是液体,沸点最高;NH4Cl为离子化合物,故C错误;同周期中,金属元素的最高价离子与非金属的最低价离子电子层数不同,故D错误。
2.[答案]B
[命题立意]旨在考查离子共存及氧化还原反应
[解析]选项A中的离子在强酸性条件下不能发生氧化还原反应;B中的ClO-、Cl-在强酸溶液中能发生氧化还原反应,生成氯气;C中的Fe2+在碱性条件下不能共存;D中的NH4+不能存在于碱性条件下,而且该组离子在强酸性条件下也不能发生氧化还原反应。
1. [答案] D
[命题立意]:本题旨在提倡中学生经常用化学视角去观察和思考日常生活中的化学问题。
[解析]盐类融雪的原理主要是因为盐溶于水后,使溶液的凝固点降低,故选项A、B均错误;盐溶解在融化的雪水中,使这种雪水成为一定浓度的盐水,这种盐水能够损害大多数植物,故C错误;钢筋混凝土中的钢筋与高浓度的盐水形成吸氧腐蚀,故正确。
12.(19分)奶油中含有一种用做香料的有机化合物A,该有机化合物只含有C、H、O三种元素,分子中C、H、O原子个数比为2:4:1,其相对分子质量为88,A的结构式中含有碳氧双键。1molB可生成2molC,也可与2mol 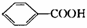 反应。
反应。

与A相关的反应如下:
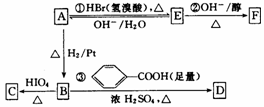
(1)写出反应②的反应类型:_____________________________。
(2)写出A、C、F的结构简式:A_____________________,C_______________,F_____________________。请写出两种与A的物质类别不同的同分异构体的结构简式:________________,________________。
(3)写出反应③的化学方程式:_____________________________________
(4)在空气中长时间搅拌奶油,A可转化为相对分子质量为86的化合物G,G的一氯代物只有一种,写出G的结构简式:____________________________。

答案及解析
11.(19分)某校开展课外研究性学习:从废旧干电池中回收碳棒、MnO2、NH4Cl、ZnCl2等物质,整个过程如下,回答有关问题: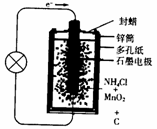
(1)如图是干电池的基本构造图,干电池工作时正极上的反应是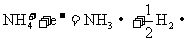 则负极上的电极反应式是________________。MnO2的作用是除去正极上的某产物,本身生成Mn2O3,该反应的化学方程式是________________________________。
则负极上的电极反应式是________________。MnO2的作用是除去正极上的某产物,本身生成Mn2O3,该反应的化学方程式是________________________________。
(2)锌皮和碳棒的回收:用钳子和剪子剪开回收的干电池的锌筒,将锌皮和碳棒取出,刷洗干净,将电池内的黑色粉末移入小烧杯中。
(3)氯化铵、氯化锌的提取、分离和检验。
①如何从黑色粉末中提取NH4Cl和ZnCl2的晶体混合物?
写出简要的实验步骤:________________________。
②用什么方法可将NH4Cl和ZnCl2的晶体混合物分离开?
_______________________________________
③写出证明ZnCl2晶体中含Zn2+的操作步骤及实验现象:___________________
_______________________(已知Zn(OH)2是两性氢氧化物且能溶解于氨水)
④最后剩余的黑色残渣的主要成分是MnO2,还有炭黑和有机物等,可用灼烧的方法除去杂质。该实验中需要用到的主要仪器除酒精灯外,还有__________________________________。
10.(10分)下面的框图是中学化学中几种常见物质的转化关系(其中部分产物已略去)。已知:A、C、D是常见的气体单质,F气体极易溶于水,且液态常做制冷剂。
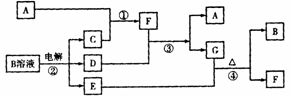
(1)D单质和E溶液反应,生成一种常见的消毒剂和漂白剂的有效成分,写出D+E溶液反应的离子方程式_____________________________________。
(2)写出鉴定G中阳离子的离子方程式:_____________________。
(3)工业上电解B溶液制得一系列化工原料,写出其电解的化学方程式,并标出电子转移的方向和数目________________________________________。
(4)③的反应可以用来检验D储运时是否泄露,检验的现象是______________,该反应的化学方程式:________________________________。
9.(12分)硼酸晶体呈片状,有滑腻感,可做润滑剂。硼酸对人体的受伤组织有缓和和防腐作用,故可以用于医药和食品防腐等方面。试回答下列问题:
(1)从题目信息可知硼酸应属于___________酸(填“弱”或“强”)
(2)硼酸的分子式为H3BO3,已知H与O成键,则其分子结构式为:__________。
(3)研究表明:在大多数情况下,元素的原子在形成分子或离子时,其最外层有达到8电子稳定结构的趋向。已知0.01mol硼酸可以被20mL 0.5mol·L-1NaOH溶液恰好完全中和,据此推测硼酸在水溶液中呈酸性的原因是(用离子方程式表示)___________________________;写出硼酸与NaOH溶液反应的离子方程式:____________________________________________。
(4)硼酸和甲醇在浓硫酸存在的条件下,可生成挥发性硼酸酯,试写出硼酸完全酯化的方程式:_______________________________________。
(5)科学家发现硼化镁在39K时呈超导性,在硼化镁晶体的理想模型中,镁原子和硼原子是分层排布的,一层镁一层硼相间排列。
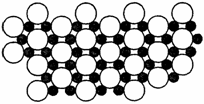
上图是该晶体微观空间中取出的部分原子沿Z轴方向的投影,白球是镁原子投影,黑球是硼原子投影,图中的硼原子和镁原子投影在同一平面上。根据下图确定硼化镁的化学式为____________________________________________。
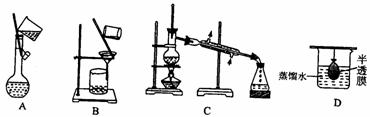
8.以下实验装置一般用于分离互溶的液体物质的是( )
7.

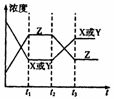 如右图所示,对于反应:X(g)+Y(g) 2Z(g); △H<0,如果反应开始经t1秒后达平衡,又经t2秒后,由于条件改变,原平衡破坏,到t3秒时又建立新的平衡,则t2到t3曲线变化的原因是( )
如右图所示,对于反应:X(g)+Y(g) 2Z(g); △H<0,如果反应开始经t1秒后达平衡,又经t2秒后,由于条件改变,原平衡破坏,到t3秒时又建立新的平衡,则t2到t3曲线变化的原因是( )
A.增大了X或Y的浓度
B.使用了催化剂
C.增大了体系压强
D.升高了该反应的温度
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com