
2.(04广东-20).海水的综合利用可以制备金属镁,其流程如下图所示:
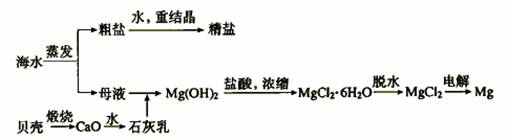
(1)若在空气中加热MgCl2·6H2O,生成的是Mg(OH)Cl或MgO,写出相应反应的化学方程式。
用电解法制取金属镁时,需要无水氯化镁。在干燥的HCl气流中加热MgCl2·6H2O时,能得到无水MgCl2,其原因是
(2)Mg(OH)2沉淀中混有的Ca(OH)2应怎样除去?写出实验步骤。
(3)实验室里将粗盐制成精盐的过程中,在溶解、过滤、蒸发三个步骤的操作中都要用到玻璃棒,分别说明在这三种情况下使用玻璃棒的目的;
溶解时: 。过滤时: 。蒸发时: 。
思维方法: 。
展望高考:
1.(02测试15).铁是自然界分布最广的金属元素之一,在地壳中的质量约占5%左右。铁矿石的种类很多,重要的有磁铁矿石(主要成分是Fe3O4)、赤铁矿石(主要成分是Fe2O3)等。
(1)写出赤铁矿炼铁的主要化学方程式: ;
(2)红热的铁能跟水蒸气反应,有一种产物是可燃性气体,则其反应式为: ;
在常温下,铁跟水不起反应。但是,在水和空气里的氧气及二氧化碳等的共同作用下,铁很容易生锈而被腐蚀,每年因腐蚀而损失的钢材占世界钢铁年产量的四分之一。刷油漆是重要的防腐蚀措施之一,油漆防腐蚀的主要原理是 。
(3)铁元素是人体的重要营养元素,举一例说明铁元素在人体中的重要作用: 。
思维方法: 。
展望高考:
2.金属冶炼的常见方法
(1) 热分解法:
请写出中学化学中常见的用此法制取某些金属的化学方程式
(2) 热还原法:
对于多数金属的冶炼,常用的还原剂如焦碳、一氧化碳、氢气和活泼金属加热反应的方法。如:
Fe2O3 + C =
CuO + CO =
WO3 + H2 =
MnO2 + Al =
(3) 电解法:
在金属活动顺序表中, 等金属的还原性很强,这些金属都很容易失电子,因此不能用一般的方法和还原剂使其从化合物中还原出来,只能用电解其 和 的方法来冶炼.如(请用相关的化学方程式举例:说明)
[例题解析]
[例1](02春招-31)Fe是地壳中含量很丰富的元素,也是生物体所必需的元素。
(1)自然界中铁矿石主要有赤铁矿和磁铁矿,金属铁是在高炉中冶炼的,高炉炼铁除了加入铁矿石外,还需加入焦炭和石灰石。请填空:
①写出磁铁矿主要成分的化学式: 。
②写出赤铁矿被还原成铁的化学方程式: 。
③写出焦炭在高炉中参与反应的两个化学方程式: 。
④写出CaCO3所参与反应的两个化学方程式: 。
解题思路: 。
易错点: 。
[例2](01上海-31).已知Fe2O3在高炉中有下列反应
Fe2O3+CO→2FeO+CO2
反应形成的固体混和物(Fe2O3、FeO)中,元素铁和氧的质量比用mFe︰mO表示。
(1)上述固体混和物中,mFe︰mO不可能是 (选填 a、b、c多选扣分)
(a)21︰9 (b)21︰7.5 (c) 21︰6
(2)若mFe︰mO=21︰8,计算Fe2O3被CO还原的百分率
(3)设 Fe2O3被CO还原的百分率为A%,则A%和混和物中mFe︰mO的关系式为(用含mFe、mO的代数式表示)。
 A%=
A%=
请在下图中画出A%和mFe/mO关系的图形。
(4)如果 Fe2O3和CO的反应分两步进行:
3Fe2O3+CO→2Fe3O4+CO2
Fe3O4+CO→3FeO+CO2
试分析反应形成的固体混和物可能的组成及相应的mFe︰mO(令mFe︰mO=21︰a,写出a的取值范围)。将结果填入下表。
|
混和物组成(用化学式表示) |
a的取值范围 |
|
|
|
解题思路: 。
易错点: 。
[考题再现]
1.金属在自然界存在有 态也有 态,
(1) 你能否给金属的冶炼下一个定义?
(2) 金属冶炼的原理是什么?
(3) 金属冶炼一般要经过那几个步骤?
(4) 金属冶炼有哪些方法?金属活动顺序与金属冶炼方法有没有联
系呢?如果有,有什么规律吗?
金属冶炼的一般规律:
K Ca Na Mg Al
( )法
Zn Fe Sn Pb (H) Cu
( )法
Hg Ag Pt Au
( )法 ( )取法
(5)在热还原法中还原剂通常是与金属氧化物反应,如果矿石不是氧化物而
是硫化物或碳酸盐时,怎么办?
(6)焦炭和氢气作为还原剂有什么区别(优缺点),如果要冶炼纯度很高的
金属一般要选用什么还原剂?用Al作为还原剂一般用于冶炼哪些金属?
3. 常识性了解金属回收与环境资源保护的意义;能写出冶炼金属
方法中对应的常见金属冶炼的有关化学发方程式.

教与学方案 笔记与反思
[自学反馈]
2.了解金属冶炼的一般原理及步骤,记住金属冶炼的三种方法,即热分解法、
热还原法和电解法;
1. 常识性了解金属在自然界中的分布、存在形态以及储量;
6.其它置换反应:
Na+TiCl4 =4NaCl+Ti 2H2+SiCl4====Si+4HCl Na+KCl = NaCl+K
Cl2+2HI = 2HCl+I2 F2+2HCl= 2HF+Cl2 H2S+Cl2 = S+2HCl
4NH3+3O2 = 2N2+6H2O 3 H2+Fe2O3 = 2Fe+3H2O
例1. 如图:
已知:化合物E与水反应生成白色浆状物;化合物F是不能成盐的氧化物;单质D能与某些稀有气体反应。
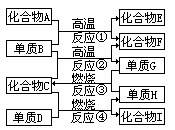
据此,请填空:
(1)化合物F是______;化合物I是______。
(2)反应②、反应④的化学方程式是______;______。
[
分析]由题目给定条件知:D为最活泼的非金属单质→F2;F为不成盐氧化物,且由单质B与化合物C发生置换反应得到→F为CO,B为碳,化合物C为氧化物,再结合G与H燃烧生成C,判断H为O2,C为H2O,G为H2,I为HF;化合物E由碳与化合物A反应得到(可能是碳化物),再考虑E与水反应生成白色浆状物,E是CaC2,A是CaO。
答案:(1)CO;HF (2)略
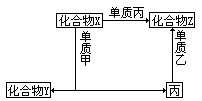
例2.下图表示物质之间的相互转化关系:
(1)若单质甲为金属,单质乙为非金属,指出它们的物质名称,并写出有关反应的化学方程式。
(2)若单质甲为非金属,单质乙为金属,指出它们的物质名称,并写出有关反应的化学方程式。
[分析]①X+甲→Y+丙,是置换反应。
②X与Z都是含Z、丙两种元素的化合物,则:X+丙→Z,为相同元素的不同价态的转化,若甲为非金属,乙为金属,能形成X与甲置换关系的只有:
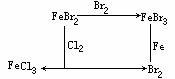
答案:(1)X:二氧化碳;Z:一氧化碳;Y:氧化镁
甲:镁;乙:氧气;丙:碳(化学方程式从略)。
(2)X:溴化亚铁;Y:氯化铁;Z:溴化铁;
甲:氯气;乙:铁;丙:溴。(化学方程式从略)
练习1.X、Y、Z是主族元素的单质,U、V为化合物。它们有如下反应(式中的反应系数和条件均已略去):
①X+U→V+Y ②X+Z→V ③Y+Z→U
(1)若X、Y的组成元素不是同一族,请写出符合①式的3个不同的化学方程式,并要求3个式子中的3种X和3种Y,分别由不同族的元素组成。
_____________________________________________。
(2)今有某化合物W,它跟化合物U或CO2反应,都能生成单质Y。符合题设的3个反应式关系的单质X是______,单质Y是______,单质Z是______,化合物W为______。
答案:(1)2Al+6HCl=2AlCl3+3H2↑ 2Mg+CO2=2MgO+C 2F2+2H2O=4HF+O2↑
(2)F2 O2 H2 Na2O2
甲
X
丙
Y
丙
乙
Z
练习2.如图所示,甲、乙、丙是三种常见单质,X、Y、Z是常见化合物,它们之间有如下转化关系:
(1)若甲是短周期金属单质,乙、丙是短周期非金
属单质,X、Y、Z中只有一种是离子晶体,试推断:
①X的电子式是_______________,若丙为灰黑色
固体,则其晶体类型为_________________
(分子晶体,原子晶体,混合型晶体)。
②工业上有些气体中也含有一定量的Z成分,试列举一种气体_____________。
③X与甲反应的化学方程式__________________________________________。
(2)若甲是具有氧化性的黄绿色气体单质,丙通常是深红棕色液体,Y和Z具有相同的阳离子,X与Z含有相同的阴离子,试写出X与足量的甲在溶液中完全反应的离子方程式:________ _____________
答案:(1)①CO2(电子式略) 混合型晶体
②水煤气 ③2Mg+CO2=2MgO+C
(2)3Cl2+2Fe2++4Br-=2 Fe3++2Br2+6Cl-
5.重要的置换反应:
①2Na+2H2O=2NaOH+H2↑ ②3Fe+4H2O Fe3O4+4H2↑
高温
高温
③F2+2H2O=4HF+O2 ④Cl2+H2S=S+2HCl
点燃
⑤2H2S+O2=2S+2H2O ⑥2C+SiO2 Si+2CO
高温
⑦2Mg+CO2 2MgO+C ⑧2Al+Fe2O3 =====2Fe+Al2O3
⑨C+H2O CO+H2 ⑩3Cl2+2NH3 === N2+6HCl
⑾Si+4HF===SiF4+2H2 ⑿极活泼金属及F2不能从水溶液中置换其它元素,非水溶液中不活泼的可置换活泼的。CuO+H2==Cu+H2O、2CuO+C==2Cu+CO2↑
△
4.按单质状态分
有“固→固”、“固→气”、“气→固”、“气→气”、“气→液”
高温
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com