
2.阿伏伽德罗常数NA= 6.0×1023 mol--1,分子直径的数量级d= 1.0×10-10m 。
1.分子运动论基本内容是:
(1) 物质是由分子组成的 ;
(2) 组成物质的分子在不停地做无规则的运动 ;
(3) 分子间存在相互作用力 。
4.分子间的的相互作用力。
3.分子的热运动、布朗运动。
2.阿伏伽德罗常数。
1.物质是由大量分子组成的。
23. (江苏)二氧化氯
(江苏)二氧化氯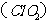 是一种在水处理等方面有广泛应用的高效安全消毒剂。与
是一种在水处理等方面有广泛应用的高效安全消毒剂。与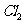 相比,
相比,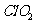 不但具有更显著地杀菌能力,而且不会产生对人体有潜在危害的有机氯代物。
不但具有更显著地杀菌能力,而且不会产生对人体有潜在危害的有机氯代物。
 (1)在
(1)在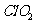 的制备方法中,有下列两种制备方法:
的制备方法中,有下列两种制备方法:
 方法一:
方法一: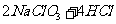 ====
====
 方法二:
方法二: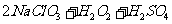 ====
====
 用方法二制备的
用方法二制备的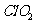 更适合用于饮用水的消毒,其主要原因是
。
更适合用于饮用水的消毒,其主要原因是
。
 (2)用
(2)用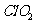 处理过的饮用水(
处理过的饮用水(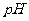 为5.5~6.5)常含有一定量对人体不利的亚氯酸根离子
为5.5~6.5)常含有一定量对人体不利的亚氯酸根离子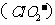 .2001年我国卫生部规定,饮用水
.2001年我国卫生部规定,饮用水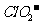 的含量应不超过0.2
的含量应不超过0.2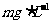 。
。
 饮用水中
饮用水中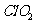 、
、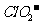 的含量可用连续碘量法进行测定。
的含量可用连续碘量法进行测定。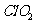 被
被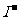 还原为
还原为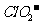 、
、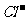 的转化率与溶液PH的关系如右图所示。当
的转化率与溶液PH的关系如右图所示。当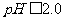 时,
时,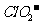 也能被
也能被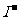
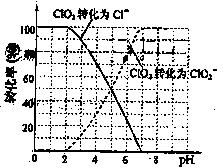
 完全还原成
完全还原成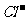 。反应生成的
。反应生成的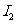 用标准
用标准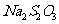 溶液滴定:
溶液滴定:

 ====
====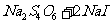
 ① 请写出
① 请写出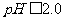 时,
时,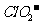 与
与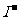 反应的离子方程式
。
反应的离子方程式
。
 ②请完成相应的实验步骤:
②请完成相应的实验步骤:
 步骤1:准确量取
步骤1:准确量取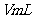 水样加入到锥形瓶中。
水样加入到锥形瓶中。
 步骤2:调节水样的
步骤2:调节水样的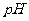 为7.0~8.0
为7.0~8.0
 步骤3:加入足量的
步骤3:加入足量的 晶体。
晶体。
 步骤4:加少量淀粉溶液,用
步骤4:加少量淀粉溶液,用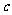
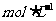
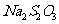 溶液滴定至终点,消耗
溶液滴定至终点,消耗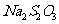 溶液
溶液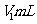 .
.
 步骤5: 。
步骤5: 。
 步骤6;再用
步骤6;再用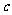
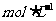
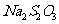 溶液滴定至终点,消耗
溶液滴定至终点,消耗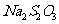 溶液
溶液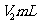 。
。
 ③根据上述分析数据,测得该引用水样中的
③根据上述分析数据,测得该引用水样中的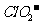 的浓度为
的浓度为 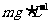 (用含字母的代数式表示)。
(用含字母的代数式表示)。
 ④若饮用水中
④若饮用水中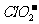 的含量超标,可向其中加入适量的,该反应的氧化产物是
(填化学式)
的含量超标,可向其中加入适量的,该反应的氧化产物是
(填化学式)
22.(广东) 某实验小组利用如下装置(部分固定装置略)制备氧化钙(Ca3N2),并探究其实验式。
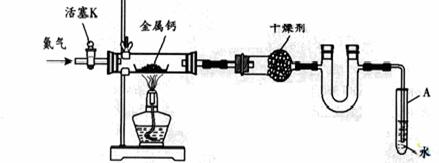
(1)按图连接好实验装置。检查装置的气密性,方法是 。
(2)反应过程中末端导管必须插入试管A的水中,目的是 。
(3)制备氮化钙的操作步骤是:①打开活塞K并通入N2;②点燃酒精灯,进行反应;③反应结束后, ;④拆除装置,取出产物。
(4)数据记录如下:

① 计算得到实验式CaxN2,其中x= .
② 若通入的N2中混有少量O2,请比较x与3的大小,并给出判断依据: 。
21.(浙江)单晶硅是信息产业中重要的基础材料。通常用碳在高温下还原二氧化硅制得粗硅(含铁、铝、硫、磷等杂质),粗硅与氯气反应生成四氯化硅(反应温度450-500°C),四氯化硅经提纯后用氢气还原可得高纯硅。以下是实验室制备四氯化硅的装置示意图。
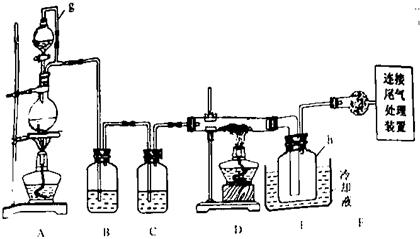
相关信息如下:
a.四氯化硅遇水极易水解;
b.硼、铝、铁、磷在高温下均能与氯气直接反应生成相应的氯化物;
c.有关物质的物理常数见下表:
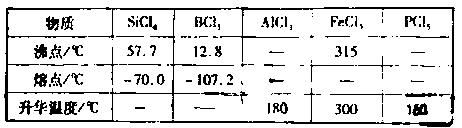
请回答下列问题:
(1)写出装置A中发生反应的离子方程式 。
(2)装置A中g管的作用是 ;装置C中的试剂是 ;装置E中的h瓶需要冷却理由是 。
(3)装置E中h瓶收集到的粗产物可通过精馏(类似多次蒸馏)得到高纯度四氯化硅,精馏后的残留物中,除铁元素外可能还含有的杂质元素是 (填写元素符号)。
(4)为了分析残留物中铁元素的含量,先将残留物预处理,是铁元素还原成Fe2+ ,再用KMnO4标准溶液在酸性条件下进行氧化还原滴定,反应的离子方程式是:
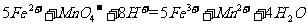
①滴定前是否要滴加指示剂? (填“是”或“否”),请说明理由 。
②某同学称取5.000g残留物,预处理后在容量瓶中配制成100ml溶液,移取25.00ml,试样溶液,用1.000×10-2mol· L-1KMnO4标准溶液滴定。达到滴定终点时,消耗标准溶液20.00ml,则残留物中铁元素的质量分数是 。
20.

 (全国Ⅱ卷)
(全国Ⅱ卷)
 已知氨可以与灼热的氧化铜反应得到氮气和金属铜,用示意图中的装置可以实现该反应。
已知氨可以与灼热的氧化铜反应得到氮气和金属铜,用示意图中的装置可以实现该反应。


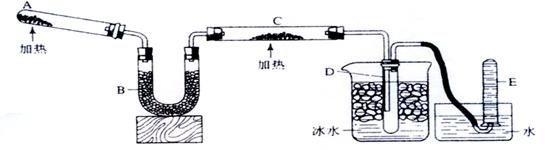



 回答下列问题:
回答下列问题:

 (1)A中加入的物质是_________________________________________.
(1)A中加入的物质是_________________________________________.

 发生反应的化学方程式是_____________________________________;
发生反应的化学方程式是_____________________________________;

 (2)B中加入的物质是___________,其作用是______________________:
(2)B中加入的物质是___________,其作用是______________________:

 (3)实验时在C中观察到得现象是____________________________,
(3)实验时在C中观察到得现象是____________________________,

 发生反应的化学方程式是____________________________________;
发生反应的化学方程式是____________________________________;

 (4) 实验时在D中观察到得现象是________________________________,
(4) 实验时在D中观察到得现象是________________________________,

 D中收集到的物质是___________,检验该物质的方法和现象是____________________.
D中收集到的物质是___________,检验该物质的方法和现象是____________________.
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com