
22.(山东省临沭一中2009届高三上学期期中考试)已知I-、Fe2+、SO2和H2O2均有还原性,
它们在酸性溶液中还原性的强弱顺序是:( B )
H2O2< Fe2+<I-<SO2。则下列反应不能发生的是
 A.2Fe3++
SO2+2H2O 2Fe2++SO42-+4H+
A.2Fe3++
SO2+2H2O 2Fe2++SO42-+4H+
 B.H2O2+H2SO4 SO2↑+O2↑+2H2O
B.H2O2+H2SO4 SO2↑+O2↑+2H2O
 C.I2+ SO2+2H2O H2SO4+2HI
C.I2+ SO2+2H2O H2SO4+2HI
 D.2Fe3++
2I- 2Fe2++ I2
D.2Fe3++
2I- 2Fe2++ I2
20.(山东省临沭一中2009届高三上学期期中考试) (4分)某钠盐溶液可能含有阴离子NO3-、CO32-、SO32-、SO42-、Cl-、Br-、I-、为鉴别这些离子,分别取少量溶液进行以下实验:
①测得混合液呈碱性;②加HCl后,生成无色无味气体,该气体能使饱和石灰水溶液变浑
浊;③加CCl4后,滴加少量氯水,振荡后,CCl4后层未变色;④加BaCl2溶液产生白色
沉淀,分离,在沉淀中加入足量盐酸,沉淀不能完全溶解;
⑤加HNO3酸化后,再加过量AgNO3,溶液中析出白色沉淀。
该溶液一定含有的离子是 ,上述5个实验不能确定是否存在的离子是 。
答案..肯定含有CO32-、SO42-、 Cl-,可能含有NO3-(每个一分共4分)
21(山东省临沭一中2009届高三上学期期中考试)下列化学反应的离子方程式正确的是( C )
A.用稀HNO3溶解FeS固体:FeS+2H+==Fe2++H2S↑
B.少量SO2通入Ca(ClO)2溶液中:SO2+H2O+Ca2++2ClO-==CaSO3↓+2HClO
C.在稀氨水中通入过量CO2:NH3·H2O+CO2==NH4++HCO3-
D.氢氧化钙溶液与等物质的量的稀硫酸混合:Ca2++OH-+H++SO42-==CaSO4↓+H2O
19.(山东省日照一中2009届高三阶段性测试化学试题 )(11分)某钠盐溶液可能含有阴离
子NO3-、CO32-、SO32-、SO42-、Cl-、Br-、I-、为鉴别这些离子,分别取少量溶液进
行以下实验:
①测得混合液呈碱性;
②加HCl后,生成无色无味气体,该气体能使饱和石灰水溶液变浑浊;
③加CCl4后,滴加少量氯水,振荡后,CCl4后层未变色;
④加BaCl2溶液产生白色沉淀,分离,在沉淀中加入足量盐酸,沉淀不能完全溶解;
⑤加HNO3酸化后,再加过量AgNO3,溶液中析出白色沉淀。
(1)分析上述5个实验,写出每一步实验鉴定离子的结论与理由。
实验① ;
实验② ;
实验③ ;
实验④ ;
实验⑤ ;
(2)上述5个实验不能确定是否存在的离子是 。
答案..(1)①说明可能含有CO32-或者含有SO32- 因为二者水解均显碱性;
②肯定含有CO32- ,肯定不含SO32-、因SO2有刺激性气味
③肯定不含有Br-、I-,因两者均能与氯水反应后生成单质溴和单质碘,溴和碘单质溶
解于CCl4显色;
④肯定含有SO42-,因BaSO4不溶于盐酸。
⑤肯定含有Cl-,因AgNO3与Cl-反应生成的AgCl不溶于稀HNO3。
(2)NO3-
18.(山东省泰安英雄山中学2009届高三年级第一次复习检测化学卷)已知硫酸铅难溶于水,也难溶于硝酸,却可溶于醋酸铵溶液形成无色溶液,其化学方程式是
PbSO4+2CH3COONH4==Pb(CH3COO)2+(NH4)2SO4。当在Pb(CH3COO)2(醋酸铅)溶液
中通入H2S时,有黑色沉淀PbS生成。表示这个反应的有关离子方程式正确的是
( A )
A.Pb(CH3COO)2+H2S==PbS↓+2CH3COOH
B.Pb2++H2S==PbS↓+2H+
C.Pb2++2CH3COO-+H2S==PbS↓+2CH3COOH
D.Pb2++2CH3COO-+2H++S2-==PbS↓+2 CH3COOH
17.(山东省泰安英雄山中学2009届高三年级第一次复习检测化学卷)下列离子方程式中正
确的是 ( D )
A.澄清石灰水与稀盐酸反应:Ca(OH)2+2H+==Ca2+2H2O
B.钠与水的反应:Na+2H2O==Na++2OH-+H2↑
C.铜片插入硝酸银溶液中:Cu+Ag+==Cu2+Ag
D.大理石溶于醋酸的反应:CaCO3+2CH3COOH==Ca2+2CH3COO-+CO2↑+H2O
16.(山东省泰安英雄山中学2009届高三年级第一次复习检测化学卷)下列溶液中, 能大量
共存的离子组是 ( C )
A.pH=7的溶液:Na+、Fe3+、Cl-、SO42-
B.c(H+)=1×10-2mol·L-1的溶液:Na+、NH4+、CO32-、SO42-
C.含有大量SO42-的溶液:K+、Cu2+、Cl-、NO3-
D.含有大量ClO-的溶液:SO42-、H+、Mg2+、I-
15.在下表中,欲用一种试剂Z来判别盐溶液中的离子X和离子Y是否存在时,此试剂使用正确的是 ( A )
|
试剂Z |
离子X |
离子Y |
|
A.氨水 |
Al3+ |
Mg2+ |
|
B.硝酸银 |
Cl- |
CO32- |
|
C.硫酸钠 |
Ba2+ |
Ca2+ |
|
D.硝酸钠 |
SO42- |
Cl- |
14.(山东省泰安英雄山中学2009届高三年级第一次复习检测化学卷)(5分)写出下列反应
的离子方程式:
(1)用烧碱溶液吸收氯气 ;
(2)铜与氯化铁溶液反应 ;
(3)铝与氢氧化钠反应 ;
(4)澄清石灰水中通入少量二氧化碳 ;
(5)碳酸钠溶液显碱性的原因 。
答案.(1)2Na+2H2O=2Na++2OH-+H2↑
(2)2OH-+Cl2=Cl-+ClO-+H2O
(3)Fe+Cu2+=Fe2++Cu
(4)Fe+2H+=Fe2++ H2↑
(5)Ca2++2OH-+CO2=CaCO3↓+H2O
13.(山东省泰安英雄山中学2009届高三年级第一次复习检测化学卷)(8)化学实验中,如使某步中的有害产物作为另一步的反应物,形成一个循环,就可不再向环境排放该种有害物质。例如:
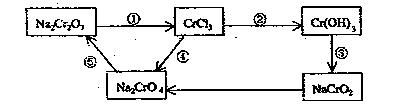
(1)在上述有编号的步骤中,需用还原剂的是 ,需用氧化剂的是 。
(2)在上述循环中,既能与强酸反应又能与强碱反应的两性物质是 (填化学式)
(3)完成并配平步骤①的化学方程式,标出电子转移的方向和数目:
□Na2Cr2O7+□KI+□HCl→□CrCl3+□NaCl+□KCl+□I2+□
答案.(1)① ④ (2)Cr(OH)3
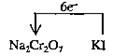 (3)1
6 14 2
2 6 3
7H2O
(3)1
6 14 2
2 6 3
7H2O
12.(山东省泰安英雄山中学2009届高三年级第一次复习检测化学卷)(7分)A、B、C、D、E五种可溶性化合物,分别由阳离子Fe3+、Ba2+、Al3+、Na+、Ag+和阴离子NO3-、OH-、SO42-、Cl-、CO32-中的各一组成(离子不重复)。现做如下实验:
①A和E的溶液显碱性,0.1mol/LA溶液的pH小于13;
②在B的溶液中逐滴加入氨水有白色沉淀生成,继续加氨水至过量,沉淀消失;
③在C的溶液中加入铁粉,溶液的质量增加;
④在D的溶液中加入过量的Ba(OH)2溶液,没有沉淀。
(1)根据以上事实推断A、B、E的化学式:
A 、B 、E
(2)写出③和④的离子方程式:
③
④
答案.(1)Na2CO3 AgNO3 Ba(OH)2
(2)③2Fe3++Fe=3Fe2+ ④Al3++4OH-=[Al(OH)4]
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com