
23. (ЩНДѓИНжа2008-2009бЇФъЩЯбЇЦкИпШ§дТПМ)дкУмБеШнЦїжаНјаа
(ЩНДѓИНжа2008-2009бЇФъЩЯбЇЦкИпШ§дТПМ)дкУмБеШнЦїжаНјаа
ЁЁ
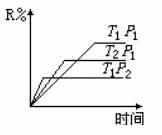
ЯТСаЗДгІЃКM(g)+N(g) R(g)+2LЃЌДЫЗДгІЗћКЯЯТУцЭМ
R(g)+2LЃЌДЫЗДгІЗћКЯЯТУцЭМ
ЁЁЁЁ ЯёЃЌЯТСаа№Ъіе§ШЗЕФЪЧЁЁ(ЁЁ C ) ЁЁ
ЁЁ A. е§ЗДгІЮќШШЃЌLЪЧЦјЬх ЁЁ B. е§ЗДгІЮќШШЃЌLЪЧЙЬЬх ЁЁ C. е§ЗДгІЗХШШЃЌLЪЧЦјЬх ЁЁ D. е§ЗДгІЗХШШЃЌLЪЧЙЬЬхЛђвКЬх
22. (ЩНДѓИНжа2008-2009бЇФъЩЯбЇЦкИпШ§дТПМ)ЮТЖШвЛЖЈЪБ, гкУмБеШнЦїжаЗЂЩњПЩФцЗДгІ: ЁЁЁЁ
mA(Цј) + nB(Цј)  pC(Цј), ДяЕНЦНКтКѓ, ШєНЋЛьКЯЦјЬхЕФЬхЛ§бЙЫѕЕНдРДЕФ
pC(Цј), ДяЕНЦНКтКѓ, ШєНЋЛьКЯЦјЬхЕФЬхЛ§бЙЫѕЕНдРДЕФ
1/2,ЕБдйДЮДяЕНЦНКтЪБ, CЕФХЈЖШЮЊдЦНКтЪБCЕФХЈЖШЕФ 1 .9 БЖ, дђЯТСаа№Ъіжае§ШЗ
ЕФЪЧ( BЁЁ )
A. ЦНКтЯђФцЗДгІЗНЯђвЦЖЏЁЁЁЁЁЁЁЁЁЁЁЁ B. CЦјЬхЕФЬхЛ§ЗжЪ§діДѓ
C. ЦјЬхAЕФзЊЛЏТЪЩ§ИпЁЁЁЁЁЁЁЁЁЁЁЁЁЁ D. m + n > p
21. (ЩНДѓИНжа2008-2009бЇФъЩЯбЇЦкИпШ§дТПМ)дкУмБеШнЦїжаНјааЛЏбЇЗДгІЃК2SO2 + O2
2SO3ЁЃвбжЊЗДгІЙ§ГЬжаФГвЛЪБПЬSO2ЁЂO2ЁЂSO3ХЈЖШЗжБ№ЮЊ0.2mol/LЁЂ0.1mol/LЁЂ0.2mol/LЁЃ
ЕБЗДгІДяЕНЦНКтЪБПЩФмДцдкЕФЪ§ОнЪЧ( BЁЁ )
AЁЂSO2ЮЊ0.4mol/LЁЂO2ЮЊ0.2mol/LЁЁЁЁ BЁЂSO2ЮЊ0.25mol/L
CЁЂSO2ЁЂSO3ЖМЮЊ0.15mol/LЁЁЁЁЁЁЁЁЁЁ DЁЂSO2ЮЊ0.4mol/L
20. (ЩНДѓИНжа2008-2009бЇФъЩЯбЇЦкИпШ§дТПМ)ЁЂКуЮТКубЙЯТЃЌдкШнЛ§ПЩБфЕФЦїУѓжаЃЌЗДгІ2NO2ЁЁ
ЁЁ (g)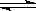 N2O4(g)ДяЕНЦНКтКѓЃЌдйЯђШнЦїФкЭЈШывЛЖЈСПNO2ЃЌгжДяЕНЦНКтЪБЃЌN2O4
N2O4(g)ДяЕНЦНКтКѓЃЌдйЯђШнЦїФкЭЈШывЛЖЈСПNO2ЃЌгжДяЕНЦНКтЪБЃЌN2O4
ЁЁЁЁ ЕФЬхЛ§ЗжЪ§( AЁЁ )
A. ВЛБфЁЁЁЁЁЁ ЁЁЁЁЁЁB. діДѓЁЁЁЁЁЁЁЁЁЁЁЁ C. МѕЩй ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁD. ЮоЗЈХаЖЯ
19.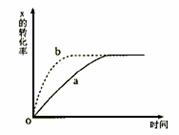 (ЩНДѓИНжа2008-2009бЇФъЩЯбЇЦкИпШ§дТПМ)гвЭМЧњЯпaБэЪОЗХЁЁ
(ЩНДѓИНжа2008-2009бЇФъЩЯбЇЦкИпШ§дТПМ)гвЭМЧњЯпaБэЪОЗХЁЁ
ШШЗДгІX(g)+Y(g)ЁЁ  Z(g)+M(g)+N(s)НјааЙ§ГЬжаXЕФзЊ
Z(g)+M(g)+N(s)НјааЙ§ГЬжаXЕФзЊ
ЛЏТЪЫцЪБМф ЁЁ БфЛЏЕФЙиЯЕЁЃШєвЊИФБфЦ№ЪМЬѕМўЃЌЪЙ
ЁЁ ЁЁЁЁЗДгІЙ§ГЬАДbЧњЯпНјааЃЌПЩВЩШЁЕФДыЪЉЪЧ(ЁЁ C )
ЁЁЁЁЁЁЁЁЁЁ ЁЁAЃЎЩ§ИпЮТЖШЁЁЁЁЁЁЁЁ BЃЎМгДѓXЕФЭЖШыСП
ЁЁЁЁЁЁЁЁЁЁ ЁЁCЃЎМгДпЛЏМСЁЁЁЁЁЁЁЁ DЃЎдіДѓЬхЛ§
18. (ЩНДѓИНжа2008-2009бЇФъЩЯбЇЦкИпШ§дТПМ) дк100ЁцЪБЃЌНЋ0.50 mol N2O4ЦјЬхЭЈШыЕНЬхЛ§ЁЁ
ЁЁ ЮЊ5.0 LЕФецПеУмБеШнЦїжаСЂМДГіЯжКьзиЩЋЃЌЗДгІНјааЕН2УыЪБЃЌNO2ЕФХЈЖШЮЊ0.02 mol/LЃЌ
ЁЁ 60УыЪБЬхЯЕвбДяЦНКтЃЌДЫЪБШнЦїФкбЙЧПЮЊПЊЪМЕФ1.6БЖЃЌЯТСаЫЕЗЈе§ШЗЕФЪЧ(ЁЁ B )
ЁЁ AЃЎЧА2УывдN2O4ЕФХЈЖШБфЛЏБэЪОЕФЦНОљЗДгІЫйТЪЮЊ0.010 mol/(LЁЄs)
ЁЁ BЃЎдк2УыЪБЬхЯЕФкбЙЧПЮЊПЊЪМЪБЕФ1.1БЖ
ЁЁ CЃЎЦНКтЪБЬхЯЕФкКЌN2O4 ЮЊ0.25mol
ЁЁ DЃЎЦНКтЪБШчЙћбЙЫѕШнЦїЬхЛ§ЃЌдђПЩвдЬсИпN2O4ЕФзЊЛЏТЪ
17. (ЩНДѓИНжа2008-2009бЇФъЩЯбЇЦкИпШ§дТПМ)дкШнЛ§вЛЖЈЕФУмБеШнЦїжаЃЌЗДгІ2A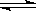 B(g)ЁЁ
B(g)ЁЁ
ЁЁ +C(g)ДяЕНЦНКтКѓЃЌЩ§ИпЮТЖШШнЦїФкЦјЬхЕФУмЖШдіДѓЃЌдђЯТСаа№Ъіе§ШЗЕФЪЧ(ЁЁ A )
ЁЁA.е§ЗДгІЪЧЮќШШЗДгІЃЌЧвAВЛЪЧЦјЬЌ
ЁЁB.е§ЗДгІЪЧЗХШШЗДгІЃЌЧвAЪЧЦјЬЌ
ЁЁC.ЦфЫћЬѕМўВЛБфЃЌМгШыЩйСПAЃЌИУЦНКтЯђе§ЗДгІЗНЯђвЦЖЏ
ЁЁD. ИФБфбЙЧПЖдИУЦНКтЕФвЦЖЏЮогАЯь
15. (ЩНДѓИНжа2008-2009бЇФъЩЯбЇЦкИпШ§дТПМ)Яђ50mL 18mol/LЕФСђЫсжаМгШызуСПЕФЭЦЌМгЁЁ
ЁЁ ШШЃЌГфЗжЗДгІКѓЃЌБЛЛЙдЕФСђЫсЪЧЁЁ(ЁЁ A )ЁЁ
AЃЎаЁгк0.45molЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ BЃЎ0.45mol
CЃЎНщгк0.45molКЭ0.90molжЎМфЁЁЁЁЁЁ DЃЎДѓгк0.90mol
16 (ЩНДѓИНжа2008-2009бЇФъЩЯбЇЦкИпШ§дТПМ)ЯТСаЫЕЗЈжаПЩвдГфЗжЫЕУїЗДгІ
P(g)+Q(g)  R(g)+S(g)дкКуЮТЬѕМўЯТвбДяЕНЦНКтзДЬЌЕФЪЧ(ЁЁ B )
R(g)+S(g)дкКуЮТЬѕМўЯТвбДяЕНЦНКтзДЬЌЕФЪЧ(ЁЁ B )
AЃЎШнЦїФкЕФбЙЧПВЛЫцЪБМфЕФБфЛЏЖјИФБфЁЁЁЁ BЃЎPКЭRЕФЩњГЩЫйТЪЯрЕШ
CЃЎЛьКЯЦјЬхЕФУмЖШВЛдйЫцЪБМфЖјБфЛЏЁЁЁЁЁЁ DЃЎШнЦїФкPЁЂQЁЂRЁЂSЙВДц
14ЃЎ(ЩНЖЋЪЁСФГЧвЛжа08-09бЇФъЖШЩЯбЇЦкИпШ§ЦкФЉзлКЯВтЪд)ШчгвЭМЃЌдквЛЖЈЮТЖШЯТЃЌЂёЮЊКубЙУмБеШнЦї,ЂђЮЊКуШнУмБеШнЦїЁЃдкЂёЁЂЂђжаЗжБ№МгШы2 mol AКЭ2 mol B,Ц№ЪМЪБШнЦїЬхЛ§ОљЮЊV L,ЗЂЩњШчЯТЗДгІВЂДяЕНЛЏбЇЦНКтзДЬЌЃК 2AЪЎB xC(g)ЃЌЦНКтЪБСНШнЦїжаAЁЂBЁЂCЕФЮяжЪЕФСПжЎБШОљЮЊ1ЃК3ЃК6ЁЃЯТСаЫЕЗЈвЛЖЈе§ШЗЕФЪЧ( ACЁЁ )
xC(g)ЃЌЦНКтЪБСНШнЦїжаAЁЂBЁЂCЕФЮяжЪЕФСПжЎБШОљЮЊ1ЃК3ЃК6ЁЃЯТСаЫЕЗЈвЛЖЈе§ШЗЕФЪЧ( ACЁЁ )
 ЁЁ AЃЎxЕФжЕЮЊ3ЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
ЁЁ AЃЎxЕФжЕЮЊ3ЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
ЁЁ BЃЎBЮяжЪПЩЮЊЙЬЬхЛђвКЬх
ЁЁ CЃЎЂёЁЂЂђШнЦїжаДгЦ№ЪМЕНЦНКтЫљашЪБМфЯрЭЌЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
ЁЁ DЃЎЦНКтЪБЃЌЂёШнЦїЕФЬхЛ§аЁгкV L
13ЁЂ(ЩНЖЋЪЁЮФЕЧЪаЬьИЃЩНжабЇ2009НьИпШ§ЕкЫФДЮдТПМ)дкШнЛ§ВЛБфЕФУмБеШнЦїжаДцдкШчЯТ
ЁЁЁЁ ЗДгІЃК2SO2(g)+O2(g) 2SO3(g)ЃЛЁїH=ЃQkJ/mol(QЃО0)ЃЌФГбаОПаЁзщбаОПСЫ
2SO3(g)ЃЛЁїH=ЃQkJ/mol(QЃО0)ЃЌФГбаОПаЁзщбаОПСЫ
ЁЁЁЁ ЦфЫћЬѕМўВЛБфЪБЃЌИФБфФГвЛЬѕМўЖдЩЯЪіЗДгІЕФгАЯьЃЌЯТСаЗжЮіе§ШЗЕФЪЧ(B )
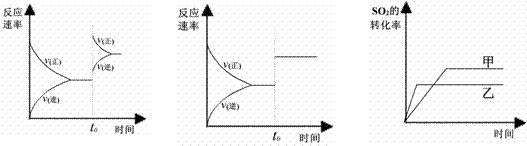
IЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ IIЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ IIIЁЁЁЁ
AЃЎЭМIбаОПЕФЪЧt0ЪБПЬдіДѓO2ЕФХЈЖШЖдЗДгІЫйТЪЕФгАЯь
BЃЎЭМIIбаОПЕФЪЧt0ЪБПЬМгШыДпЛЏМСКѓЖдЗДгІЫйТЪЕФгАЯь
CЃЎЭМIIIбаОПЕФЪЧДпЛЏМСЖдЦНКтЕФгАЯьЃЌЧвМзЕФДпЛЏаЇТЪБШввИп
DЃЎЭМIIIбаОПЕФЪЧЮТЖШЖдЛЏбЇЦНКтЕФгАЯьЃЌЧвввЕФЮТЖШНЯЕЭ
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com