
16.(12分)现欲配制100 mL 1.0 mol/L的硫酸铜(CuSO4)溶液,试求:
(1) 若用无水硫酸铜配制,则需要无水硫酸铜粉末的质量是多少?
(2) 若用5.0 mol/L CuSO4溶液配制,则需要该溶液多少毫升?
(3) 若用胆矾(CuSO4 5H2O)配制,则需要胆矾的质量是多少?
合肥一中09-10学年高一上学期第一阶段测试
15.(20分)为除去粗盐中的Ca2+、Mg2+、SO42-以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量)
 (1)判断BaCl2已过量的方法是
。
(1)判断BaCl2已过量的方法是
。
(2)第④步中,写出相应的化学方程式(设粗盐溶液中Ca2+的主要存在形式为CaCl2)
; ___________________________________.
 (3)在 中填写所使用除杂试剂的化学式__________,在( )中的操作名称是_______。
(3)在 中填写所使用除杂试剂的化学式__________,在( )中的操作名称是_______。
(4)从实验设计方案优化的角度分析步骤②和④可否颠倒____________(填“是”或“否”,如果“否”,请说明理由。)原因是:_______________________________________________;
步骤③和④可否颠倒____________。
(5)若先用盐酸再进行操作⑤,将对实验结果产生影响,其原因是:
__________ 。
14.(16分)右图为实验室某浓盐酸试剂瓶标签上的有关数据,
|
⑴该浓盐酸中HCl的物质的量浓度为___________ mol·L-1 。
⑵取用任意体积的该盐酸溶液时,下列物理量中不随所取体
积的多少而变化的是_______________。
A.溶液中HCl的物质的量 B.溶液的浓度 C.溶液中Cl-的数目 D.溶液的密度
⑶某学生欲用上述浓盐酸和蒸馏水配制500 mL物质的量浓度为0.400 mol·L-1的稀盐酸。
①该学生需要量取____________ mL上述浓盐酸进行配制。
②在配制过程中,下列实验操作对所配制的稀盐酸的物质的量浓度有何影响?
(在空格中填 “偏大”、填 “偏小”或“无影响”)。
I、定容时俯视观察凹液面______________;
II、定容后经振荡、摇匀、静置,发现液面下降,再加适量的蒸馏水_______________。
13.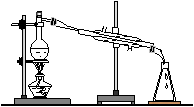 (16分)掌握仪器的名称、组装及使用方法
(16分)掌握仪器的名称、组装及使用方法
是中学化学实验的基础,下图为两套实验装置。
⑴写出下列仪器的名称:
①____________;②_____________;
④__________; I II
⑵仪器①-④中,使用时必须检查是否漏水的有______。(填序号)
⑶若利用装置I分离四氯化碳和乙醇的混合物,还缺少的仪器是_________,将仪器补充完整后进行的实验操作的名称为_____________ 。现需配制250 mL 0.2 mol/L NaCl溶液,装置II是某同学转移溶液的示意图,图中的错误是______________、_________________ 。
12.下列溶液中的氯离子数目与50 mL 1 mol·L-1的AlCl3溶液中氯离子数目相等的是 ( )
A.150 mL 1 mol·L-1的NaCl B.75 mL 1 mol·L-1的FeCl3
C.150 mL 3 mol·L-1的KCl D.75 mL 2 mol·L-1的CaCl2
11.下列叙述正确的是 ( )
A.同温同压下,相同体积的物质,其物质的量一定相等
B.任何条件下,等体积的甲烷和一氧化碳所含的分子数一定相等
C.1L一氧化碳气体一定比1L氧气的质量小
D.相同条件下的一氧化碳气体和氮气,若体积相等,则质量一定相等
10.某位同学配制一定物质的量浓度的NaOH溶液时,造成所配溶液浓度偏高的原因是( )
A.所用NaOH已经潮解
B.向容量瓶中加水未到刻度线
C.有少量NaOH溶液残留在烧杯里
D.用带游码的托盘天平称2.4gNaOH时误用了“左码右物”方法
9.除去下列物质中的杂质,所用试剂和方法不正确的是 ( )
|
|
物质 |
杂质 |
除杂质所用试剂和方法 |
|
A |
KCl溶液 |
I2 |
CCl4,萃取 |
|
B |
KNO3 |
K2SO4 |
Ba(NO3)2溶液,过滤 |
|
C |
Cu |
CuO |
盐酸,过滤 |
|
D |
CaCO3 |
CaO |
盐酸,过滤 |
8.有以下四种物质:① 标况下11.2L CO2 ②1g H2 ③1.204×1024个N2 ④4℃时18 mLH2O,
下列说法不正确的是: ( )
A.分子个数:③>④>①=② B.原子个数:③>④>①>②
C. 体 积: ③>④>①=② D. 质 量: ③>①>④>②
7.下列实验操作中错误的是 ( )
A.蒸发操作时,不能等到混合物中的水分完全蒸干后,才停止加热
B.蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的支管口处
C.分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出
D.萃取操作时,应选择有机萃取剂,且萃取剂的密度必须比水大
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com