
32、(17分)工业上制取CuCl2的生产流程如下:

请结合下表数据,回答问题:
|
物 质 |
Fe(OH)2 |
Cu(OH)2 |
Fe(OH)3 |
|
溶度积/25℃ |
8.0×10-16 |
2.2×10-20 |
4.0×10-38 |
|
完全沉淀时的pH范围 |
≥9.6 |
≥6.4 |
3-4 |
(1)写出下列离子方程式:
A→B ; B→C+D 。
(2)溶液A中加入NaClO的目的是 。
(3)在溶液B中加入CuO的作用是 。
(4)操作①应控制的pH范围是: ;操作②的目的是 。
(5)由Cu(OH)2加入盐酸使Cu(OH)2转变为CuCl2。采用“稍多量盐酸”和“低温蒸干”的目的是 。
31、(16分)环境保护和能源开发是当今社会的热门话题。根据所学化学知识解答下列问题:
⑴在汽车上安装三效催化转化器,可使汽车尾气中的主要污染物(CO、NOx、碳氢化合物)进行相互反应,生成无毒物质,减少汽车尾气污染。
已知:N2(g)+ O2(g)=2NO(g) △H=+180.5 kJ/mol; 2C(s)+ O2(g)=2CO(g) △H=-221.0 kJ/mol;C(s)+ O2(g)=CO2(g) △H=-393.5 kJ/mol
尾气转化的反应之一:2NO(g)+2CO(g)=N2(g)+2CO2(g) △H = 。
请在答题纸中画出这个反应在反应过程中体系能量变化示意图,并进行必要标注:
⑵汽车尾气分析仪对CO的分析是以燃料电池为工作原理,其装置如图所示,该电池中电解质为氧化钇-氧化钠,其中O2-可以在固体介质NASICON中自由移动。
 下列说法错误的是 。
下列说法错误的是 。
A.负极的电极反应式为:CO+O2-―2e-=CO2
B.工作时电极b作正极,O2-由电极a流向电极b
C.工作时电子由电极a通过传感器流向电极b
D.传感器中通过的电流越大,尾气中CO的含量越高
(3)某新型铝-空气燃料电池,以铝为负极,在正极通入空气,若以NaCl溶液或NaOH溶液为电解质溶液,放电时正极反应都为O2+2H2O+4e-=4OH-。那么若以NaOH溶液为电解质溶液,电池负极反应为: ;若以NaCl溶液为电解质溶液,则总反应为: 。
30、(15分)在足量的稀氯化亚铁溶液中,加入1-2滴液溴,振荡后溶液变为黄色。
(1)甲同学认为这不是发生化学反应所致,使溶液变黄色的物质是: (填粒子的化学式,下同);乙同学认为这是发生化学反应所致,使溶液变黄色的物质是 。
(2)现提供以下试剂:
A.酸性高锰酸钾溶液 B.氢氧化钠溶液 C.四氯化碳 D.硫氰化钾溶液.
请判断哪位同学的推断是正确的,并用两种方法加以验证,写出选用的试剂编号及实验中观察到的现象。
|
同学正确 |
选用试剂(填代号) |
实验现象 |
|
第一种方法 |
|
|
|
第二种方法 |
|
|
(3)根据上述实验推测,若在稀溴化亚铁溶液中通入氯气,首先被氧化的离子是 若选用淀粉碘化钾溶液来判断哪位同学的推断是正确的,你认为是否可行? 理由是:
23.下列说法正确的是
A.根据Ksp(AgCl)=1.77×10-10mol2·L-2,Ksp(Ag2CrO4)=1.12×10-12mol3·L-3,可以推知AgCl的溶解度比Ag2CrO4的溶解度大
B.0.1mol·L-1的ZnCl2溶液中通入足量硫化氢气体最终得不到ZnS沉淀是因为溶液中
c(Zn2+)·c(S2-)<Ksp(ZnS)
C.AgCl在10mL 0.01mol·L-1的KCl溶液中比在20mL0.05mol·L-1的AgNO3溶液中溶解的质量大
D.向碳酸钡沉淀中加入稀硫酸,沉淀发生转化,可推知硫酸钡的Ksp比碳酸钡的小
22.草酸(H2C2O4)是二元弱酸,KHC2O4溶液呈酸性。向100mL0.2mol/L的草酸溶液中加入1.68gKOH固体,若溶液体积不变,则对所得溶液中各粒子浓度之间的关系描述正确的是
 A.c(C2O42-)+c(HC2O4-)+c(OH-)=c(K+)+c(H+)
A.c(C2O42-)+c(HC2O4-)+c(OH-)=c(K+)+c(H+)
 B.c(C2O42-)+c(HC2O4-)+c(H2C2O4)=0.2mol/L
B.c(C2O42-)+c(HC2O4-)+c(H2C2O4)=0.2mol/L
 C.c(C2O42-)<c(HC2O4-)<c(H2C2O4)
C.c(C2O42-)<c(HC2O4-)<c(H2C2O4)
 D.c(H+)<c(HC2O4-)<c(C2O42-)<c(K+)
D.c(H+)<c(HC2O4-)<c(C2O42-)<c(K+)
12.已知:CO2(g) + 3H2(g)
 CH3OH(g) + H2O(g)
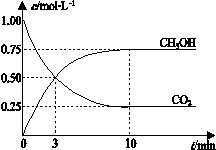
ΔH=-49.0 kJ•mol-1。一定条件下,向体积为1 L的密闭容器中充入1 mol CO2和3 mol H2,测得CO2和CH3OH(g)的浓度随时间变化曲线如右图所示。下列叙述中,正确的是
CH3OH(g) + H2O(g)
ΔH=-49.0 kJ•mol-1。一定条件下,向体积为1 L的密闭容器中充入1 mol CO2和3 mol H2,测得CO2和CH3OH(g)的浓度随时间变化曲线如右图所示。下列叙述中,正确的是
 A.升高温度能使
增大
A.升高温度能使
增大
B.反应达到平衡状态时,CO2的平衡转化率为75%
C.3 min时,用CO2的浓度表示的正反应速率等于
用CH3OH的浓度表示的逆反应速率
D.从反应开始到平衡,H2的平均反应速率
υ(H2)=0.075 mol•L-1•min-1
11.元素X、Y、Z原子序数之和为37,X、Y在同一周期,X+与Z-具有相同的核外电子层结构。下列推测不正确的是
A.同周期元素中X的金属性最强 B.原子半径X>Y,离子半径X+>Z-
C.同族元素中Z的氢化物稳定性最高 D.同周期元素中Y的最高价含氧酸的酸性最强
10.NA代表阿伏加德罗常数。下列有关叙述正确的是
A.将NA个NH3分子气体溶于1L水中得到1mol·L-1的氨水
B.标准状况下,11.2L氦气中约含有NA个氦原子
C.常温下32g含有少量臭氧的氧气中,共含有2NA个氧原子
D.100mL0.1mol·L-1醋酸溶液含有的分子总数一定小于0.01NA
9. 下图所示的实验装置或操作不能达到实验目的的是
下图所示的实验装置或操作不能达到实验目的的是
8.下列叙述不正确的是
A.可用溴的四氯化碳溶液区分直馏汽油和裂化汽油
B.蛋白质溶液中加入浓的硫酸铵溶液会有蛋白质析出
C.甲烷、苯、乙醇、乙酸和酯类都可以发生取代反应
D.棉花和合成纤维的主要成分都是纤维素
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com