
22.(1)
1.880 4分
31、Ⅰ(18分)下图是人体内以丙酮酸为中心的代谢途径,A、B、C、D代表不同物质;①-⑩代表生理过程,请据图回答下列问题:
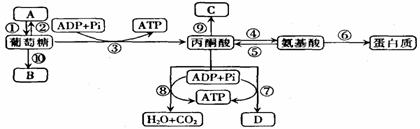
(1)B、C物质分别是 和 。
(2)⑦过程发生在 中,试写出葡萄糖经③⑦过程生成D物质的化学反应式
。若D物质在人体内增多时,参与调节内环境稳态的主要物质是 。
(3)过程⑤在人体内 时会加强。
Ⅱ、(12分)下图为吞噬细胞杀灭细菌的示意图,图中的溶酶体内含有多种水解酶,据图回答:
(1)图中①过程进行的是溶酶体释放水解酶,将细菌分解,该过程属于 免疫。
 (2)有些毒性很强的细菌经过上述过程虽然还不能被清除,但其内部隐藏的
可以被暴露出来,呈递给相应的免疫细胞,使之迅速增殖分化成
。当该细菌在体液中活动时,会被相应的抗体消灭,这属于特异性免疫中的
。
(2)有些毒性很强的细菌经过上述过程虽然还不能被清除,但其内部隐藏的
可以被暴露出来,呈递给相应的免疫细胞,使之迅速增殖分化成
。当该细菌在体液中活动时,会被相应的抗体消灭,这属于特异性免疫中的
。
理综·物理部分答案
选择题
A卷:14.AB
15.B 16.B 17.AC 18.B 19.C 20.C 21.B
B卷:14BC
15.D 16.D 17.BC 18D
19.C 20.A 21A
30.回答下列与细胞有关的实验问题。(12分)
(1)下列4项实验中,需保持细胞生理活性的有__________(填序号)。
①观察叶绿体和原生质的流动
②观察洋葱鳞片叶内表皮细胞中DNA的分布
③探究酵母菌的呼吸方式
④红细胞中血红蛋白的提取和分离
(2)按下面步骤进行质壁分离实验。
步骤一:在洁净的载玻片中央加一滴清水,取一片藓类小叶,盖上盖玻片。
步骤二:从盖玻片一侧滴入0.3g/mL的蔗糖溶液,在盖玻片的另一侧用吸水纸吸引。这样重复几次,使盖玻片下面的藓类小叶浸润在0.3/mL的蔗糖溶液中。
步骤三:在显微镜下观察,结果如图27-1所示。

图27-1
①图27-1中A、B处的颜色分别是__________。
②如果上述实验步骤二中从盖玻片的一侧滴入的是加有伊红(植物细胞不吸收的红色染料)的0.3g/mL的蔗糖溶液,则在显微镜下观察到A、B处颜色分别是_______________________。
③如果将步骤二中浸润在0.3g/mL的蔗糖溶液中的藓类小叶的装片,放在80℃条件下处理一段时间(装片中的藓类小叶保持在0.3/mL的蔗糖溶液中)。在显微镜下清晰地观察到细胞结构后,为更准确地判断A处颜色,对显微镜的操作方法是____________________、________________________________________。
如果A处呈绿色,可能的原因是________________________________________。
29.(15分)
(1)下列物质属于非电解质的是 ,属于弱电解质的是
①氨水 ②SO2 ③CI2 ④甲酸 ⑤BaSO4 ⑥CH3CH2OH ⑦H2O ⑧NaHCO3
(2)将浓度均为2mol·L-1的AgNO3与Cu(NO3)2溶液各0.5L混合,以铜为电极进行电解一段时间之后,阴极上有1.6g铜析出.
回答下列问题:
①阴极上是否有银析出? (填“有”或“没有”).若有,析出银的质量为 g
②直流电源已输出 mol电子.
③溶液中Cu2+的物质的量浓度为 mol·L-1
28.(15分)实验室里临时需要用NaOH溶液和CO2来制取纯Na2CO3溶液.已知CO2气体通入NaOH溶液过程中极易过量生成NaHCO3,且无明显现象.
实验室有下列试剂:①未知浓度的NaOH溶液;②37﹪的盐酸;③37﹪的硫酸;④14﹪的盐酸;⑤大理石;⑥K2CO3固体;⑦碱式碳酸铜.
实验室有以下仪器:铁架台,启普发生器,量筒,烧杯,橡皮管,玻璃导管,分液漏斗.已知下表中各物质在常温时的溶解度(g/100g·H2O)
|
Na2CO3 |
NaHCO3 |
NaCl |
Na2SO4 |
NaHSO4 |
NaOH |
|
15.9 |
8.4 |
35 |
35.5 |
20 |
40 |
⑴.实验应选用的仪器:除启普发生器,橡皮管,玻璃导管外,还需要: .
⑵.为了保证制得的Na2CO3溶液尽量纯,应选用的药品(填编号):除①外,还需要: .
⑶.简要叙述实验步骤,直到制得纯Na2CO3溶液(仪器安装可省略).
.
⑷.据实验给出的溶解度表,求出当NaOH溶液中溶质的质量分数大于多少时,在通入CO2过程中会有晶体析出(写出计算步骤和必要的文字说明)?
27.(15分)卤代烃R-Cl在一定条件下可发生如下反应:R-Cl+KCN→R-CN+KCl;
R-CN+2H2O+H+→R-COOH+NH4+ ,以乙烯为原料经过下图所示的反应可制取有机物w(A、B、C、D、E均为烃的衍生物)
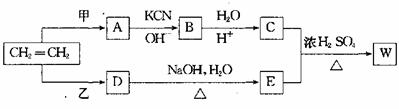
(1)若甲为Cl2,乙为HCl,A和D两种物质的关系是
①同一物质 ② 同系物 ③ 同分异构体 ④ 以上都不对
(2)若甲为HCl,乙为Cl2,生成物W的分子式为C5H10O3,则W的结构简式为 。
(3)若甲为Cl2,乙为Br2 。按下列要求写出C+E→W的化学方程式:
①W为最小环状分子 。
②W为高分子 。
26.(15分)
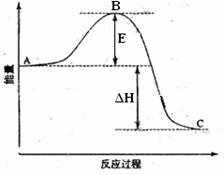
2SO2(g)+O2(g) =2SO3(g)反应过程的能量变化如图所示。已知1mol SO2(g)氧化为1mol SO3的ΔH=-99kJ·mol-1.请回答下列问题:
 (1)图中A、C分别表示 、 ,E的大小对该反应的反应热有无影响? 。该反应通常用V2O5作催化剂,加V2O5会使图中B点升高还是降低? ,理由是 ;
(1)图中A、C分别表示 、 ,E的大小对该反应的反应热有无影响? 。该反应通常用V2O5作催化剂,加V2O5会使图中B点升高还是降低? ,理由是 ;
 (2)图中△H= KJ·mol-1;
(2)图中△H= KJ·mol-1;
 (3)V2O5的催化循环机理可能为:V2O5氧化SO2时,自身被还原为四价钒化合物;四价钒化合物再被氧气氧化。写出该催化循环机理的化学方程式 ;
(3)V2O5的催化循环机理可能为:V2O5氧化SO2时,自身被还原为四价钒化合物;四价钒化合物再被氧气氧化。写出该催化循环机理的化学方程式 ;
 (4)如果反应速率υ(SO2)为0.05 mol·L-1·min-1,则υ(O2)= mol·L-1·min-1
(4)如果反应速率υ(SO2)为0.05 mol·L-1·min-1,则υ(O2)= mol·L-1·min-1
 (5)已知单质硫的燃烧热为296 KJ·mol-1,计算由S(s)生成3 molSO3(g)的△H (要求计算过程)。
(5)已知单质硫的燃烧热为296 KJ·mol-1,计算由S(s)生成3 molSO3(g)的△H (要求计算过程)。
25.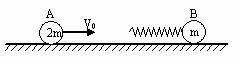 (20分)如图所示,在光滑水平面上,质量为m的小球B连接着一个轻质弹簧,弹簧与小球均处于静止状态.质量为2m的小球A以大小为v0的水平速度向右运动,接触弹簧后逐渐压缩弹簧并使B运动,经过一段时间,A与弹簧分离.
(1)当弹簧压缩至最短时,弹簧的弹性势能EP为多大?
(2)若开始时,在B球的右侧某位置固定一块挡板,在A与弹簧未分离前使B球与挡板发生碰撞,并在碰撞后立即将挡板撤走.设B球与挡板碰撞时间极短,碰后B球的速度大小不变,但方向与原来相反.欲使此后弹簧被压缩到最短时弹簧的弹性势能能达到第(1)问中EP的2.5倍,必须使两球在速度达到多大时与挡板发生碰撞?
(20分)如图所示,在光滑水平面上,质量为m的小球B连接着一个轻质弹簧,弹簧与小球均处于静止状态.质量为2m的小球A以大小为v0的水平速度向右运动,接触弹簧后逐渐压缩弹簧并使B运动,经过一段时间,A与弹簧分离.
(1)当弹簧压缩至最短时,弹簧的弹性势能EP为多大?
(2)若开始时,在B球的右侧某位置固定一块挡板,在A与弹簧未分离前使B球与挡板发生碰撞,并在碰撞后立即将挡板撤走.设B球与挡板碰撞时间极短,碰后B球的速度大小不变,但方向与原来相反.欲使此后弹簧被压缩到最短时弹簧的弹性势能能达到第(1)问中EP的2.5倍,必须使两球在速度达到多大时与挡板发生碰撞?
24.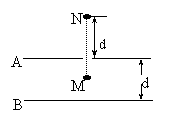 (18分)带有等量异种电荷的两个金属板A和B水平放置,相距为d(d远小于板的长和宽),一个带正电的油滴M悬浮在两板的正中央,处于平衡,油滴的质量为m,带电量为q,如图所示。在油滴的正上方距A板d处有另一个质量也为m的带正电的油滴N,油滴N由静止释放后,可以穿过A板上的小孔,进入两金属板间与油滴M相碰,并立即结合成大油滴(设在碰撞瞬间不考虑重力、电场力的影响)整个装置处于真空环境中,如不计油滴M、N间的库仑力和万有引力以及金属板的厚度,要使油滴N能与M相碰,且结合成大油滴(油滴可视为质点)又不至于与金属板B相碰。求
(1)两个金属板A、B间的电压是多少?哪一个板的电势较高?
(2)油滴N所带电量的范围是多少?
(18分)带有等量异种电荷的两个金属板A和B水平放置,相距为d(d远小于板的长和宽),一个带正电的油滴M悬浮在两板的正中央,处于平衡,油滴的质量为m,带电量为q,如图所示。在油滴的正上方距A板d处有另一个质量也为m的带正电的油滴N,油滴N由静止释放后,可以穿过A板上的小孔,进入两金属板间与油滴M相碰,并立即结合成大油滴(设在碰撞瞬间不考虑重力、电场力的影响)整个装置处于真空环境中,如不计油滴M、N间的库仑力和万有引力以及金属板的厚度,要使油滴N能与M相碰,且结合成大油滴(油滴可视为质点)又不至于与金属板B相碰。求
(1)两个金属板A、B间的电压是多少?哪一个板的电势较高?
(2)油滴N所带电量的范围是多少?
23.(18分)人们到医院检查身体时,其中有一项就是做胸透,我们可以把做胸透的原理等效如下:如图所示,P是一个放射源,从开口处在纸面内向各个方向放出某种粒子(不计重力),而这些粒子最终必须全部垂直射到底片MN这一有效区域,并要求底片MN上每一地方都有粒子到达。假若放射源所放出的是质量为m、电量为q的带正电的粒子,且所有的粒子速率都是v,M与放射源的出口在同一水平面,底片MN竖直放置,底片MN长为L。 为了实现上述目的,我们必须在P的出口处放置一有界匀强磁场。求: (1)匀强磁场的方向 (2)画出所需最小有界匀强磁场的区域,并用阴影表示 (3)匀强磁场的磁感应强度B的大小以及最小有界匀强磁场的面积S

湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com