
12.某混合溶液中所含离子的浓度如下表,则Mn+离子及a值可能为 ( )
|
所含离子 |
NO-3 |
SO2-4 |
H+ |
Na+ |
Mn+ |
|
浓度(mol·L-1) |
3 |
1 |
2 |
1 |
a |
A.Mg2+、1 B.Ba2+、0.5 C.Al3+、1.5 D.Fe2+、2
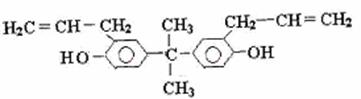 13.据《华盛顿邮报》报道,美国食品与药物管理局2009年10月公布了一份草拟的评估报告,指出塑料奶瓶和婴儿奶粉罐普遍存在的化学物质双酚A(如下图),并不会对婴儿或成人的健康构成威胁。关于双酚A的下列说法正确的是 ( )
13.据《华盛顿邮报》报道,美国食品与药物管理局2009年10月公布了一份草拟的评估报告,指出塑料奶瓶和婴儿奶粉罐普遍存在的化学物质双酚A(如下图),并不会对婴儿或成人的健康构成威胁。关于双酚A的下列说法正确的是 ( )
A.该化合物属于芳香烃
B.该化合物与三氯化铁溶液反应显紫色
C.双酚A不能使溴水褪色,但能使酸性的高锰酸钾溶液褪色
D.1mol双酚A最多可与4mol Br2发生加成反应
11.下列离子方程式正确的是 ( )
A.向次氯酸钙溶液中通入SO2:Ca2++2ClO-+SO2+H2O==CaSO3↓+2HClO
B.向NH4Al(SO4)2溶液中滴入Ba(OH)2溶液恰使SO2-4沉淀完全
NH+4+Al3++2Ba2++2SO2-4+4OH-=Al(OH)3↓+NH3·H2O+2BaSO4↓
C.硫化铜固体中加入硫酸锌稀溶液[已知
Ksp(CuS)<Ksp(ZnS)]:CuS+Zn2+==ZnS+Cu2+
D.向硝酸银溶液中滴加稀氨水至过量:
AgNO3+NH3·H2O==AgOH+NH4NO3
10.常温下pH为2的盐酸,下列叙述正确的是 ( )
A.将10mL该溶液稀释至100mL后,pH小于3
B.向该溶液中加入等体积pH为12的氨水恰好完全中和
C.该溶液中由水电离出的c(H+)(水)×c(OH-)(水)==1×10-14
D.该溶液中盐酸最离的c(H+)与水最离出的c(H+)之比为1010:1
9.四氯化硅还原法是当前制备较高纯度硅的一种方法,有关反应的化学方程式为:
|
SiCl4(g)+2H2(g) ====Si (s)+4HCl(g)。下列说法合理的是 ( )
A.光导纤维的主要成分是硅单质
B.减小压强有利于加快化学反应速率
C.高温下,氢气的还原性强于硅
D.混入少量空气对上述反应无影响
8.甲醇广泛用作燃料电池的燃料,可用天然气来合成,已知:
 ①2CH4(g)+O2(g)=2CO(g)+4H2(g); △H=-71kJ·mol-1
①2CH4(g)+O2(g)=2CO(g)+4H2(g); △H=-71kJ·mol-1
②CO(g)+2H2(g)=CH3OH(l) ; △H=-90.5kJ·mol-1
下列描述错误的是( )
A.CO(g)+2H2(g)==CH3OH(g)
△H>-90.5kJ·mol-1
B.在甲醇燃料电池中,甲醇所在电极为正极
C.CH4(g)+1/2o2(g)===CH3(OH)(l)
△H=-126kJ·mol-1
D.反应①中的能量变化如右图所示
7.在下列给定条件的溶液中,一定能大量共存的离子组是 ( )
A.无色溶液:Ca2+、H+、Cl-、HSO-3
B.强酸性溶液中:Al3+、Fe2+、ClO-、SO2-4
C.c(OH-)=0.1mol·L-1的溶液:Na+、K+、SiO2-3、NO-3
D.含有0.1mol·L-1Ca2+的溶液:Na+、K+、Cl2-3、Cl-
6.在一定条件下,Na2CO3溶液存在水平平衡:CO2-3+H2O HCO-3+OH-。下列说法正确的是 ( )
HCO-3+OH-。下列说法正确的是 ( )
A.稀释溶液,上述可逆反应平衡常数不变
B.通入CO2,溶液pH增大
C.加入NaOH固体,平衡向正反应方向移动
D.升高温度, 不变
不变
4.设NA为阿伏加德罗常数,下列叙述正确的是 ( )
A.40g Ca所含的电子数为NA
B.1L 0.1mol·L-1乙酸溶液中H+数为0.1NA
C.1 mol-CH3所含质子数为9NA
D.标准状况下,22.4L SO3中的分子数为NA
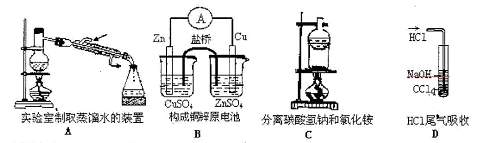 5.下列用途或操作合理的是 ( )
5.下列用途或操作合理的是 ( )
3.分类方法在化学学科的发展中起到了非常重要的作用。下列有关分类标准的说法合理的是 ( )
①根据是否有新物质产生把物质变化分为化学变化和物理变化
②根据分散系是否具有丁达尔现象将分散系分为溶液、胶体和浊液
③根据是否有电子得失把化学反应分为氧化反应和还原反应
④根据电解质在水溶液里是否完全电离,将电解质分为强电解质和弱电解质
A.只有①④ B.只有①② C.只有②③ D.只有③④
2.正确掌握好化学用语是学好化学的基础,下列有关表述正确物是 ( )
A.次氯酸的电子式:
B.质量数为16的氧原子的原子符号:816O
C.乙烯的结构简式:CH2CH2
D.亚硫酸氢根离子的电离方程式:
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com