
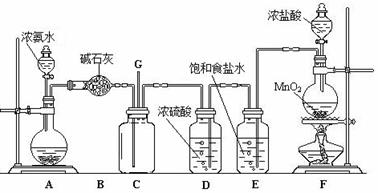
26.(12分)某学生利用以下装置探究氯气与氨气之间的反应。其中A、F分别为氨气和氯气的发生装置,C为纯净干燥的氯气与氨气反应的装置。
请回答下列问题:
(1)装置A中的烧瓶内固体不可以选用 (选填序号)。
A.生石灰 B.碱石灰 C.五氧化二磷 D.烧碱
(2)装置F中发生反应的离子方程式为 ;
(3)B装置的作用 ____________________________________ ;
E装置的作用 _____________________________ ;
(4)装置C内出现浓厚的白烟并在容器内壁凝结,另一生成物是空气的主要成分之一。请写出反应的化学方程式:
_________________________ ;
(5)从装置C的G处逸出的尾气中可能含有黄绿色的有毒气体,如何处理?
。
25.(共6分) 实验室要用98%(ρ=1.84g·cm-3)的硫酸配制3.68mol·L-1的硫酸溶液500mL (1)需98%的硫酸______________mL。 (2)量取一定体积的98%的硫酸后,要配制成3.68mol·L-1 的硫酸溶液500 mL,必须用到的实验仪器是(填写序号)_______________________________。 ①500mL量筒 ②烧杯 ③1000mL容量瓶 ④500mL容量瓶 ⑤天平
⑥胶头滴管 ⑦锥形瓶 ⑧玻璃棒 ⑨酸式滴定管 (3)若配制3.68mol·L-1的硫酸溶液的其他操作均正确,但出现下列错误操作,将使所配制的硫酸溶液浓度偏低的是____________________________(填写序号)。 A.将稀释的硫酸溶液转移至容量瓶后,未洗涤烧杯和玻璃棒。 B.将烧杯内的稀硫酸向容量瓶中转移时,因操作不当使部分稀硫酸溅出瓶外。 C.用胶头滴管向容量瓶中加水时溶液凹液面高于容量瓶刻度,此时立即用滴管将瓶内液体吸出,使溶液凹液面与刻度相切。 D.用胶头滴管加水时,仰视观察溶液凹液面与容量瓶刻度相切。
24.(10分)有编号为A、B、C、D、E的五种透明溶液,它们是盐酸、硝酸银溶液、氯化钡溶液、碳酸钠溶液和硫酸铝溶液。将有关溶液以两两混合法进行实验,相关内容见下表。
|
实验顺序号 |
① |
② |
③ |
④ |
⑤ |
|
混合液编号 |
A+B |
A+C |
A+E |
C+D |
B+D |
|
实验现象 |
有气体生成 |
有沉淀生成 |
有气体、沉淀生成 |
有沉淀生成 |
有沉淀生成 |
则各编号的物质是(填化学式):
A.__________;B.___________;C.___________;D.__________;E.___________。
23.(10分)下表是元素周期表的一部分。表中所列的字母分别代表某一元素。
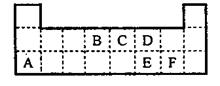
(1)1molA与D的氢化物完全反应产生的气体在标准状况下的体积
为 。
(2)写出B的最高价氧化物的电子式 _________ 。
(3) 写出实验室制取C的氢化物的化学方程式
__________________________ ;
(4)写出工业制取E的最高价氧化物水化物的第一步和第三步反应的化学方程式 ________________ ;
_________________________ ;
(5)表中的另一种金属元素(未标出)的单质G,可以发生如下图所示转化
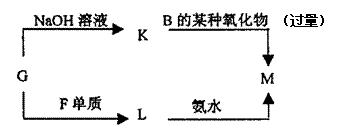
①其中化合物M是一种白色胶状沉淀,则M为(填化学式) ____ ;
②一种新型无机非金属材料由G元素和C元素组成,其化学式为 _ 。
22.(6分)对于A(g)+B(g)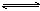 xC(g),反应热为ΔH,根据下图变化分析比较下列各量大小(图中P为压强,T为温度,α(A)表示气体A转化率)
xC(g),反应热为ΔH,根据下图变化分析比较下列各量大小(图中P为压强,T为温度,α(A)表示气体A转化率)
|
(1)图a表示P1________ P2,且x值___________1(填>、<或=。以下同)
(2)图b表示T1________T2,且ΔH________0。
(3)图c,若R1、R2表示压强,则R1__________R2 ,且x_______2。
21.(共10分)(1)物质的量浓度相同的下列溶液, pH值由大到小的顺序是(填序号)_____________________________________。
①H2SO4 ②Ba(OH)2 ③NaCl ④HNO3 ⑤NaHCO3
⑥NaOH ⑦CH3COOH ⑧NH4Cl ⑨Na2CO3
(2)KClO3和浓盐酸在一定温度下反应会生成黄绿色易爆物二氧化氯,其表达式为:
KClO3+ HCl(浓) KCl+ ClO2↑+ Cl2↑+ .
KCl+ ClO2↑+ Cl2↑+ .
①请完成上述方程式(未知化学式及计量数填入框内)。
②浓盐酸在反应中显示出来的性质是:(填写编号) 。
a.只有还原性 b.具有还原性与酸性
c.只有氧化性 d.具有氧化性和酸性
③产生0.1 mol Cl2,则转移电子物质的量为 mol。
④ClO2具有很强的氧化性,因此常被用作消毒剂,其消毒效率(以单位物质的量的物质得到的电子数表示)是Cl2的 倍。
20.下列溶液中:①石灰水 ②H2S溶液 ③KMnO4溶液 ④溴水 ⑤酸化的Ba(NO3)2溶液 ⑥品红溶液,不能区别SO2和CO2气体的是
A.只有① B.①③ C. ①②③⑤ D.②③④⑤
第 Ⅱ 卷(共60分)
19. 据报道,最近摩托罗拉公司研发了一种由甲醇和氧气以及强碱做电解质溶液的新型手机电池,电量可达现在使用的镍氢电池或锂电池的十倍,可连续使用一个月才充一次电。其电池反应为:
据报道,最近摩托罗拉公司研发了一种由甲醇和氧气以及强碱做电解质溶液的新型手机电池,电量可达现在使用的镍氢电池或锂电池的十倍,可连续使用一个月才充一次电。其电池反应为:
2CH3OH+3O2+4OH- 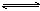 2CO32-+6H2O
2CO32-+6H2O
则下列说法错误的是
A.放电时CH3OH参与反应的电极为正极
B.充电时电解质溶液的pH逐渐增大
C.放电时负极的电极反应为:CH3OH-6e-+8OH-=CO32-+6H2O
D.充电时每生成1 mol CH3OH转移6 mol电子
18.把X溶液逐滴滴入Y溶液中, 与把Y溶液逐滴滴入X溶液中, 产生的实验现象相同的是
A. X是HCl,Y是Na2CO3 B. X是HCl, Y是NaAlO2
C. X是AgNO3,Y是NH3·H2O D. X是Na2SO4, Y是BaCl2
17.对于反应:A+B→C ,下列条件的改变一定能使化学反应速率加快的是
A.增加A的物质的量 B.升高体系的温度
C.增加体系的压强 D.减少C的物质的量
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com