
35.(8分)[生物--现代生物科技专题]
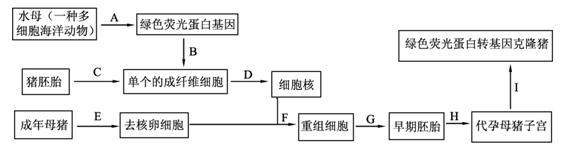
2008年诺贝尔化学奖授予了3位在研究绿色荧光蛋白(GFP)方面做出突出贡献的科学家。绿色荧光蛋白能在蓝光或紫外线的激发下发出荧光,借助GFP发出的荧光可以跟踪蛋白质在细胞内部的移动情况,帮助推断蛋白质的功能。2006年12月26日,我国首例绿色荧光蛋白转基因克隆猪在东北农大降生,具体培育过程如图所示,请据图回答下列问题:
(1)上述过程涉及到的现代生物技术,属于分子水平的是______________。
(2)绿色荧光蛋白基因我们称之为目的基因,在将其导入受体细胞前需将其与载体结合以构建______________,在其过程中需要用到的工具酶有_________________________。B过程最有效地方法是________________。
(3)若要获得单个的成纤维细胞进行培养,需用________________处理猪胚胎的部分组织。
(4)E过程中若要获得大量的卵母细胞需用___________________________方法处理成年母猪。
(5)经过培养得到早期胚胎后可以用__________________技术以获得更多的转基因克隆猪,且在进行H过程之前,需要对代孕母猪进行____________________处理,以给早期胚胎移入受体提供相同的生理环境。
34.(8分)[生物--生物技术实践]
2007年,我国利用秸秆生产车用燃料乙醇的关键技术获得了重大突破,目前已顺利进入工业化实验阶段。实验显示,每4吨秸秆(玉米、麦草秸秆等)可生产1吨燃料乙醇。秸秆的主要成分是纤维素,通过自主创新,我国已经掌握了纤维素的水解技术。请回答:
(1)利用玉米秸秆生产乙醇首先选用_______________酶处理秸秆,使之转化为发酵所需的_________等物质,然后进行发酵,获得乙醇。
(2)在培养分离纤维素分解菌的过程中,接种微生物可以采用平板划线法和____________________法。进行平板划线时,在划线结束后仍然要灼烧接种环,原因是__________________________________________________。
(3)在筛选纤维素分解菌的过程中,通常采用____________染色法,这种方法能够通过颜色反应直接对纤维素分解菌进行筛选。从物理状态看,培养基应使用____________培养基。
(4)在酒精发酵过程中,在不同时间内对发酵液样品进行检测,发现发酵液的pH一直下降,原因是__________________________________________________________。
(5)为了提高乙醇的品质和降低生产成本,研究人员提出可以使用固定化酵母细胞。制备固定化酵母细胞多采用_______________法。
32.(8分)[化学-有机化学基础]
有机物A是最常用的食用油氧化剂,分子式为C10H12O5,可发生如下转化:
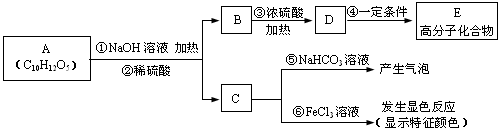
已知B的相对分子质量为60,分子中只含一个甲基。C的结构可表示为: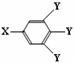 (其中X、Y均为官能团)。请回答下列问题:
(其中X、Y均为官能团)。请回答下列问题:
(1)官能团-X的名称为 ,高聚物E的链节为 。
(2)A的结构简式为 。
(3)反应⑤的化学方程式为 。
(4)C有多种同分异构体,写出期中2种符合下列要求的同分异构体的结构简式 。
a.含有苯环 b.能发生银镜反应 c.不能发生水解反应
(5)从分子结构上看,A具有抗氧化作用的主要原因是 (填序号)。
a.含有苯环 b.含有羰基 c.含有酚羟基
32.(8分)[化学-物质结构与性质]
已知A、B、D、E、F五种元素的原子序数依次增大,其中A原子所处的周期数、族序数都与其原子序数相等;B原子s轨道电子数是p轨道电子数的2倍;D原子中未成对电子数是同周期元素中最多的;E原子L层上有2对成对电子;F原子核外共有21个电子。
请回答下列问题:
(1)写出F元素基态原子的电子排布式为 。
F单质的晶体具有体心立方结构,则在该晶体的一个晶胞中,含有的原子数是________。
(2)B、D、E三种元素的第一电离能最大的是_________(填元素符号),
(3)B与D原子结合形成的晶体目前是世界上最硬的材料,晶体结构类似金刚石,但硬度超过了金刚石,其原因是_________________________________________。
该晶体中任一原子的配位数比E单质晶体中分子的配位数要___________。
31.(8分)[化学-化学与技术]
钢铁工业对促进经济和社会发展起了重要作用。
(1)炼铁高炉分为五部分,铁矿石与高温煤气主要在__________部分发生反应,在__________部分开始生成生铁和炉渣。
(2)炼钢时,除磷的化学方程式为_________;加入硅、锰和铝的目的是_______________________。
(3)不锈钢含有的Cr元素是在炼钢过程的氧吹_______(填“前”或“后”)加入,原因是 ______________________________。
(4)炼铁和炼钢生产中,尾气均含有的主要污染物是______________。从环保和经济角度考虑,上述尾气经处理可用作____________________________________。
30.(18分)硫酸渣是用黄铁矿制造硫酸过程中排出的废渣,主要化学成分为SiO2:约45%,Fe2O3:约40%,Al2O3:约10%,MgO:约5%。目前我国已经在技术上取得突破――用硫酸渣炼铁。
I.某学生探究性学习小组的同学设计了不同的方案,用化学基本知识进行金属元素的提取实验(已知25℃氢氧化镁Ksp=5.6×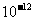 ;氢氧化铁Ksp=3.5×10-38;一水合氨电离常数K=1.8×10-5,其饱和溶液中c(OH-)约为1×10-3mol·L-1)。
;氢氧化铁Ksp=3.5×10-38;一水合氨电离常数K=1.8×10-5,其饱和溶液中c(OH-)约为1×10-3mol·L-1)。
方案一:

请回答:
(1)写出固体E的化学式:__________________。
(2)试剂①是_____________
A.氢氧化钠 B.氧化铝
C.氨水 D.水
(3)若要准确测定溶液的pH是否达到3.7,下列物品中可供使用的是_________
A.石蕊试液 B.广泛pH试纸
C.精密pH试纸 D.pH计
(4)溶液H中溶质的化学式:__________________
(5)要将固体C、固体E和固体G都转化为相应的稳定的氧化物,需进行的实验操作为_________________。
(6)若不考虑溶液体积的变化,请计算溶液H中c(Mg2+)=__________________。
方案二:

请回答:
(7)此方案的主要问题有:____________________________________________
(8)写出由溶液M固体乙这个过程中,最主要化学反应的离子方程式:
_______________________________________________________________
II.为了分析某硫酸渣中铁元素的含量,先将硫酸渣预处理,把铁元素还原成Fe2+ ,再用KMnO4标准溶液在酸性条件下进行氧化还原滴定,反应的离子方程式是:
5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O。
(1)判断到达滴定终点的现象是___________________________________________。
(2)某同学称取2.000g硫酸渣,预处理后在容量瓶中配制成100mL溶液,移取25.00mL,试样溶液,用1.000×10-2mol·L-1KMnO4标准溶液滴定。达到滴定终点时,消耗标准溶液10.00mL,则残留物中铁元素的质量分数是 。
[选做部分]
共8个题,考生必须从中选择2个物理题、1个化学题和1个生物题在答题卡规定的区域作答。
29.(14分)乙醇是重要的化工原料和液体燃料,可以利用下列反应制取乙醇:
2CO2(g) + 6H2(g)\s\up8(催化剂催化剂△CH3CH2OH(g) + 3H2O(g)
(1)写出该反应的平衡常数表达式:K=_________________________。
(2)在一定压强和温度下,在反应物总物质的量相同的情况下,测得该反应的实验数据如下表:

|
500 |
600 |
700 |
800 |
||
|
1.5 |
45 |
33 |
20 |
12 |
||
|
2.0 |
60 |
43 |
28 |
15 |
||
|
3.0 |
83 |
62 |
37 |
22 |
① 该反应是___________反应(填“吸热”或“放热”)。
② 提高氢碳比[n(H2)/n(CO2)],则CO2的转化率___________;化学平衡____________移动,平衡常数K__________(填“增大”、“减小”、或“不变”)。
(3)一种乙醇燃料电池中发生的化学反应为:在酸性溶液中乙醇与氧气作用生成水和二氧化碳。该电池的负极反应式为:_____________________________________。
若以上述燃料电池为电源来电解饱和食盐水,当消耗46g乙醇时,电解产生的H2
体积(标况)为_________L。
(4)25℃、101 kPa下,H2(g)、C2H4(g)和C2H5OH(l)的燃烧热分别是285.8 kJ · mol-1、1411.0 kJ · mol-1和1366.8 kJ · mol-1,请写出由C2H4(g)和H2O(l)反应生成C2H5OH(l)的热化学方程式__________________________________________。
28.(10分)(1)向20.00mL稀氨水中逐滴加入等物质的量浓度的盐酸,请回答相关问题:
①当加入10.00mL盐酸时,溶液中各种离子浓度之间的大小关系为(请在括号中填入离子符号):c( )>c( )>c( )>c( )
②当盐酸与氨水等物质的量反应时,溶液的pH_____7(填“>”或“<”或“=” ,下同)
③当溶液pH=7时,反应所消耗的物质(包括还在溶液中存留的物质)之间的关系为:n(NH3·H2O)_______n(HCl),溶液中c( NH4+)_______c(Cl-)。
(2)已知某弱酸的酸式酸根离子HB-既能发生电离,又能发生水解,请通过实验确定HB-离子是电离程度大还是水解程度大?请简述实验过程和结论。
_____________________________________________________________________
_____________________________________________________________________
27.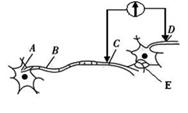 (16分)回答下列有关生物生命活动调节的相关问题:
(16分)回答下列有关生物生命活动调节的相关问题:
(1)若在右图中C和D两点的细胞膜表面安放电极,
中间接记录仪(电流左进右出为+),当信号
在神经细胞间传递时,检测到的结果是( )

(2)在外界环境发生剧烈变化的情况下,人体的内环境仍能维持稳态。当环境温度高于38℃时,人体只有通过__________方式散热,该过程的调节方式是以_____________为主。人在炎热环境中大量出汗后,__________细胞产生兴奋,传导至大脑皮层产生渴觉,同时血液中的抗利尿激素___________。
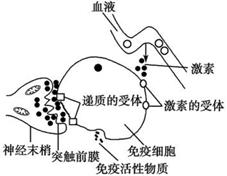 (3)科学研究表明:精神因素(焦虑、紧张等的心理应激)会使T细胞活性下降,对病毒、真菌感染的抵抗能力和对肿瘤细胞的监控能力下降,还间接引起机体生成抗体的能力降低。下图表示神经、免疫、内分泌三大系统相互调节的部分示意图,请据图回答:
(3)科学研究表明:精神因素(焦虑、紧张等的心理应激)会使T细胞活性下降,对病毒、真菌感染的抵抗能力和对肿瘤细胞的监控能力下降,还间接引起机体生成抗体的能力降低。下图表示神经、免疫、内分泌三大系统相互调节的部分示意图,请据图回答:
①精神因素能使T细胞活性下降,导致机体生成抗体能力降低的原因是
______________________________。
②由图可知,神经系统可通过突触前膜 ,直接调节免疫器官或免疫细胞的活动,还可通过有关激素间接调节免疫器官或免疫细胞的活动。
③维持机体稳态离不开细胞间的信息交流,动物细胞间进行信息交流的途径有:一是通过 (至少填两种)等信息分子经体液运输并作用于靶细胞来实现;二是通过细胞间的接触实现信息交流。吞噬细胞将抗原呈递给T细胞是通过 途径实现的。
(4)某同学认为一种植物(X植物)的提取液对SARS病毒有抑制作用,他以小白鼠为研究材料设计了下面的实验进行证明:
实验步骤:
①选择一只健康的小白鼠,让小白鼠感染SARS病毒;
②给喂养小白鼠的饲料中加入一定量的X植物提取液,观察小白鼠是否出现患病症状;我们认为该同学的实验存在明显的不科学之处,请指出两点:
① ;
② ;
26.(17分) 请回答下列有关遗传问题:
 Ⅰ.2009年诺贝尔生理学或医学奖授予因发现端粒和端粒酶如何保护染色体的三位学者。端粒(右图中染色体两端所示)通常是由富含鸟嘌呤核苷酸(G)的短的串联重复序列组成。它们能防止不同染色体末端发生错误融合。但是,细胞每分裂一次,端粒就会丢失一部分;在细胞衰老过程中端粒逐渐变小。端粒
Ⅰ.2009年诺贝尔生理学或医学奖授予因发现端粒和端粒酶如何保护染色体的三位学者。端粒(右图中染色体两端所示)通常是由富含鸟嘌呤核苷酸(G)的短的串联重复序列组成。它们能防止不同染色体末端发生错误融合。但是,细胞每分裂一次,端粒就会丢失一部分;在细胞衰老过程中端粒逐渐变小。端粒
酶可利用某段RNA序列作为模板合成端粒DNA,对端
粒有延伸作用。
(1)非同源染色体末端发生错误融合属于染色体结构变
异中的_________________,结果使染色体上基因
的________________________发生改变。
(2)从功能上看,端粒酶属于__________________酶。
(3)如果正常体细胞中不存在端粒酶的活性,你认为新
复制出的DNA与亲代DNA完全相同吗?______
______________________。体外培养正常组织细胞,
细胞中端粒长度与细胞增殖能力呈______________
(正相关、负相关)关系。
 Ⅱ.正常小鼠体内常染色体上的B基因编码胱硫醚γ-裂解酶(G酶),体液中的H2S主要由G酶催化产生。为了研究G酶的功能,现需要选育基因型为B- B-的小鼠。选育时可通过将小鼠一条常染色体上的B基因去除,培育出一只基因型为B+ B- 的雄性小鼠(B+ 表示具有B基因,B- 表示去除了
Ⅱ.正常小鼠体内常染色体上的B基因编码胱硫醚γ-裂解酶(G酶),体液中的H2S主要由G酶催化产生。为了研究G酶的功能,现需要选育基因型为B- B-的小鼠。选育时可通过将小鼠一条常染色体上的B基因去除,培育出一只基因型为B+ B- 的雄性小鼠(B+ 表示具有B基因,B- 表示去除了
B基因,B+ 和B- 不是显隐性关系)。请回答:
(1)若在右图中A点将核DNA带上同位素标记
后放在不含同位素标记的地方培养,则在GH
段可检测到有放射性的脱氧核苷酸链占
__ _ ,有放射性的精子所占的比例为
__________。
(2)B基因控制G酶的合成,其中翻译过程在细胞质的核糖体上通过tRNA上的___________与mRNA上的相应碱基识别,将氨基酸转移到肽链上。
(3)右图表示不同基因型小鼠血浆中G酶浓 度和
度和
H2S浓度的关系。据图描述B+ B+ 和B+ B-
个体的基因型、G酶浓度与H2S浓度
之间的关系:__________________________。
B- B-个体的血浆中没有G酶而仍有少量
H2S产生,可能的原因是___________________。
 (4)以该B+ B- 雄性小鼠与正常小鼠(B+ B+ )为亲本,进行杂交育种,选育B- B- 雌性小鼠。请将育种过程补充完整。
(4)以该B+ B- 雄性小鼠与正常小鼠(B+ B+ )为亲本,进行杂交育种,选育B- B- 雌性小鼠。请将育种过程补充完整。
第一步:
第二步:(用遗传图解表示,其中表现型不作要求。)
第三步:从子二代雌性小鼠中选出B- B-小鼠,选择的方法是__________________________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com