
13.  (1) 志士仁人,____________________,____________________。(《论语•卫灵公》)
(2) ____________________,则凡可以辟患者何不为也?(《孟子•鱼我所欲也》)
(3) 仰观宇宙之大,____________________。(王羲之《兰亭集序》)
(4) ____________________。独上高楼,望尽天涯路。(晏殊《鹊踏枝》)
(5) ____________________,暗香浮动月黄昏。( 林逋《山园小梅》)
(6) 其两膝相比者,____________________。(魏学洢《核舟记》)
(7) 位卑则足羞,____________________。(韩愈《师说》)
(1) 志士仁人,____________________,____________________。(《论语•卫灵公》)
(2) ____________________,则凡可以辟患者何不为也?(《孟子•鱼我所欲也》)
(3) 仰观宇宙之大,____________________。(王羲之《兰亭集序》)
(4) ____________________。独上高楼,望尽天涯路。(晏殊《鹊踏枝》)
(5) ____________________,暗香浮动月黄昏。( 林逋《山园小梅》)
(6) 其两膝相比者,____________________。(魏学洢《核舟记》)
(7) 位卑则足羞,____________________。(韩愈《师说》)
21.(9分)将2.5g碳酸钠、碳酸氢钠和氢氧化钠的固体混合物完全溶解于水,制成稀溶液,然后向该溶液中逐滴加入1mol·L-1的盐酸,所加入盐酸的体积与产生CO2的体积(标准状况)关系如下图所示:
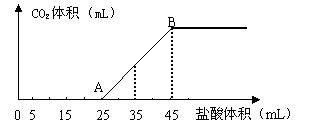





(1)写出OA段所发生反应的离子方程式
、
。
(2)当加入35mL盐酸时,产生CO2的体积为
mL(标准状况)。
(3)原混合物中NaOH的质量为
g,碳酸钠的质量分数为
。
合肥一六八中学复读年级第二次段考
20. (12分)硫酸亚铁晶体(FeSO4·7H2O)在医药上作补血剂。某课外小组测定该补血剂中铁元素的含量。实验步骤如下:
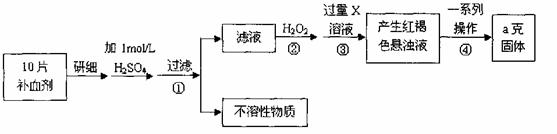
请回答下列问题:
(1)步骤②加入过量H2O2的目的:
(2)步骤③中反应的离子方程式:
(3)步骤④中一系列处理的操作步骤:过滤、 、灼烧、 、称量。
(4)若实验无损耗,则每片补血剂含铁元素的质量 g(用含a的代数式表示)。
(5)该小组有些同学认为用KMnO4溶液滴定也能进行铁元素含量的测定。
(5Fe2++MnO4-+8H+ = 5Fe3++Mn2++4H2O)
①实验前,首先要精确配制一定物质的量浓度的KMnO4溶液250mL,配制时需要的仪器除天平、玻璃棒、烧杯、胶头滴管外,还需
②上述实验中的KMnO4溶液需要酸化,用于酸化的酸是 。
a.稀硝酸 b.稀硫酸 c.稀盐酸 d.浓硝酸
③某同学设计的下列滴定方式中,最合理的是 (夹持部分略去)(填字母序号)
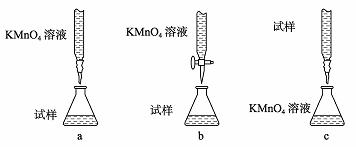
(6)正常人每天应补充14mg左右的铁。其中绝大部分来自于食物。如果全部通过服用含FeSO4·7H2O的片剂来补充铁,则正常人每天服需用 片含FeSO4·7H2O的片剂。
19.(12分)现有A、B、C、D、E五种强电解质,它们在水中可电离产生下列离子(各种离子不重复)。
|
阳离子 |
H+、Na+、A13+、Ag+、Ba2+ |
|
阴离子 |
OH-、C1-、CO32-、NO3-、SO42- |
已知:①A、B两溶液呈碱性;C、D、E溶液呈酸性。
②A溶液与E溶液反应既有气体又有沉淀产生;A溶液与C溶液反应只有气体产生(沉淀包括微溶物,下同)。
③D溶液与另外四种溶液反应都能产生沉淀; C只能与D反应产生沉淀。
试回答下列问题:
(1) 写出化学式:A___________ B___________ D_________
(2) E溶液呈酸性的原因是:(用离子方程式表示)_______________________________
(3 ) 将C溶液逐滴加入等体积、等物质的量浓度的A溶液中,反应后溶液中各种离子浓度由大到小的顺序为: 。
(4 )在100mL0.1mol·L-1 E溶液中,逐滴加入35mL 2mol·L-1NaOH溶液,最终得到沉淀物质的量为 mol
18.(13分)化工生产中常常用到“三酸两碱”,“三酸”指硝酸、硫酸和盐酸,“两碱”指烧碱和纯碱。
(1)从物质的分类角度看,不恰当的一种物质是 (写化学式)
(2)“三酸”与“两碱”之间均可反应,若用化学方程式表示有六个(酸过量时),若用离子方程式表示却只有两个,请写出这两个离子方程式(酸过量时)
、 。
(3)烧碱、纯碱均可吸收CO2,当含0.1molNaOH的溶液吸收一定量CO2后,将溶液低温蒸干得到固体的组成可能有四种情况。按吸收CO2由少到多的顺序,四种固体组成的化学式分别是:
16.下列关系图中,A是一种正盐,B是气态氢化物,C是单质,F是强酸。当X无论是强酸还是强碱时都有如下转化关系(其他反应产物及反应所需条件均已略去),当X是强碱时,过量的B跟Cl2反应除生成C外,另一产物是盐酸盐。
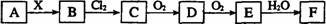
下列说法中不正确的是( )
A.当X是强酸时,A、B、C、D、E、F中均含同一种元素,F可能是H2SO4
B.当X是强碱时,A、B、C、D、E、F中均含同一种元素,F是HNO3
C.无论X是强酸还是强碱时,上面的一系列反应中都需要经历3个化合反应
D.A是一种离子化合物
第Ⅱ卷 (非选择题共52分)
17(6分)下列三组物质中,均有一种物质的类别与其它三种不同
A.MgO、Na2O、CO2、CuO
B.HCl、H2O、H2SO4、HNO3
C.NaOH、Na2CO3、KOH、Cu(OH)2
(1)三种物质依次是(填化学式):A B C 。
(2)A、B、C三种物质相互作用可生成一种新物质,该反应 氧化还原反应(填“是”或“不是”)。这种新物质与盐酸反应的离子方程式为________________ 。
15.一定体积0.01mol/L的稀硝酸溶液恰好能氧化一定质量的铁、铝混合物,已知两种金属均被氧化为最高价态,还原产物只有NO。若用0.01mol/L的NaOH溶液溶解相同质量的该混合物,当反应完全时所需氢氧化钠溶液的体积是稀硝酸溶液的1/5,则样品中铁、铝的物质的量之比为
A.2:3 B.1:3 C.1:4 D.5:3
14. (NH4)2SO4在一定条件下发生如下反应:4(NH4)2SO4=N2↑+6NH3↑+3SO2↑+SO3↑+7H2O 将反应后的混合气体通入足量的BaCl2溶液,产生的沉淀为
A.BaSO4 B.BaSO3 C.BaSO4 和BaSO3 D.BaS
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com