
37、[化学--选修物质结构与性质](15分)
(1)请写出Cr原子基态的电子排布式: _______。
 (2)H3O+的空间构型是 ,其中O原子呈 _杂化。
(2)H3O+的空间构型是 ,其中O原子呈 _杂化。
(3)Fe(CO)5常温下呈液态,熔点为-20.5℃,沸点为103℃,
易溶于非极性溶剂,据此可判断Fe(CO)5晶体属于 晶体。
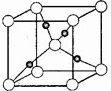
(4)某铜的氧化物晶体的晶胞结构如图所示,其中小球表示Cu
原子,在1个晶胞包含的氧原子数目为 。
36、[化学--选修化学与技术](15分)
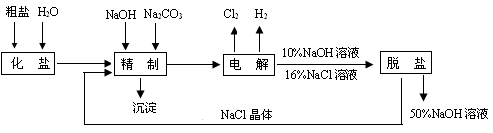 氯碱厂电解饱和食盐水制取NaOH的工艺流程示意图如下:
氯碱厂电解饱和食盐水制取NaOH的工艺流程示意图如下:
依据上图,完成下列填空:
(1) 在电解过程中,与电源正极相连的电极上所发生反应的方程式为: 。
与电源负极相连的电极附近溶液pH 。(填“不变”“增大”或“减小”)
(2)如果粗盐中SO42-含量较高,必须添加钡试剂除去SO42-,该试剂可以选 。
a.Ba(OH)2 b.Ba(NO3)2 c.BaCl2
(3)为有效除去Ca2+、Mg2+、SO42-,加入试剂的合理顺序为 (选a、b、c,多选扣分)。
a.先加NaOH,后加Na2CO3,再加钡试剂
b.先加NaOH,后加钡试剂,再加Na2CO3
c.先加钡试剂,后加NaOH,再加Na2CO3
(4)在用阳离子交换膜法电解食盐水时,电解槽分隔为阳极区和阴极区,防止Cl2与NaOH反应;采用无隔膜电解冷的食盐水时,Cl2与NaOH充分反应,产物最终仅有NaClO和H2,相应的化学反应方程式为 、 。
35、[物理--3-5 模块]
(1) (6分)下列说法正确的是:
A.卢瑟福通过α粒子散射实验确定了原子核是由质子和中子组成的
B.γ射线是核反应过程中产生的一种高速运动的粒子流,它的穿透能力很差
C.铀235能自发的发生裂变反应,但因半衰期不变,所以秦山核电站的发电功率也是固定不变的
D.爱因斯坦质能方程E=mc2表明,物体具有的能量和它的质量之间有简单的正比关系,但不能说核反应中质量会转化成能量
(2) (9分)如图所示,光滑水平面上,轻弹簧两端分别拴住质量均为m的小物块A和B,B物块靠着竖直墙壁。今用水平外力缓慢推A,使A、B间弹簧压缩,当压缩到弹簧的弹性势能为E时撤去此水平外力,让A和B在水平面上运动。求:
①当弹簧达到最大长度时A、B的速度大小;
 ②当B离开墙壁以后的运动过程中,弹簧弹性势能的最大值。
②当B离开墙壁以后的运动过程中,弹簧弹性势能的最大值。
34、[物理--3-4 模块]
(1)(6分)下列说法中正确的是:
A.次声波是频率低于20 Hz的声波,它比超声波更易发生衍射
B.托马斯•杨通过光的单缝衍射实验,证明了光是一种波
C.光导纤维丝内芯材料的折射率比外套材料的折射率大
D.在光的双缝干涉实验中,若仅将入射光由绿光改为红光,则干涉条纹间距变窄
(2)(9分)如图为一列简谐横波在t1=0时刻的波形图象,此时波中质点M正处于平衡位置,运动方向沿y轴负方向。到t2=0.55s时质点M恰好第三次到达y轴正方向最大位移处。试求:①该波传播方向及波速大小;
②从t1=0到t3=1.2s,波中质点N走过的路程和相对于平衡位置的位移分别是多少?

33、[物理--3-3 模块]
(1)(6分)下列说法正确的是:
A.第二类永动机不可能制成的原因是违反了能量守恒定律
B.物体的温度越高,分子运动速率越大
C.熵是物体内分子运动无序程度的量度
D.晶体和非晶体在适当条件下是可以相互转化的
(2) (9分) 一气象探测气球,在充有压强为1.00atm(即76.0cmHg)、温度为27.0℃的氦气时,体积为3.50m3。在上升至海拔6.50km高空的过程中,气球内氦气逐渐减小到此高度上的大气压36.0cmHg,气球内部因启动一持续加热过程而维持其温度不变。此后停止加热,保持高度不变。已知在这一海拔高度气温为-48.0℃。求:
①氦气在停止加热前的体积;
②氦气在停止加热较长一段时间后的体积。
32、( 11 分)生长素的主要作用是促进细胞纵向伸长,其作用机理如图所示,请回答下列问题:
(1)
 生长素作用的第一步是与细胞膜上的受体结合,
生长素作用的第一步是与细胞膜上的受体结合,
形成“激素一受体复合物”,这一过程体现了细胞
膜的__ _功能。
(2) 被激活的“激素一受体复合物”能引起内质网
释放 Ca2 + , Ca2 +促使细胞内的 H十以______的方式
运往细胞外,增加了细胞壁的延展性,使细胞壁对
细胞的压力减小,导致细胞吸水、体积增大而发生
不可逆增长。细胞在生长过程中体积变化最大的细胞器是________。
(3)此外,Ca2 +还能激活细胞中的转录因子,它进入细胞核后,能引起________酶催化 mRNA 的合成。
(4)生长素促进根系生长的最适宜浓度要比茎低得多,稍高浓度的生长素能促进乙烯的生物合成,从而抑制了根的伸长,这说明生长素的作用具有__________
(5)科学家研究发现紫外光可以抑制植物生长,原因是紫外线增加了植物体内吲哚乙酸氧化酶的活性,从而促进了生长素氧化为 3 一亚甲基氧代吲哚,而后者没有促进细胞伸长的作用。现在提供生长状况相同的健康的小麦幼苗若干作为实验材料,请完成下列实验方案,以验证紫外线抑制植物生长与生长素的氧化有关。
步骤 1 :将小麦幼苗平均分为甲组和乙组。
步骤 2 :给予甲组________光照,给予乙组________光照。
步骤 3 :观察两组幼苗的__________,并测量_________的含量。
预测实验结果: ________
31、(12分) 鸭蛋蛋壳的颜色主要有青色和白色两种。金定鸭产青色蛋,康贝尔鸭产白色蛋。为研究蛋壳颜色的遗传规律,研究者利用这两个鸭群做了五组实验,结果如下表所示。
鸭蛋蛋壳的颜色主要有青色和白色两种。金定鸭产青色蛋,康贝尔鸭产白色蛋。为研究蛋壳颜色的遗传规律,研究者利用这两个鸭群做了五组实验,结果如下表所示。
|
杂交组合 |
第1组 |
第2组 |
第3组 |
第4组 |
第5组 |
|
|
康贝尔鸭♀ × 金定鸭♂ |
金定鸭♀ × 康贝尔鸭♂ |
第1组的F1自交 |
第2组的F1自交 |
第2组的F1♀ × 康贝尔鸭♂ |
||
|
后代所产蛋(颜色及数目) |
青色(枚) |
26178 |
7628 |
2940 |
2730 |
1754 |
|
白色(枚) |
109 |
58 |
1050 |
918 |
1648 |
请回答问题:
(1)根据第1、2、3、4组的实验结果可判断鸭蛋壳的 色是显性性状。
(2)第3、4组的后代均表现出 现象,比例都接近 。
(3)第5组实验结果显示后代产青色蛋的概率接近 ,该杂交称为 ,用于检验 。
(4)第1、2组的少数后代产白色蛋,说明双亲中 鸭群混有杂合子。
(5)运用 方法对上述遗传现象进行分析,可判断鸭蛋壳颜色的遗传符合孟德尔的 定律。
30、(6分)下图为处于不同分裂时期的某动物细胞中部分染色体示意图,图中均有性染色体X。请据图回答问题:

(1)细胞中具有同源染色体的是图________;等位基因的分离发生在图_______。
(2)该动物体内有可能同时出现这三种细胞的器官是______。图中含有X染色体数目最多的是_______。若配子中出现了两条X染色体,原因可能是减数第_______次分裂过程出现了异常。
(3)若用32P标记该生物一个体细胞中所有染色体的DNA分子,再将这些细胞转入不含32P的培养液中培养,则在第二次细胞分裂至甲图所处时期,一个细胞中被32P标记的染色体条数占染色体总条数的_________%。
29、
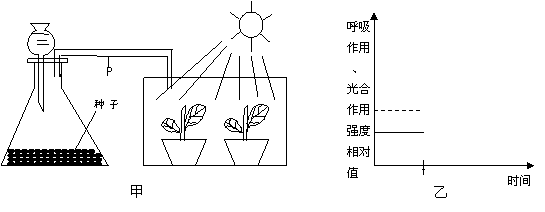 (10分)图甲装置为含水量较少的种子呼吸作用及幼苗光合作用实验图,图乙中的曲线表示种子呼吸作用(实线)和幼苗光合作用(虚线)的强度变化过程。请回答:
(10分)图甲装置为含水量较少的种子呼吸作用及幼苗光合作用实验图,图乙中的曲线表示种子呼吸作用(实线)和幼苗光合作用(虚线)的强度变化过程。请回答:
(1)在较强的光照条件下,水平玻璃管P处气体(CO2、O2)的流动方向是 ,气体的这种运动是通过 方式实现的。
(2)适当提高光照强度,此时叶肉细胞中C5含量将 。
(3)t时刻,向装有种子的瓶内加入适量的水后,呼吸作用及幼苗光合作用曲线将发生怎样的变化,请在图中绘出变化曲线,并说明理 。
28、(14分)现在普遍应用的工业合成氨的方法是哈伯于1905年发明的,但此法反应物的
转化率不高。
(1)已知:1 mol N2(g)与适量H2(g)完全反应,生成NH3(g),放出92.2 kJ热量,若该反应在298K、398K时的化学平衡常数分别为K1、K2,则K1 K2(填“>” “=” 或 “<” )。
(2)在一定温度下,向容积不变(始终为10L)的密闭容器中加入2 mol N2、8 mol H2 及固体催化剂。10分钟后反应达到平衡状态,容器内气体压强变为起始的80%,此时氨气的体积分数为 ,用氮气表示的反应速率为: 。若想提高氨气的产率,根据化学平衡移动原理,请提出合理的建议: (任意写一条)。
(3)在上述相同条件下,若起始时加入4 mol NH3、2 mol H2及固体催化剂,反应达到平衡时NH3的体积分数比(2)中 (填“大”、“小”或“相等”)。
(4)随着对合成氨研究的发展,2001年两位希腊化学家提出了电解合成氨的方法,即在常压下把氢气和用氦气稀释的氮气,分别通入一个加热到570℃的电解池中,采用高质子导电性的SCY陶瓷(能传递H+)为介质,用吸附在它内外表面上的金属钯多晶薄膜做电极,实现了常压、570℃条件下高转化率的电解法合成氨(装置如下图)。

请回答:在电解法合成氨的电解池中 (填“能”或“不能”) 用水作电解质溶液的溶剂,原因是 。钯电极A是电解池的 极(填“阳”或“阴”),该极上的电极反应式是 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com