
10、1mol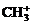 比1mol
比1mol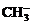 少
少 个电子。(×)
个电子。(×)
当题目针对的微粒不同时,答案不一样。微料可以是分子、原子、离子、中子、电子、××原子、最外层电子、价电子,判断时一定要注意。如将上述2中“分子数”改为“原子数”、“氧原子数”后,情况就有变化。
另外,涉及核外电子数时要注意“根”、“基”、“离子”的变换,如:
9、8g 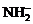 离子含有的电子数为5
离子含有的电子数为5 。(√)
。(√)
8、标准状况下,3.36L 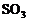 含有的分子数为1.5
含有的分子数为1.5 。(×)
。(×)
其中7是1996年的高考20题的(B)选项,当时许多考生一看见“标准状况”,便断定1L辛烷(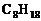 )为1/22.4mol,从而推出其完全燃烧生成8/22.4mol气体(
)为1/22.4mol,从而推出其完全燃烧生成8/22.4mol气体( ),即8/22.4
),即8/22.4 个气体分子。殊不知,在标准状况下,辛烷为液体,此时的1L辛烷远不止1/22.4mol。8也是类似情况,标准状况下
个气体分子。殊不知,在标准状况下,辛烷为液体,此时的1L辛烷远不止1/22.4mol。8也是类似情况,标准状况下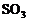 也不是气态。
也不是气态。
设陷方式主要有:如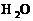 、
、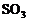 及C原子数多于4的烷烃等在标准状况下不是气体物质。
及C原子数多于4的烷烃等在标准状况下不是气体物质。
看两个例子:
7、标准状况下,1L辛烷完全燃烧后,所生成气体产物的分子数为8/22.4 个。(×)
个。(×)
6、25℃,1atm下, 个
个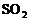 分子的体积大于22.4L。(√)
分子的体积大于22.4L。(√)
上述4、5并不涉及体积,而直接给出质量或物质的量,这时与物质是否处于标准状况无关。而6则巧妙地改常用的“等于”为“大于”,稍不注意,就会出错。
5、常温常压下,0.5mol 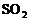 气体含有0.5
气体含有0.5 个分子。(√)
个分子。(√)
4、常温常压下,32g 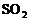 气体含有0.5
气体含有0.5 个分子。(√)
个分子。(√)
3、标准状况下,3.36L CO与 的混合气体含有的碳原子数为0.15
的混合气体含有的碳原子数为0.15 。(√)
。(√)
分析:在1中,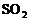 所处状况是常温常压而非标准状况,
所处状况是常温常压而非标准状况, 个
个 分子的物质的量为1mol,但体积并非22.4L。2则恰为标准状况,11.2L
分子的物质的量为1mol,但体积并非22.4L。2则恰为标准状况,11.2L  气体的物质的量为11.2L÷22.4mol/L=0.5mol,则含有的分子数为0.5
气体的物质的量为11.2L÷22.4mol/L=0.5mol,则含有的分子数为0.5 ,该说法正确。类似地分析3,该说法是正确的。
,该说法正确。类似地分析3,该说法是正确的。
值得指出的是,有些同学由于受“题海”影响,一看到“常温常压”或非标准状况就认为该说法错误,如:
2、1atm273K时,11.2L  气体含有的分子数为0.5
气体含有的分子数为0.5 (√)
(√)
只有当气体处于标准状况时,才可将气体体积除以“22.4L/mol”而转化为物质的量,进而由 计算微粒数。例如:
计算微粒数。例如:
1、常温常压下, 个
个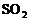 分子的体积为22.4L。(×)
分子的体积为22.4L。(×)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com