
7. --- John and I will celebrate our fortieth wedding anniversary next month.
--- Oh, _______!
A. cheer up B. well done C. go ahead D. congratulations
6. Hearing the dog barking fiercely, away __________.
A. fleeing the thief B. was fleeing the thief
C. the thief was fleeing D. fled the thief
5. Mary went to the box office at lunch time, but all the tickets _______ out.
A. have sold B. would sell C. was selling D. had sold
4. It ______ Tom that parked the car here, as he is the only one with a car.
A. may be B. can be C. must have been D. should have been
3. The ship went down with all its crew ______.
A. aboarding B. on board C. abroad D. being boarded
2. The naughty boy ____ to his mother that the duck that ____ under the tree had ____ two eggs.
A. laid; lied; lain B. laid; lay; lain C. lied; laid; lain D. lied; lay; laid
第一节 单项填空(共20小题;每题1分,共20分)
从每题所给的A,B,C,D四个选项中,选出可以填入空白处的最佳选项,并在答题卡上将该项涂黑。
1. Quite a few problems _______ after the new examination system was introduced, and the number of students in this school _____ by 5% last year.
A. arose; raised B. arose; rose C. rose; raised D raised; rose
[例题讲解] [例1] 下列有关胶体和溶液的比较中正确的是 ( ) A.溶液呈电中性,胶体带有电荷 B.溶液中溶质粒子运动有规律,胶体粒子运动无规律 C.溶液中通过光束没有特殊现象,胶体中通过光束有丁达尔现象 D.通电后,溶液中溶质粒子分别向两极移动,而胶体中分散质粒子向某一极移动 解析: A.胶体的分散质粒子带有电荷,但整个胶体不带电; B.溶液中的溶质粒子和胶体粒子的运动均无规律,但胶体粒子比溶质粒子大,其无规则的运动现象可用电子显微镜观察得到; C. 溶质粒子太小,无丁达尔效应,而胶体有丁达尔效应; D.如果溶质粒子是某种分子,则在通电时不会向两校移动。所以,上述比较中,只有C项正确。 答案:C [例2] 将不溶性物质与KCl固体混合后放入一定量的水中,充分搅拌后,有以下实验数据:
|
温度(℃) |
20 |
40 |
60 |
|
剩余固体物质(g) |
38 |
20 |
10 |
已知KCl的溶解度(g)
|
20℃ |
30℃ |
40℃ |
50℃ |
60℃ |
70℃ |
|
34.0 |
37.0 |
40.0 |
42.6 |
45.5 |
48.6 |
求:
(1)所加入水的质量是多少?
(2)该固体混合物中KCl的含量是多少g?
(3)使60℃时所得的溶液成为饱和溶液,应加入多少g KCl?
解析:
从剩余的固体物质可知20℃、40℃时都是饱和溶液,而60℃时虽然剩余l0g,但不一定是饱和溶液,原因是10 g可能全部是杂质,没有比60℃更高的实验数据,因此无法判断60℃时是否为饱和溶液。
(1)
设加入水的质量为xg
(40-34)∶100=(38-20)∶x x=300g
温度由40℃升到60℃应溶解的KCl为: ×300g=16.5g
而实际只溶解了(20-10)g=10g,所以60℃时为KCl的不饱和溶液。
(2)
该固体混合物中KCl 的含量是:
×300g=16.5g
而实际只溶解了(20-10)g=10g,所以60℃时为KCl的不饱和溶液。
(2)
该固体混合物中KCl 的含量是:
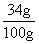 ×300g+(38-10)g=130g
或
×300g+(38-10)g=130g
或 ×300g+(20-10)g=130
(3)
应加入的KCl质量为
×300g+(20-10)g=130
(3)
应加入的KCl质量为  ×300g-130g=6.5g
[例3] 某温度下,在100 g水中加入mg CuSO4或加入ng CuSO4·5H2O,均可使溶液恰好达到饱和,则m与n的关系符合 ( )
A.m=
×300g-130g=6.5g
[例3] 某温度下,在100 g水中加入mg CuSO4或加入ng CuSO4·5H2O,均可使溶液恰好达到饱和,则m与n的关系符合 ( )
A.m= B.m=
B.m= C.m=
C.m= D.m=
D.m= 解析:
根据溶解度定义求解:
解析:
根据溶解度定义求解:
 答案:B
[例4] A、B两种化合物的溶解度曲线如图所示,现要用结晶法从A、B混合物中提取A(不考虑A、B共存时对各自溶解度的影响)。
答案:B
[例4] A、B两种化合物的溶解度曲线如图所示,现要用结晶法从A、B混合物中提取A(不考虑A、B共存时对各自溶解度的影响)。

(1)取50g混合物,溶于100g热水,然后冷却至20℃。若要使A析出而B不析出。 则混合物中B的质量分数(B%)最高不能超过多少?(写出推理及计算过程) (2)取Wg混合物。溶于100 g的热水,然后冷却至10℃若仍要使A析出而B不析出。请写出下列两种情况下,混合物中A的质量分数(A%)应满足什么关系式。(以W、a、b表示) 当W<a+b时,A%_____________ 当W>a+b时, A%______________ 解析: (1)在20℃时,若要B不析出,该溶液中B的质量不能超过20 g,由于A、B质量共50g,所以这时A的质量超过30 g,大于它的溶解度,A析出。符合题意。即50 g×B%≤20 g,B%≤40%。 (2)根据题意应满足下列关系式
 解得:
解得:  显然,答案应取(1)(2)两解之较大者。
根据差值比较法有:
当W<a+b时, 因为
显然,答案应取(1)(2)两解之较大者。
根据差值比较法有:
当W<a+b时, 因为 所以
所以 (1)式A%>
(1)式A%>  为解
当W>a+b时,因为
为解
当W>a+b时,因为  所以
所以 (2)式A%≥
(2)式A%≥  为解
答案:
(1)B%≤40%; (2)>
为解
答案:
(1)B%≤40%; (2)> ;≥
;≥


(上面饱和溶液、不饱和溶液、晶体间的关系是一般转化关系,有例外情况)
溶质:被溶解的物质(即分散质)
溶剂:能溶解其他物质的物质(即分散剂)
说明:
(1)溶液是分散系中的一种,其分散质通常是分子或离子,大小为10-9m以下。
(2)溶液的特点是:均一、稳定、多为透明。
2、常用的溶剂
无机溶剂:H2O,NH3(液),HF(液)等。
有机溶剂:C2H5OH,O(C2H5)2,丙酮,苯,CCl4,氯仿(CHCl3),CS2,汽油等。
3、溶液的分类:
①按状态分成
固体“溶液”:例如合金
液体“溶液”:例如水溶液
气体“溶液”:例如空气
②按饱和程度分类
饱和溶液:一定温度下一定体积的溶液不能再溶解某溶质时叫做这种溶质的饱和溶液。
不饱和溶液:一定温度下一定体积的溶液还能继续溶解某溶质时叫做这种溶质的不饱和溶液。
4、关于溶解度计算的方法
(1)温度不变时,饱和溶液蒸发溶剂或向饱和溶液中加入溶剂时,析出或溶解溶质(达到饱和)的质量x:
 (2)若溶剂不变,改变温度,求析出或溶解溶质达到饱和的质量x:
(2)若溶剂不变,改变温度,求析出或溶解溶质达到饱和的质量x:
 (3)溶剂和温度改变时,求析出或溶解溶质达到饱和的质量x:
其方法是:先求原饱和溶液中溶质和溶剂的质量,再求形成的新饱和溶液中的溶剂、溶质的质量,并列相应比例关系计算。
(4)加入或析出的溶质带有结晶水;
既要考虑溶质质量的变化,又要考虑溶剂质量的变化,一般情况下,先求原饱和溶液的溶质与溶剂,再求新饱和溶液中所含溶质与溶剂。
5.溶液的浓度
(1)溶质的质量分数(ω):用溶质质量占全部溶液质量的百分比来表示的溶液的浓度。
(2)物质的量浓度(c):以1L溶液中含有多少摩尔溶质表示的溶液浓度。
溶质的质量分数与物质的量浓度之间的换算关系(必须知道溶液的密度):c=1000ρω/摩尔质量(溶质的)
注意:
既然溶解度是指“溶解的最多克数”,那么得到的必定是饱和溶液。但饱和溶液不一定是浓溶液,因为它指的是溶质不能再溶解了,并不是说溶质溶解了很多,如CaCO3饱和溶液中溶质 浓度很小。同样,不饱和溶液也不一定是稀溶液,浓溶液不一定是饱和溶液。
二.胶体
1、定义:分散质的大小介于10-7-10-9m之间的分散系叫做胶体。
2、胶体的分类
按分散质的组成分为:
粒子胶体:如Fe(OH)3胶体,Al(OH)3胶体
分子胶体:如蛋白质溶于水所得分散系,淀粉溶于水所得分散系
按分散剂的状态分成:
液溶胶:如Na2SiO3溶于水所得分散系,肥皂水
固溶胶:有色玻璃
气溶胶:烟、云、雾
3、胶体的性质、提纯、凝聚方法
(3)溶剂和温度改变时,求析出或溶解溶质达到饱和的质量x:
其方法是:先求原饱和溶液中溶质和溶剂的质量,再求形成的新饱和溶液中的溶剂、溶质的质量,并列相应比例关系计算。
(4)加入或析出的溶质带有结晶水;
既要考虑溶质质量的变化,又要考虑溶剂质量的变化,一般情况下,先求原饱和溶液的溶质与溶剂,再求新饱和溶液中所含溶质与溶剂。
5.溶液的浓度
(1)溶质的质量分数(ω):用溶质质量占全部溶液质量的百分比来表示的溶液的浓度。
(2)物质的量浓度(c):以1L溶液中含有多少摩尔溶质表示的溶液浓度。
溶质的质量分数与物质的量浓度之间的换算关系(必须知道溶液的密度):c=1000ρω/摩尔质量(溶质的)
注意:
既然溶解度是指“溶解的最多克数”,那么得到的必定是饱和溶液。但饱和溶液不一定是浓溶液,因为它指的是溶质不能再溶解了,并不是说溶质溶解了很多,如CaCO3饱和溶液中溶质 浓度很小。同样,不饱和溶液也不一定是稀溶液,浓溶液不一定是饱和溶液。
二.胶体
1、定义:分散质的大小介于10-7-10-9m之间的分散系叫做胶体。
2、胶体的分类
按分散质的组成分为:
粒子胶体:如Fe(OH)3胶体,Al(OH)3胶体
分子胶体:如蛋白质溶于水所得分散系,淀粉溶于水所得分散系
按分散剂的状态分成:
液溶胶:如Na2SiO3溶于水所得分散系,肥皂水
固溶胶:有色玻璃
气溶胶:烟、云、雾
3、胶体的性质、提纯、凝聚方法
胶体的性质及意义
|
胶体的性质 |
原 因 |
意 义 |
|
丁达尔现象(光学性质) |
胶粒对光的散射 |
区别胶体与溶液的方法 |
|
布朗运动(动力学性质) |
胶粒与水分子撞击产生的不规则运动 |
证明分子是运动的 |
|
胶体的聚沉 |
胶体粒子结合成大颗粒而沉降 |
破坏胶体,如做豆腐 |
|
电泳现象(电学性质) |
胶粒带电荷 |
静电除尘 |
|
粘性 |
总表面积大,吸附性强 |
胶水 |
|
渗析 |
胶粒直径大于小分子、离子直径而不能透过半透膜 |
净化胶体 |
4、胶体的制备
(1)物理法:
如研磨(制豆浆、研墨),直接分散(制蛋白胶体)
(2)水解法:
[Fe(OH)3胶体]向20mL沸蒸馏水中滴加1mL-2mLFeCl3饱和溶液,继续煮沸一会儿,得红褐色的Fe(OH)3胶体。离子方程式为
 (3)复分解法:
(AgI胶体)向盛10mL 0.01mol·L-1 KI的试管中,滴加8-10滴0.01mol·L-1 AgNO3,边滴边振荡,得浅黄色AgI胶体。
(硅酸胶体)在一大试管里装入5mL-10mL1mol·L-1HCl,加入1mL水玻璃,然后用力振荡即得。
离子方程式分别为:
Ag++I-=AgI(胶体)
SiO32-+2H++2H2O=H4SiO4(胶体)
复分解法配制胶体时溶液的浓度不宜过大,以免生成沉淀。
5、常见的胶体分散系
①FeCl3溶液,AlCl3溶液或明矾溶液,水玻璃,肥皂水等。形成胶体的原因是盐水解生成不溶物所致。
FeCl3溶液:Fe3++3H2O=Fe(OH)3(胶体)+3H+
明矾溶液:Al3++3H2O=Al(OH)3(胶体)+3H+
水玻璃:SiO32-+3H2O=H4SiO4(胶体)+2OH-
肥皂水:C17H35COO-+H2O=C17H35COOH(胶体)+OH-
②Ag++X-=AgX(胶体)
③土壤胶体。
④豆奶、牛奶、蛋清的水溶液。
⑤有色玻璃,如蓝色钴玻璃(分散质为钴的蓝色氧化物,分散剂为玻璃)。
⑥烟、云、雾。
(3)复分解法:
(AgI胶体)向盛10mL 0.01mol·L-1 KI的试管中,滴加8-10滴0.01mol·L-1 AgNO3,边滴边振荡,得浅黄色AgI胶体。
(硅酸胶体)在一大试管里装入5mL-10mL1mol·L-1HCl,加入1mL水玻璃,然后用力振荡即得。
离子方程式分别为:
Ag++I-=AgI(胶体)
SiO32-+2H++2H2O=H4SiO4(胶体)
复分解法配制胶体时溶液的浓度不宜过大,以免生成沉淀。
5、常见的胶体分散系
①FeCl3溶液,AlCl3溶液或明矾溶液,水玻璃,肥皂水等。形成胶体的原因是盐水解生成不溶物所致。
FeCl3溶液:Fe3++3H2O=Fe(OH)3(胶体)+3H+
明矾溶液:Al3++3H2O=Al(OH)3(胶体)+3H+
水玻璃:SiO32-+3H2O=H4SiO4(胶体)+2OH-
肥皂水:C17H35COO-+H2O=C17H35COOH(胶体)+OH-
②Ag++X-=AgX(胶体)
③土壤胶体。
④豆奶、牛奶、蛋清的水溶液。
⑤有色玻璃,如蓝色钴玻璃(分散质为钴的蓝色氧化物,分散剂为玻璃)。
⑥烟、云、雾。
三种分散系比较
|
分散系 |
溶液 |
胶体 |
浊液 |
|
分散质微粒直径 |
<10-9m |
10-9m-10-7m |
>10-7m |
|
外观 |
均一、透明、稳定 |
多数均一、透明、稳定 |
不均一、不透明、不稳定 |
|
分散质微粒组成 |
单个分子或离子 |
分子集合体或有机高分子 |
许多分子集合体 |
|
能否透过滤纸 |
能 |
能 |
不能 |
|
能否透过半透膜 |
能 |
不能 |
不能 |
|
实例 |
食盐水、碘酒 |
肥皂水、淀粉溶液 |
泥水 |
20.(8分)加热500g含(NH4)2SO413.2%的硫酸铵和碱石灰组成的混合物,并把生成的氨气氧化成NO,再继续氧化成NO2,最后全部转化成HNO3(反应过程中无损耗),求:
(1)反应共需标准状况下的氧气多少升?
(2)可制得多少克硝酸?
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com