
8. X、Y、Z、W、R是5种短周期元素,其原子序数依次增大。X是周期表中原子半径最小的元素,Y原子最外层电子数是次外层电子数的3倍,Z、W、R处于同一周期,R与Y处于同一族,Z、W原子的核外电子数之和与Y、R原子的质子数之和相等。下列说法正确的是
A.元素Y、Z具有相同电子层结构的离子,其离子半径大小为Y < Z

B.元素X不能与元素Y形成化合物X2Y2
C.元素Y、R分别与元素X形成的化合物的热稳定性:XmY
> XmR
D.元素W、R的最高价氧化物的水化物都是强酸

7.下列实验设计和结论相符的是
A.将碘水倒入分液漏斗,加适量乙醇,振荡后静置,可将碘萃取到乙醇中
B.某气体能使湿润的红色石蕊试纸变蓝,该气体水溶液一定显碱性
C.某无色溶液中加Ba(NO3)2溶液,再加入稀盐酸,沉淀不溶解,则原溶液中一定有SO42-
D.在含FeCl2杂质的FeCl3溶液中通足量Cl2后,充分加热,除去过量的Cl2,即可得到较纯净的FeCl3溶液
6.25 ℃时,浓度均为0.2 mol·L-1的NaHCO3和Na2CO3溶液中,下列判断不正确的是
A.均存在电离平衡和水解平衡 
B.存在的粒子种类相同
C.c(OH-)前者大于后者 
D.分别加入NaOH固体,恢复到原温度,c(CO32-)均增大
5.下列叙述中正确的是
( )
A.物质的溶解过程,实质上就是其电离过程
B.二氧化硫的水溶液能导电,所以二氧化硫是电解质
C.1 L 0.1 mol·L-1的H2SO4溶液中含有0.2 mol的H+
D.1 L 0.2 mol·L-1的H2SO3溶液中含有0.2 mol的H+
4. 下列叙述正确的是(用NA代表阿伏加德罗常数的值)
A.2.4g金属镁变为镁离子时失去的电子数为0.1NA
B.1molHCl气体中的粒子数与0.5 mo1/L盐酸中溶质粒子数相等
C.在标准状况下,22.4LCH4与18gH2O所含有的电子数均为10 NA
D.CO和N2的质子数相等,22.4L的CO气体与lmol N2所含的电子数也相等
3.能实现下列物质间直接转化的元素是
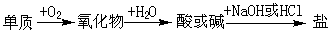

A. 硅
B. 硫
C. 铜
D. 铁
2.化学与生活密切相关,下列有关说法正确的是
A.维生素C具有还原性,在人体内起抗氧化作用 
B.糖类、蛋白质、油脂属于天然高分子化合物
C.煤经气化和液化两个物理变化过程,可变为清洁能源
D.明矾水解形成的Al(OH)3胶体能吸附水中悬浮物,可用于水的消毒净化
1. 铋(Bi)被称为“绿色”金属,在医药方面有重要应用。下列关于20983Bi和21083Bi的说法正确的是
A.20983Bi和21083Bi是同一种核素
B.20983Bi和21083Bi都含有83个中子
C.20983Bi和21083Bi的核外电子数相同,中子数不同
D.20983Bi和21083Bi分别含有126和127个质子
28.(8分)C1化学是指从一个碳原子的化合物(如CH4,CO,CO2 CH3OH,HCHO等)出发合成各种化学品的技术。从煤、天然气制合成气再进一步制备各种化工产品和洁净燃料,已成为当今化学工业发展的必然趋势。其中甲醇是C1化学的基础。
①CO与H2按一定比例可生成乙二醇,则n(CO)/n(H2)= 。(填数字)
②若汽油平均组成用CmHn表示,则合成汽油应控制n(CO)/n(H2)= 。(用m 、 n表示),
③甲醇在一定条件下与CO、H2作用生成有机物A,A发生加聚可生成高分子

27.(12分)对乙酰氨基酚,俗称扑热息痛(Paracetamol),具有很强的解热镇痛作用,工业上通过下列方法合成(B1和B2、C1和C2分别互为同分异构体,无机产物略去):
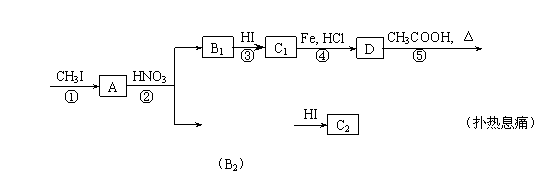
请按要求填空:
⑴上述①-⑤的反应中,属于取代反应的有_____________(填数字序号)。
⑵C2分子内通过氢键又形成了一个六元环,用“ ”表示硝基、用“…”表示氢键,画出C2分子的结构______________________。C1只能通过分子间氢键缔合,工业上用水蒸气蒸馏法将C1和C2分离,则首先被蒸出的成分是_________(填“C1”或“C2”)。
”表示硝基、用“…”表示氢键,画出C2分子的结构______________________。C1只能通过分子间氢键缔合,工业上用水蒸气蒸馏法将C1和C2分离,则首先被蒸出的成分是_________(填“C1”或“C2”)。
⑶工业上设计反应①、②、③,而不是只通过反应②得到C1、C2,其目的是
____________________________________________。
⑷扑热息痛有很多同分异构体,符合下列要求的同分异构体有5种:(Ⅰ)是对位二取代苯;(Ⅱ)苯环上两个取代基一个含氮不含碳、另一个含碳不含氮;(Ⅲ)两个氧原子与同一原子相连。其中2种的结构简式是 和
和 ,写出另3种同分异构体的结构简式_______________________________________________。
,写出另3种同分异构体的结构简式_______________________________________________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com