
6.下列说法正确的是
①世博会中国馆--“东方之冠”使用的钢筋混凝土属于高分子化合物;②CH3COONa、BaSO4都是强电解质;③明矾和氯气可用于饮用水的净化和杀菌消毒,且两者的作用原理不同;④ 0.1 mol/L NaOH溶液与0.1 mol/L Ba(OH)2 溶液的pH相同;⑤一定温度下,适量CO2 分别通入饱和碳酸钠溶液和澄清石灰水中,都会出现浑浊。
A.①③④ B.①②④ C.②③⑤ D.③④⑤
28.(J4分)
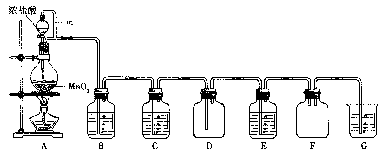 二氧化锰(MnO2)与浓盐酸混合加热可得到氯气、氯化锰等,下图是制取并探究Cl2化学性质的装置图。
二氧化锰(MnO2)与浓盐酸混合加热可得到氯气、氯化锰等,下图是制取并探究Cl2化学性质的装置图。
(1)已知锰元素的常见化合价为+7、+6、+4、+2,写出圆底烧瓶中反应的化学方程式
。
(2)A中m管的作用是 ,装置F的作用是 。
(3)若要得到干燥纯净的气体,则B中应盛放的试剂是 。
(4)E中若装有FeCl2溶液,反应的离子方程式为 ;E中若装有淀粉碘化钾溶液,能观察到的实验现象是 。
(5)实验中发现:浓盐酸与Mn0:混合加热生成氯气,稀盐酸与Mn0:混合加热不生成氯气。针对上述现象,化学小组对“影响氯气生成的原因”进行了讨论,并设计了以下实验方案:
a.稀盐酸滴入MnO2中,然后通人HCl气体,加热
b.稀盐酸滴人MnO2中,然后加入NaCl固体,加热
c.稀盐酸滴入MnO2中,然后加入浓硫酸,加热
d.Mn02与NaCl的浓溶液混合,加热
e.浓硫酸与NaCl固体、MnO2固体共热
①实验b的目的是 ;实验c的目的是 。
②实验现象:a、c、e有黄绿色气体生成,b、d没有黄绿色气体生成。由此得出影响氯气生成的原因是 。
27.(12分)
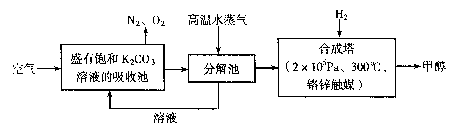 为减小和消除CO2对环境的影响,有科学家提出“绿色自由”构想。即先把空气吹人碳酸钾溶液,然后再把CO2从溶液中提取出来,并使之变为可再生燃料甲醇。“绿色自由”构想技术流程如下:
为减小和消除CO2对环境的影响,有科学家提出“绿色自由”构想。即先把空气吹人碳酸钾溶液,然后再把CO2从溶液中提取出来,并使之变为可再生燃料甲醇。“绿色自由”构想技术流程如下:
(1)写出分解池中反应的化学方程式 。
(2)在合成塔中,当有4.4kg CO2与足量H2完全反应,可放出热量4947 kJ,写出合成塔中反应的热化学方程式 。
(3)写出以氢氧化钾为电解质的甲醇燃料电池的负极反应式 。
当电子转移为 mol时,参加反应的氧气的体积是6.72L(标准状况下)。
(4)在体积为l L的密闭容器中,充人1mol CO2和3molH2在500°C下发生反应。有关物质的浓度随时问变化如下图所示。

①从反应开始到平衡,H2的平均反应速率v(H2)= 。
②若其他条件不变,只将温度提高到800°C,再次达平衡时,n(CH3OH)/n(CO2)比值 (填“增大”、“减小”或“不变”)。
26.(16分)
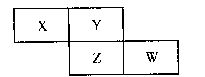 X、Y、Z、W四种短周期元素在周期表中的位置关系如图:
X、Y、Z、W四种短周期元素在周期表中的位置关系如图:
I.若Z元素原子的最外层电子数是电子层数的2倍
(1)W在周期表中的位置为 。
(2)Y和Z可组成的化合物的化学式为 。
(3)写出铜和X的最高价氧化物水化物稀溶液反应的离子方程式 。
(4)W最高价氧化物水化物的浓溶液不稳定,受热可分解,产物之一是黄绿色气体,且当有28mol电子转移时,共产生9mol气体,写出该反应的化学方程式 。
II.若Y和z的核外电子数之和为22
(1)Y的气态氢化物电子式为 ,工业合成该物质的化学方程式为 。
(2)将X的最高价氧化物通人到苯酚钠溶液中,实验现象是 。
(3)X单质与W的最高价氧化物水化物的浓溶液反应,当电:子转移0.4mol时,产生气体的体积(标准状况下)是 。
25.(16分)
以A和乙醇为有机基础原料,合成香料甲的流程图如下:
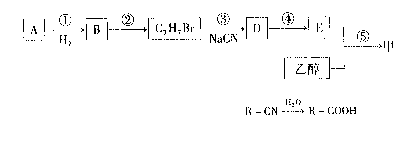
已知:R-Br+NaCN→R→CN+NaBr;
杏仁中含有A,A能发生银镜反应。质谱测定,A的相对分子质量为106。5.3g A完全
燃烧时,生成15.4g CO:和2.7g HO。
(1)A的分子式为 ,A发生银镜反应的化学方程式为 。
(2)写出反应②的化学方程式 。
(3)上述反应中属于取代反应的是: 。
(4)符合下列条件的E的同分异构体有 种;
a.能发生银镜反应 b.不含Cu c.不能水解
写出其中2种结构简式
(5)写出反应⑤的化学方程式 。
10. 在恒温容器中,可逆反应C(s)+H2O(g) CO(g)+H2(g)一定达平衡状态的是 ( )
在恒温容器中,可逆反应C(s)+H2O(g) CO(g)+H2(g)一定达平衡状态的是 ( )
A.气体的压强不变
B.气体的体积不变
C.混合气的密度不变
D.有n个H-O键断裂的同时有n个H-H键断裂
 11.关于下列装置用途的判断正确的是 ( )
11.关于下列装置用途的判断正确的是 ( )
①装置甲可防止铁钉生锈 ②装置乙可除去乙烯中混有的SO2
③装置丙可检验NH3在水中的溶解性 ④装置丁可用于实验室制取乙酸乙酯
⑤装置戊可用于收集H2、CO2、Cl2、CHl、NO2等气体
A.只有③④ B.只有③⑤ C.只有①③⑤ D.只有①②④
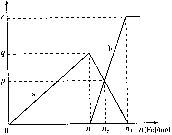 12.含有1mol HNO3的稀硝酸分别与不同质量的铁粉反应,
12.含有1mol HNO3的稀硝酸分别与不同质量的铁粉反应,
所得氧化产物a、b与铁粉物质的量关系如图所示。下
列有关判断正确的是 ( )
A.a是Fe(NO3)2
B.n1=0.375
C.P=0.125
D.n2=0.30
第Ⅱ卷(非选择题共180分)
7.下列说法正确的是 ( )
A.含10.6 g Na2CO3的溶液中,所含阴离子总数等于6.02×1022
B.28 g由乙烯和氮气组成的混合气体中,含有6.02×1023个原子
C.电解法精炼铜,当阴极质量增加32 g时,有6.02×1023个电子转移
D.含0.2 mol H2SO4的浓硫酸与足量铜反应,生成SO2的分子数为6.02×1022
 8.向25.00mL 0.10mo/L NaOH溶液中逐滴加入0.10mol/L CO3COOHH溶液,溶液pH变化曲线如图所示,下列有关判断错误的是 ( )
8.向25.00mL 0.10mo/L NaOH溶液中逐滴加入0.10mol/L CO3COOHH溶液,溶液pH变化曲线如图所示,下列有关判断错误的是 ( )
A.在A点,溶液的pH=13
B.在B点,c(Na+)=c(CH3COO一)>c(OH一)=c(H+)
C.在C点,c(Na+)>c(CH3COO-)>c(H+)>c(OH一)
D.在D点,c(CH3COO-)+c(CH3COOH)=2c(Na+)
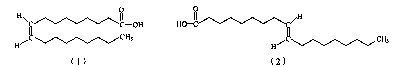 9.某脂肪酸的两种异构体结构简式如图所示
9.某脂肪酸的两种异构体结构简式如图所示
下列叙述错误的是 ( )
A.该脂肪酸含有羧基和碳碳双键两种官能团
B.(1)式为顺式结构,(2)式为反式结构
C.该脂肪酸最简单的同系物是CH2=CH-COOH
D.(1)和(2)分别与氢气加成,所得产物不同
6.下列说法正确的是 ( )
A.味觉上有酸味的食物即酸性食物
B.生石灰可防止食物受潮,铁粉可防止食物氧化变质
C.油脂、淀粉、蛋白质和维生素等均为高分子化合物
D.食品添加剂苯甲酸钠是苯的一种同系物所对应的钠盐
2010.5
本试卷分第1卷(选择题)和第Ⅱ卷(非选择题)两部分,共300分。考试时间150分钟。考生务必将答案答在答题卡上,在试卷上作答无效。
以下数据可供解题时参考:
可能用到的相对原子质量:H 1 C 12 N 14 0 16 Na 23 S32 Cu 64
第Ⅰ卷(选择题共120分)
28.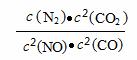 (10分)(1)
(2分)
(10分)(1)
(2分)
(2)-746 (2分) (3)③④(全对得2分,漏选得1分,有错选得0分)
(4)②③(全对得2分,漏选得1分,有错选得0分)
(5)0.05 (2分)




湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com