
5.下列说法中正确的是_
A.X射线是处于激发态的原子核辐射出的
B.放射性元素发生一次β衰变,原子序数增加1
C.原子核的半衰期不仅与核内部自身因素无关,还与原子所处的化学状态无关
D.光电效应揭示了光具有粒子性,康普顿效应揭示了光具有波动性
4.图中气缸内盛有定量的理想气体,气缸壁是导热的,缸外环境保持恒温,活塞与气缸壁
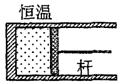 的接触是光滑的,但不漏气,现将活塞杆与外界连接并使之缓慢地向右移动,这样气体将等
的接触是光滑的,但不漏气,现将活塞杆与外界连接并使之缓慢地向右移动,这样气体将等
温膨胀并通过杆对外做功.若已知理想气体的内能只与温度有关,则下列说法正确的是
A.气体是从单一热源吸热,全用来对外做功,因此此过程违反热力学第二定律
B.气体是从单一热源吸热,但并未全用来对外做功,所以此过程不违反热力学第二
定律
C.气体是从单一热源吸热,全用来对外做功,但此过程不违反热力学第二定律
D.A、B、C三种说法都不对
3.据报道在2004年底印度洋发生地震形成海啸之前,我国的“风云二号”气象卫星在2004年12月20日拍摄的五张气象图上已经显示出地震发生的征兆.气象卫星是用来拍摄云层照片,观测气象资料和测量气象数据的.我国先后自行成功研制和发射了"风云一号"和"风云二号"两颗气象卫星,"风云一号"卫星轨道与赤道平面垂直,通过两极,每12小时巡视一周,称为"极地圆轨道","风云二号"气象卫星轨道平面在赤道平面内,称为"地球同步轨道",则( )
A.“风云一号”比"风云二号"的发射速度大
B.“风云一号”比"风云二号"的线速度小
C.“风云一号”比"风云二号" 的向心加速度小
D.“风云一号”比"风云二号"的运动周期小
2.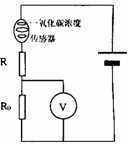 氧化锡传感器主要用于汽车尾气中一氧化碳浓度的检测。它的电阻随一氧化碳浓度的变化而变化,在如图
所示的电路中,不同的一氧化碳浓度对应着传感器的不同电阻,这样,显示仪表的指针就与一氧化碳浓度有了对应关系,观察仪表指针就能判断一氧化碳是否超标。有一种氧化锡传感器,其电阻的倒数与一氧化碳的浓度成正比,那么,电压表示数U与一氧化碳浓度C之间的对应关系正确的是 ( )
氧化锡传感器主要用于汽车尾气中一氧化碳浓度的检测。它的电阻随一氧化碳浓度的变化而变化,在如图
所示的电路中,不同的一氧化碳浓度对应着传感器的不同电阻,这样,显示仪表的指针就与一氧化碳浓度有了对应关系,观察仪表指针就能判断一氧化碳是否超标。有一种氧化锡传感器,其电阻的倒数与一氧化碳的浓度成正比,那么,电压表示数U与一氧化碳浓度C之间的对应关系正确的是 ( )
A.U越大,表示C越大,C与U成正比
B.U越大,表示C越小,C与U成反比
C.U越大,表示C越大,但是C与U不成正比
D.U越大,表示C越小,但是C与U不成反比
1.在显像管的电子枪中,从炽热的金属丝不断放出的电子进入电压为 U的加速电场,设其初速度为零,经加速后形成横截面积为 S、电流为 I的电子束。已知电子的电量为e、质量为 m,则在刚射出加速电场时,一小段长为△L的电子束内电子个数是
A. B.
B.
C. D.
D.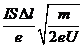
30.(17分)在某种植物的根茎叶中含有的有机物M的分子式为C16H19O5Br,可用于制取苹果酸等,M的部分结构如下:

经测定■结构中含有Br,●结构中含有苯环,有关
 有机物转化关系如下图
有机物转化关系如下图
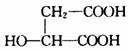
已知:①A为苹果酸,其结构简式为 。G1与G2互为同分异构
体,且所含官能团相同。
 ②C分子只含C、H、O三种元素,其分子结构模型如图所示(图中球与球之间连线代
②C分子只含C、H、O三种元素,其分子结构模型如图所示(图中球与球之间连线代
表单键或双键。)
回答下列问题:
(1)苹果酸A中所含官能团的名称是 。
(2)①的反应类型是 ,③的反应类型是 。
(3)C的结构简式为 ,■部分的结构简式为 ;写出B→E反应的化学方程式: 。1molM与足量NaOH反应消耗NaOH的物质的量为 mol。
(4)写出满足下列条件的C的同分异构体的结构简式: 。
a.能发生银镜反应 b.苯环上的一溴代物有2种
29.(16分)下图为实验室制取气体的常用装置。
可提供的药品有:大理石、浓盐酸、浓硝酸、浓硫酸、浓氨水、锌粒、铜片、H2O2、Na2O2、乙醇、MnO2、生石灰。试回答下列问题:
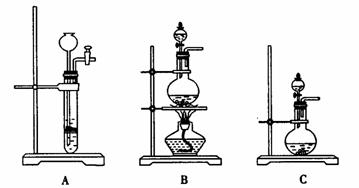
(1)上图三个制取气体的装置中,其中 (填编号)装置检验气密性的方法与另外两个不同。
(2)若要用A、B、C中某一装置来制取C2H4,应选用 装置,且必须将该装置中的分液漏斗换成 并插入液面下。
(3)编号①~④制取气体的实验中,选用的反应物及装置均合理的是 (填编号)。
|
编号 |
反应物a |
 反应物b 反应物b |
所制气体 |
装置序号 |
|
① |
浓盐酸 |
MnO2 |
Cl2[来源:学+科+网Z+X+X+K] |
B |
|
② |
浓H2SO4 |
大理石 |
CO2 |
A |
|
③ |
浓HNO3 |
Zn粒 |
H2 |
B |
|
④ |
H2O2 |
MnO2[来源:] |
O2 |
C |
若用装置C来制取氨气和氧气的混合气体,若a是浓氨水 ,则固体粉末b可以是
(填化学式)。
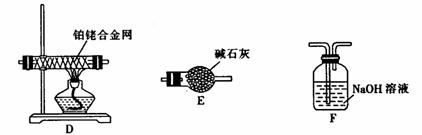 (4)用装置C制取氨气和氧气的混合气体,用装置D、E、F验证氨的还原性。
(4)用装置C制取氨气和氧气的混合气体,用装置D、E、F验证氨的还原性。
①按气流方向,D、E、F装置的顺序是 ,装置F的作用是 。
②装置D中观察到的实验现象是 ,发生反应的化学方程式为 。
28.(13分)已知有五种强电解质溶液,分别含有下列阴、阳离子中的各一种,并且互不重
复。将这五种溶液分别标记为A、B、C、D、E。试回答下列问题:
|
阳离子 |
H+ NH+4 Ba2+ Ag+ Al3+ |
|
阴离子 |
OH- NO-3 CO2-3  SO2-4 Cl- SO2-4 Cl- |
(1)不通过任何实验,根据离子反应的有关知识即可确定其中一种溶质的阴离子为OH-,则这种溶质的阳离子为 ,理由是 。(说明:在溶液中2Al3++3CO2-3+3H2O===2Al(OH)3↓+3CO2↑)
(2)若已知B、C混合后生产白色沉淀,微热混合液有刺激性气体逸出,取B、C溶液少量,分别与A、D、E混合,有关现象如表中所示,“↓”表示有沉淀生成,“↑”表示有气体逸出,“-”表示无明显现象。
|
编号 |
A |
D |
E |
|
B |
↓ |
↓ |
- |
|
C |
↓ |
↓↑ |
↑ |
据此可推断:
①A ,D 。(填化学式)
②写出B与足量D反应的离子方程式: 。
12.某种药物的主要成分x的分子结构为 ,下列关于有机物X的说法中错误的是 ( )
A.X难溶于水,易溶于有机溶剂
B.X的分子式为C12H17O2Be
C.在一定条件下,X能与NaOH水溶液发生取代反应
D.X的水解产物均不能发生消去反应
 13.25℃时,向40 mL 1mol·L-1叫盐酸溶液中逐滴加入0.5mol·L-1的氨水,溶液pH随加入氨水体积的变化曲线如图所示。下列分析中不正确的是 ( )
13.25℃时,向40 mL 1mol·L-1叫盐酸溶液中逐滴加入0.5mol·L-1的氨水,溶液pH随加入氨水体积的变化曲线如图所示。下列分析中不正确的是 ( )
A.h点时,溶液中c(NH+4)=c(Cl-)>c(H+)=c(OH-)
B.x<80
C.a点时,溶液中c(NH+4)+c(H+)=c(Cl-)+c(OH-)
D.c点时,溶液中c(NH+4)>c(Cl-)>c(OH-)>c(H+)
第Ⅱ卷(非选择题)
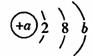 27.(14分)X、Y、Z、W、T是原子序数依次增大的常见元素,Y与X能形成原子个数比分别为1:1、1:2、1:3、1:4等多种共价化合物,T元素的单质在Z元素的单质中
27.(14分)X、Y、Z、W、T是原子序数依次增大的常见元素,Y与X能形成原子个数比分别为1:1、1:2、1:3、1:4等多种共价化合物,T元素的单质在Z元素的单质中
燃烧成一种具有磁性的化合物。W元素的原子
 结构示意图可表示为
结构示意图可表示为
且a=2b+3。试回答下列问题:
(1)X元素的名称是 ,W元素在周期表中的位置是 。
(2)Y元素与Z元素形成的非极性分子的化学式为 。
(3)X元素和Z元素可形成电子数相等的两种离子,两种离子反应后生成一种与这两种粒子的电子数相等的分子,写出该反应的离子方程式: 。
(4)常温下Y元素与X元素按原子个数比1:4组成的化合物8g,完全燃烧放出445.15kJ热量,则表示该化合物燃烧热的热化学方程式是 。
(5)将0.01mol W2单质通入100 mL 0.3mol·L-1TW2溶液中反应,然后在反应后的溶液中加入足量的单质T,则充分反应后,溶液中阳离子(H+忽略)的物质的量浓度为
mol·L-1(忽略溶液体积变化)
11.如图所示,下列有关装置的分析中正确的是 ( )

|
选项 |
开关控制 |
X溶液 |
装置叙述 |
||
|
A |
接通K2,断开Kl |
HCl |
Fe极为正极,该极质量减小 |
||
|
B |
接通K2,断开K1 |
CuCl2 |
Fe极为负极,该极质量增加 |
||
|
C |
接通K1,断开K2 |
CuSO4 |
Fe极为阴极,该极有Cu析出 |
||
|
D |
|
NaCl |
Fe极为阳极,该极逐渐溶解 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com