
29.(16分)某同学用a mol/L的酸性KMnO4溶液测定草酸晶体(H2C2O4·xH2O)中的x值。
(1)称取W g草酸晶体,配成250.00 mL水溶液。
① 在上述过程中必须用到的2种定量仪器是 和 。
② 配制主要步骤有:计算-→称量-→ -→转移-→ -→定容-→摇匀。
(2)量取配得的25.00 mL草酸溶液放入锥形瓶中,用a mol/L的酸性KMnO4溶液进行滴定,用去V mL。
① 量取25.00 mL草酸溶液的仪器是 。
② 配平离子方程式:□MnO-4+□H2C2O4+□H+-→□Mn2++□CO2↑+□H2O
③ 滴定达到终点的标志是 。
(3)由以上数据可得 x= 。
(4)在上述实验中,下列操作(其他操作正确)会造成测定结果偏低的有 。
A. 称取W g草酸晶体时,将草酸晶体放在托盘天平右盘
B. 锥形瓶用蒸馏水洗净后未干燥
C. 滴定终点读数时仰视滴定管刻度
D. 盛KMnO4溶液的酸式滴定管尖嘴部分有气泡,滴定后气泡消失
28.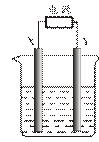 (18分)某化学兴趣小组用图示装置进行电解原理的实验探究。
(18分)某化学兴趣小组用图示装置进行电解原理的实验探究。
(1)X、Y均用石墨作电极,电解质溶液为500 mL CuSO4溶液,电解一段时间,观察到X电极表面有红色的固态物质生成。当电解质溶液中的Cu2+ 全部析出时断开电源,Y电极有280 mL(标准状况)无色气体生成(假设电解前后溶液体积不变)。
① X与电源的 极相连,写出电解总反应的离子方程式: ;② 电解后溶液的pH= ;③ 要使电解后溶液恢复到电解前的状态,需加入一定量的 (填加入物质的化学式)。
(2)用该装置精炼粗铜,电解质溶液仍为CuSO4溶液。① 与电源正极相连的X电极是用 制成的;② 粗铜中含有Zn、Fe、Ni、Ag、Au等杂质,其中有些杂质会在电极上放电,列举其中一个电极反应式: ,阳极泥的主要成分是 。
(3)X、Y均用铜作电极,电解质溶液为 NaOH溶液,电解一段时间,同学们惊奇地发现,阳极附近不是生成蓝色沉淀,而是生成红色沉淀,经过查阅资料,得知该红色沉淀是Cu2O。写出阳极上的电极反应式: ,电解总反应的化学方程式为 。
27.(12分)在2 L密闭容器中加入2 mol A和1 mol B,发生如下反应:
2A(g)+B(g) 4C(g)+D(?)
4C(g)+D(?)
4 min时达到平衡,C的浓度为0.4 mol/L,D的物质的量为0.2 mol。
(1)4 min内,用B物质表示的平均反应速率为 ,A的转化率为 。
(2)若D是气体,升高温度后,混合气体的平均相对分子质量增大,则该反应的正反应是 反应。(填“放热”、“吸热”)
(3)保持温度和体积不变,向平衡混合物中再加入2 mol A、1 mol B,达到新平衡后C的浓度 0.8 mol/L(填“>”、“<”、“=”)。
(4)若D是固体,按不同配比加入起始物质,达到平衡时,C的浓度仍是0.4 mol/L。
①如果从逆反应方向建立平衡,D的起始物质的量应满足的条件是 。
②如果加入0.2 mol A、0.1 mol B,则C和D起始物质的量分别应满足 。
26.(14分)A、B、C、D、E五种短周期元素,原子序数依次递增。A原子形成的阳离子是一个质子,B原子的最外层电子数是次外层的2倍,C原子的最外层电子数与B原子的核外电子总数相等,D在同周期元素中原子半径最大,E与C是同主族元素。C、D两种元素可形成化合物甲,甲中既有离子键又有共价键;A、B、C、D四种元素可形成化合物乙,乙放入水中所得溶液显碱性。请回答:
(1)化合物甲的电子式为 ;乙的化学式有很多种,其中无机物是 ,相对分子质量最小的有机物是 。
(2)气体A2、C2和A、C、D形成的离子化合物的水溶液可形成燃料电池,其正极的电极反应式为 ,电池总反应得到1.8 g产物时,流经外电路某一横截面的电子数为 。
(3)A、B能形成无数种化合物,其中密度最小的气态化合物燃烧热为890.3 kJ/mol,则该化合物燃烧的热化学方程式为 。
(4)都由A、C、D、E形成的两种化合物可以相互反应,其离子方程式为 。
25. (20分)如图所示,质量为m3的平板车C放在光滑水平面上,车上放有A、B两小滑块,质量分别是m1、m2,与平板车上表面间动摩擦因数分别为μ1和μ2。同时分别给A、B一个冲量使它们都获得相同大小的初速度v 0开始相向运动,A、B恰好不相碰。已知m1=10 kg,m2=2 kg,m3=6 kg, μ1=0.1,μ2=0.2, v0=9 m
/ s。g取10 m /s2。求:
(20分)如图所示,质量为m3的平板车C放在光滑水平面上,车上放有A、B两小滑块,质量分别是m1、m2,与平板车上表面间动摩擦因数分别为μ1和μ2。同时分别给A、B一个冲量使它们都获得相同大小的初速度v 0开始相向运动,A、B恰好不相碰。已知m1=10 kg,m2=2 kg,m3=6 kg, μ1=0.1,μ2=0.2, v0=9 m
/ s。g取10 m /s2。求:
(1) A、B都在平板车上不滑动时,C的速度大小v c=?
(2)开始运动前,A、B之间的距离s=?
24. (19分)如图所示,竖直平面内有一段不光滑的斜直轨道与光滑的圆形轨道相切,切点P与圆心O的连线与竖直方向的夹角为θ=60°,圆形轨道的半径为R,一质量为m的小物块从斜轨道上A点由静止开始下滑,然后沿圆形轨道运动,A点相对圆形轨道底部的高度h=7R。物块通过圆形轨道最高点时,与轨道间的压力大小为3mg。求物块与斜直轨道间的动摩擦因数μ=?
(19分)如图所示,竖直平面内有一段不光滑的斜直轨道与光滑的圆形轨道相切,切点P与圆心O的连线与竖直方向的夹角为θ=60°,圆形轨道的半径为R,一质量为m的小物块从斜轨道上A点由静止开始下滑,然后沿圆形轨道运动,A点相对圆形轨道底部的高度h=7R。物块通过圆形轨道最高点时,与轨道间的压力大小为3mg。求物块与斜直轨道间的动摩擦因数μ=?
23.(16分)质量是65 kg的建筑工人,不慎从高空跌下,由于所系的弹性安全带的保护作用,最后使工人悬挂在空中。已知弹性安全带无拉力伸直时长3.2 m。工人下跌时安全带缓冲时间为1.3 s,求安全带对工人的平均冲力的大小?( g = 10 m/s2)
2. 如下左图,是研究牛顿第二定律的实验装置,要求用该装置测定重力加速度g。
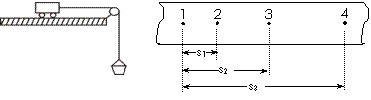
(1)由于木板不光滑,需要平衡摩擦力,其简便方法是_____________。
(2)要用电磁打点计时器测量小车运动的加速度a。
提供的电源有:(A)工作电压为4V-6V的交流电源;(B)工作电压为4V-6V的直流电源;(C)工作电压为220V的交流电源。电源应选用___________(填序号)。
按正确操作得到的一条纸带如上右图所示,打相邻两点的时间间隔为T。则车运动的加速度大小a=___________(用s1、s2、s3和T表示)。
(3)还需要测量的物理量是__________________________________(明确写出物理量的名称和符号),计算重力加速度的公式g=________________________(用该步和 (2) 中测得的物理量表示)。
1. 在“探索弹力和弹簧伸长的关系”实验中:
(1)测量弹簧的总长度,选用的测量工具是___________。
A.刻度尺 B.游标卡尺 C.螺旋测微器
(2)实验得到下表,若g = 10 m/s2,弹簧总长x为自变量,各物理量均用国际单位制中单位,弹簧弹力F的函数关系式为___________。
|
弹簧总长度x/cm |
20.00 |
25.00 |
30.00 |
35.00 |
|
钩码质量m/g |
500 |
1000 |
1500 |
2000 |
22.(17分)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com