
3. 设全集U={0,1,2,3,4},集合A{0,2,4},集合B={0,1,3},则( )
A. B.
B.
C. D.
D.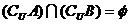
 例1.试用集合A,B的交集、并集、补集分别表示图中Ⅰ,Ⅱ,Ⅲ,Ⅳ四部分所表示的集合.
例1.试用集合A,B的交集、并集、补集分别表示图中Ⅰ,Ⅱ,Ⅲ,Ⅳ四部分所表示的集合.
例2 .设全集为R,A={x|x<5},B={x|x>3},求:
(1)A∩B; (2)A∪B; (3)CRA; CRB;
(4)(CRA)∩(CRB); (5)(CRA)∪(CRB);
(6)CR(A∩B); (7)CR(A∪B)
结论2: ;
;
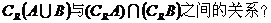
例3.已知全集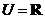 ,集合
,集合 ,
,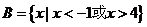
求集合
例4.设全集I={-2,-1,- ,
,  ,
, ,1,2,3},A={
,1,2,3},A={ ,
,  ,1,2,3}, B={-2,2},则集合{-2}等于 ( )
,1,2,3}, B={-2,2},则集合{-2}等于 ( )



 ?A. A∩B ? B.
I A∩B C. I
A∩ I B ?D.A∪
I B
?A. A∩B ? B.
I A∩B C. I
A∩ I B ?D.A∪
I B
练习3:1.U={x|x<20,且x∈N},A={18的正约数},B={12的正约数},求 、
、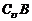 。
。
2.设U=R,A={x|-1<x<2},B={x|1<x<3},求A∩B、A∪B、 、
、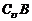 。
。
2.补集:设全集为U, 集合A是U的一个子集(即A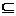 U),则
U),则
组成的集合,叫作U中子集A的补集(或余集),记作:
,读作:“A在U中补集”,即
。补集的Venn图表示如右:
(说明:补集的概念必须要有全集的限制)②结论:集合 是集合U中除去集合A之后余下来的集合。
是集合U中除去集合A之后余下来的集合。 
练习1:U={1,2,3,4,5},A={2,3,4},B=φ,则 = ,
= ,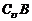 = ;
= ;
结论:A∩C A= , A∪C
A= , A∪C A= ,
C
A= ,
C (C
(C A)=
A)=
[活动过程2]:请同学们讨论:在解方程、不等式时,把什么作为全集?在研究图形集合时,把什么作为全集?
练习2:(1)设U={x|x<8,且x∈N},A={x|(x-2)(x-4)(x-5)=0},则 = ;
= ;
(2)设U={三角形},A={锐角三角形},则 =
。
=
。
(3)设U=R, A={x|
2x-5<0}, =
。
=
。
1. 全集:
的所有元素构成的集合,记作U。
全集:
的所有元素构成的集合,记作U。
24.计算题
将32克铜与100 ml一定浓度的硝酸反应,铜完全溶解,产生的NO和 NO2在标准状况下的体积为11.2L。请计算:(写出计算过程)
(1) NO和 NO2的体积分别是多少?
(2)待产生的气体全部释放后,向溶液中加入Vml amol/L的NaOH溶液,恰好使溶液中的
的Cu2+ 全部转化为沉淀,则原溶液的浓度为多少?
(3)欲使铜与硝酸反应生成的气体在NaOH溶液中全部转化为NaNO3 ,至少需要O2的体积是多少?
23.下列是中学化学中常见物质间的反应转化关系图,其中部分产物已略去。常温下,G为固体单质,B、I为液体,其余都为气体。A为化合物,I的浓溶液与G在加热条件下生成F、B和C。H可用作工业上冶炼金属的还原剂。请按要求填空:


 A
D
A
D
|
B E
C H
(1) 写出下列物质的化学式:A_________;B_________;C___________
(2) 写出F+B→I的化学方程式___________________________________
(3) 写出G和I的浓溶液反应的化学方程式______________________________________ .
22.今有一无色透明溶液,只可能含有以下离子中的若干中:K+、H+、Mg2+、Fe3+、Ba2+、SO42-、CO32-、NO3- ,现取二份各100 mL溶液进行如下实验:
①第一份加足量NaHCO3 溶液加热后,收集到气体0.04mol
② 第二份加足量Ba(NO3)2 溶液充分反应后过滤干燥,得沉淀4.66g.
根据上述实验回答
⑴溶液中一定不存在的离子是______________________;
⑵溶液中可能存在的离子是________________________;
⑶ 写出①发生反应的离子方程式
_________________________________________________________;
⑷写出②发生反应的离子方程式
__________________________________________________________.
21.用98%的浓H2SO4(密度是1.84g/cm3)配制成0.5 mol/L的稀H2SO4500mL的操作步骤如下:①计算所用浓硫酸的体积 ②量取一定体积的浓硫酸 ③溶解④转移、洗涤 ⑤定容、摇匀,请按要求填空:
⑴需量取的浓硫酸体积为______,应选用______量筒(实验室有10mL,20mL,50mL的量筒).
⑵.本实验需用到的基本实验仪器除烧杯、玻璃棒外还有:
__________________________________________________ 。
⑶.某学生的下列操作中使浓度偏低的是:___________
①用量筒量取浓硫酸时,仰视读数。
②量筒中浓硫酸全部转入烧杯中稀释后,再转移到100mL容量瓶中,烧杯未洗涤。
③用玻璃棒引流,将溶液转移到容量瓶中有溶液流到了容量瓶外面。
④用胶头滴管加蒸馏水时,加入过快而使液面超过了刻度线,立即用滴管吸去多余的水,使溶液凹液面刚好与刻度线相切。
⑤滴加蒸馏水,使溶液凹液面刚好与刻度线相切,盖上瓶塞反复摇匀后,静置,发现液面比刻度线低,再加水至刻度线。
⑥溶液定容时,俯视容量瓶刻度线。
20.已知常温下,在溶液中发生如下反应:
① 16H++10Z-+2XO4-===2X2++5Z2+8H2O; ② 2A2++B2===2A3++2B-;
③ 2B-+Z2===B2+2Z-
由此判断下列说法错误的是 ( )
A. 反应Z2+2A2+===2A3++2 Z-可以进行
B. Z元素在①的反应中被氧化
C. 氧化性由强到弱的顺序是:XO4-、Z2、B2、A3+
D. 还原性由强到弱的顺序是:Z-、B-、A2+、X2+
第Ⅱ卷(共40分)
19.用NA表示阿伏加德罗常数的值,下列说法正确的是 ( )
A.46gNO2和N2O4混合气体中含有的分子总数为NA
B.用含4molHCl的浓盐酸跟足量二氧化锰反应,生成的氯气在标准状况下的体积为22.4L
C.0.1mol金属钠与氧气在一定条件下发生反应,生成钠的氧化物的混合物时,失去的电子数为0.1NA
D.1mol苯中含有3NA个碳碳双键
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com