
5.比较N、P两点气温的大小关系,并指出其影响因素
A.N>P 地形 B.N>P 纬度
C.N<P 洋流 D.N<P 海陆分布
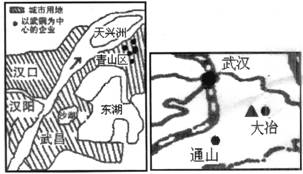
4.下列选项不是武钢选址青山区的区位因素是
A.原料 B.环境 C.市场 D.能源
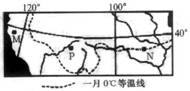 读某区域1月份0℃等温线分布图,回答5-7题。
读某区域1月份0℃等温线分布图,回答5-7题。
3.武汉的城市地域形态及天兴洲形成的
地质作用分别是
A.集中式,流水侵蚀作用
B.放射状,流水沉积作用
C.组团式,流水沉积作用
D.条带状,流水侵蚀作用
2.从总体趋势来看,在东西方向上,能源消费
重心走势趋向于GDP重心。能源消费与
GDP增长的耦合,说明:
A.我国GDP增长中能源成本较大
 B.我国GDP高的地区能源资源丰富
B.我国GDP高的地区能源资源丰富
C.我国能源供需地区不平衡的状况
已基本解决
D.我国能源消费与GDP均实现了
可持续发展
读右图并结合所学知识完成3-4题
10、阿司匹林(乙酰水杨酸)是常用的解热镇痛药,以下是合成阿司匹林的工艺流程。
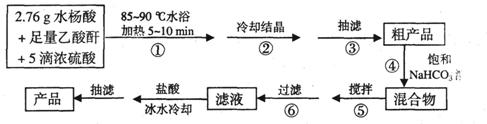
已知:①反应方程式为
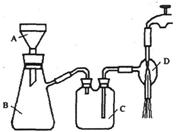
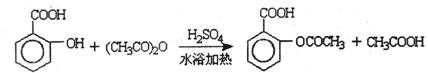
②抽滤的实验装置如右图所示。
请回答有关问题:
(1)仪器A的名称是_____________。
(2)在步骤②中,若冷却结晶时未出现结晶,可以___________,促使晶体析出。
(3)实验时,当仪器B中液面高度快达到支管口位置时,应进行的操作是_______________。
(4)仪器C中两玻璃导管的位置是否正确?答:_________。(填“正确”或“不正确”)
(5)在步骤④中,用饱和NaHC03溶液可以将阿司匹林和剐产物等分离,其化学原理是
_________________________________________。要检测产品中是否含有水杨酸,其实验操作是__________________________________ ___________________。
(6)在步骤⑤中,搅拌使反应充分进行至____________为止。
(7)若实验得到2.70g纯净的阿司匹林,则产品的产率为____________。
11 、已知:一个碳原子上连有两个羟基时不稳定,易发生下列转化:
、已知:一个碳原子上连有两个羟基时不稳定,易发生下列转化:
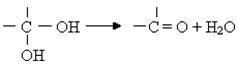
某烃A的蒸气密度是相同状况下氢气的53倍,烃A不能使溴的CCl4溶液褪色,但能使酸性KMnO4溶液褪色。氢原子核磁共振谱图表明A有2个吸收峰,强度之比为3∶2,B只有1个吸收峰,D有2个吸收峰,G为环状结构。A可以发生如右图所示的一系列变化(生成的其它无机物均未写出)。请回答下列问题:
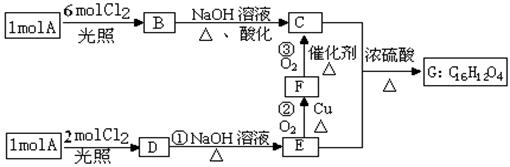
(1)A的分子式是_ _。
(2)指出下列反应的反应类型:①_ _、③_ _。
(3)写出B、G的结构简式:B_ _、G_ _。
(4)写出下列反应的化学反应方程式:反应②_ _;
C和E还能生成高分子化合物,请写出其反应的化学方程式_ _。
(5)写出满足下列条件的E的所有同分异构体的结构简式(E不必再写):_ _。
①遇FeCl3溶液显紫色;②能发生消去反应生成碳碳双键。
9、甲醇被称为2l世纪的新型燃料,工业上通过下列反应Ⅰ和Ⅱ,用CH4和H2O为原料来制备甲醇。
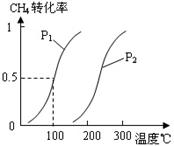 (1)将1.0 mol CH4和2.0 mol H2O(g)通入反应室(容积为
(1)将1.0 mol CH4和2.0 mol H2O(g)通入反应室(容积为
100L),在一定条件下发生反应:CH4(g)+H2O(g)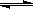
CO(g)+3H2(g)……Ⅰ,CH4的转化率与温度、压强的关
系如右图。
①已知100℃时达到平衡所需的时间为5min,则用H2表
示的平均反应速率为_ _。
②图中的P1_ _P2(填“<”、“>”或“=”),100℃时平衡
常数为_ _。
③在其它条件不变的情况下降低温度,逆反应速率将_ _(填“增大”、“减小”或“不变”)。
(2)在压强为0.1 MPa条件下, 将a mol CO与 3a mol
H2的混合气体在催化剂作用下能自发反应生成甲醇:CO(g)+2H2(g)
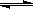 CH3OH(g) ……Ⅱ。
CH3OH(g) ……Ⅱ。
④该反应的△H_ _0,△S_ _0(填“<”、“>”或“=”)。
⑤若容器容积不变,下列措施可增加甲醇产率的是_ _。
A.升高温度 B.将CH3OH(g)从体系中分离
C.充入He,使体系总压强增大 D.再充入1mol CO和3mol H2
⑥为了寻找合成甲醇的温度和压强的适宜条件,某同学设计了
三组实验,部分实验条件已经填在下面实验设计表中。
|
1.
实验编号 |
2.
T(℃) |
3.
n (CO)/n(H2) |
4.
P(MPa) |
|
5.
ⅰ |
6.
150 |
7.
1/3 |
8.
0.1 |
|
9.
ⅱ |
10.
_ _ |
11.
_ _ |
12.
5 |
|
13.
ⅲ |
14.
350 |
15.
_ _ |
16.
5 |
A.请在上表空格中填入剩余的实验条件数据。
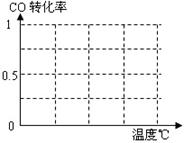
B.根据反应Ⅱ的特点,在给出的坐标图中,画出其在0.1MPa和5MPa条件下CO的转化率随温度变化的趋势曲线示意图,并标明各条曲线的压强。
8、下图所示各物质是由短周期元素组成的单质及其化合物,图中部分反应条件及生成物未列出。其中A、D、K为单质,其元素在周期表中分处不同周期,且原子最外层电子数:A原子是D原子的两倍,K原子是A原子的两倍;E是能使湿润的红色石蕊试纸变蓝的气体,工业上常用C的无水晶体制备A。
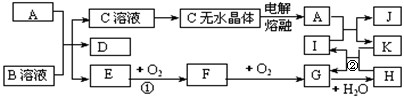

请按要求回答:
(1)写出A的化学式_ ,I的电子式_ _。
(2)从C溶液制备C无水晶体的操作要点是_ 。
(3)写出有关反应的化学方程式:
反应①_ _;反应②_ _。
(4)常温下,B溶液的PH_ _7(填>、<或=),请用离子方程式表示其原因:_
_ 。
7、短周期元素X、Y、Z原子序数依次递增且原子序数和为32, Y、Z在同一周期但不相邻,Z的最外层电子数等于其电子层数。下列有关叙述不正确的是………………( )
A.X、Y两元素能形成化合物Y2X、Y2X2
B.Z的最高价氧化物对应的水化物既能与强酸反应又能与强碱反应
C.Y、Z所在周期的所有元素中Y的金属性最强
D.X元素形成的单质不可能存在同素异形现象
6、美籍华裔科学家钱永键、日本科学家下修村和美国科学家马丁·沙尔菲因在发现和研究绿色荧光蛋白(GFP)方面做出突出贡献而分享了2008年诺贝尔化学奖。经研究发现GFP中的生色基团结构如图所示,下列有关GFP的说法中正确的是……………………………( )
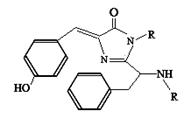 A.该有机物属于芳香烃
A.该有机物属于芳香烃
B.该有机物不能发生水解反应
C.该有机物与溴水既能发生加成反应,又能发生取代反应
D.该有机物既能与盐酸反应,又能与碳酸氢钠溶液反应
5、镁及其化合物一般无毒(或低毒)、无污染,且镁原电池放
电电时压高而平稳,使镁原电池越来越成为人们研制绿色原电池的关注焦点。其中一种镁原
电池的反应为:xMg+Mo3S4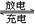 MgxMo3S4,下列说法错误的是:……………( )
MgxMo3S4,下列说法错误的是:……………( )
A.放电时,负极反应为Mg-2e-=Mg2+ B.放电时,Mo3S4发生氧化反应
C.放电过程中Mg2+向正极迁移 D.充电时,阳极反应为MgxMo3S4-2xe-=Mo3S4+xMg2+
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com