
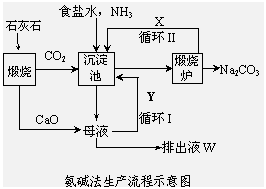
15.联碱法(候氏制碱法)和氨碱法的生产流程简要表示如下图:
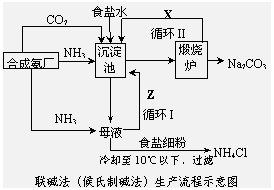
(1)沉淀池中发生反应的化学方程式为_______________________;
(2)X是________,Y是_______(填化学式);
(3)Z中除了溶解的氨气、食盐外,其它溶质还有________________________________;排出液W中的溶质除了氢氧化钙外,还有________________________;
(4)从理论上分析,在氨碱法生产过程中_________(填“需要”、“不需要”)补充氨气,从原料到产品,氨碱法总反应过程用化学方程式表示,可写为 ;
(5)根据联碱法中从母液中提取氯化铵晶体的过程推测,所得结论正确是_____;
a.常温时氯化铵的溶解度比氯化钠小
b.通入氨气目的是使氯化铵更多析出
c.加入食盐细粉目的是提高Na+的浓度, 促进碳酸氢钠结晶析出
(6)联碱法中,每当通入NH3 44.8L(已折合成标准状况下)时可以得到纯碱100.0g,则NH3的利用率为______。相比于氨碱法,指出联碱法的一项优点_________________。
14. 工业上用铝土矿(主要成分为Al2O3,含Fe2O3等杂质)为原料冶炼铝的工艺流程如下:
工业上用铝土矿(主要成分为Al2O3,含Fe2O3等杂质)为原料冶炼铝的工艺流程如下:



|


 对上述流程中的判断正确的是
对上述流程中的判断正确的是
 A.试剂X为稀硫酸
A.试剂X为稀硫酸
 B.反应 II 中生成Al(OH)3的反应为:CO2+AlO2-+2H2O==Al(OH)3↓+HCO3-
B.反应 II 中生成Al(OH)3的反应为:CO2+AlO2-+2H2O==Al(OH)3↓+HCO3-
 C.结合质子 ( H+)
的能力由强到弱的顺序是OH―>AlO2―>CO32-
C.结合质子 ( H+)
的能力由强到弱的顺序是OH―>AlO2―>CO32-
 D.Al2O3熔点很高,工业上还可采用电解熔融AlCl3冶炼Al
D.Al2O3熔点很高,工业上还可采用电解熔融AlCl3冶炼Al
13.下列有关四幅图像叙述正确的是
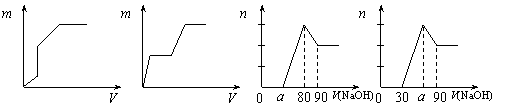

A. B. C. D.
A.向盐酸酸化的MgSO4溶液中加入Ba(OH)2溶液,产生的沉淀质量m与加入的体积V之间的关系不可能是图I
B.向盐酸酸化的MgSO4溶液中加入Ba(OH)2溶液,产生的沉淀质量m与加入的体积V之间的关系有可能是图Ⅱ
C.把一块镁铝合金投入到1mol/L HCl溶液里,待合金完全溶解后,往溶液里加入1mol/I NaOH溶液,生成沉淀的物质的量随加入NaOH溶液体积变化的关系如图Ⅲ所示,则n(Mg)/n(A1)的最大值为2
D.把一块镁铝合金投入到1mol/L HCl溶液里,待合金完全溶解后,往溶液里加入1mol/L NaOH溶液,生成沉淀的物质的量随加入NaOH溶液体积变化的关系如图Ⅳ所示,则a的取值范围为80<a<90
12. 以下物质间的相互转化关系中(如图),A、B、C是常见的金属或非金属单质,D、E、F是常见的三种氧化物,常温下,D、E呈气态,F呈固态。下列推断正确的是
以下物质间的相互转化关系中(如图),A、B、C是常见的金属或非金属单质,D、E、F是常见的三种氧化物,常温下,D、E呈气态,F呈固态。下列推断正确的是
A.E和D中一定有A元素 B.A一定是金属单质
C.单质B肯定是氧化剂 D.C一定是氧气
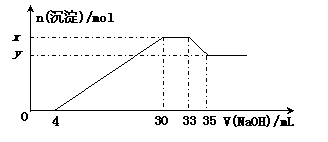
11. 在200 mL含Mg2+、Al3+、NH4+、H+、Cl-等离子的溶液中,逐滴加入5mol•L-1的氢氧化钠溶液,所加氢氧化钠溶液的体积(mL)与产生沉淀的物质的量(mol)关系如下图所示。
 下列叙述正确的是
下列叙述正确的是
A.x与y的差值为0.01 mol
B.原溶液中c(Cl-)=0.75 mol·L-1
C.原溶液的pH=1
D.原溶液中n(Mg2+)∶n(Al3+)=5∶2
10.下列离子方程式正确的是
A.氯化银可被NaCN溶液所溶解:AgCl+2CN-=[Ag(CN)2]-+C1-
B.亚磷酸是一种二元酸,在其中加入过量的烧碱溶液:H3PO3+3OH-=PO33-+3H2O
C.硫酸亚铁和稀硫酸的混合溶液中滴入双氧水:Fe2++H2O2+H+=Fe3++H2O
D.硫代乙酰胺(CH3CSNH2)滴入热的强碱溶液中,以提供硫离子。
CH3CSNH2+3OH-=CH3COO-+S2-+NH3↑+H2O
9.将质量为w1g的钠、铝混合物投入一定量的水中充分反应,金属没有剩余,共收集到标准状况下的气体V1 L。向溶液中逐滴加入浓度为a mol/L的HCl溶液,过程中有白色沉淀生成后又逐渐溶解,当沉淀恰好消失时所加HCl溶液体积为V2 L。将溶液蒸干灼烧得固体w2g。下列所列关系式中正确的是
A. 35.5a V2 =w2-w1 B. 23n(Na)+27n(Al)=w1
C. n(Na)+3n(Al)=2V1/22.4 D. a V2 =V1/22.4
8. 化合物A、B、C、D各由两种元素组成,甲、乙、丙是前两周期元素的三种单质。这些常见的化合物与单质之间存在如下关系(已知C是一种有机物),以下结论不正确的是:
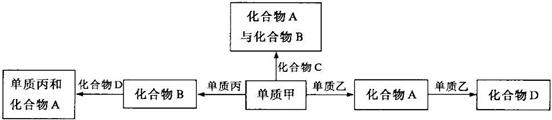
A.上图所示的五个转化关系中,有三个是化合反应
B.上述转化关系所涉及的化合物中有一种是电解质
C.甲、乙、丙三种单质的晶体一定是分子晶体
D.上图所示的五个转化关系中,均为氧化还原反应
选择题:每题有1-2个正确答案
7.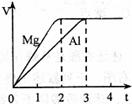
 镁和铝分别与等浓度、等体积的过量稀硫酸反应,产生
镁和铝分别与等浓度、等体积的过量稀硫酸反应,产生 气体的体积(V)与时间(t)关系如右图。反应中镁和铝的
气体的体积(V)与时间(t)关系如右图。反应中镁和铝的
 A.物质的量之比为3:2
B.质量之比为3:2
A.物质的量之比为3:2
B.质量之比为3:2
 C.摩尔质量之比为2:3
D.反应速率之比为2:3
C.摩尔质量之比为2:3
D.反应速率之比为2:3
6. 向m g镁和铝的混合物中加入适量的稀硫酸,恰好完全反应生成标准状况下的气体b L。向反应后的溶液中加入c mol/L氢氧化钾溶液V mL,使金属离子刚好沉淀完全,得到的沉淀质量为n g。再将得到的沉淀灼烧至质量不再改变为止,得到固体p g。则下列关系不正确的是
A.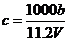 B.
B.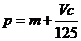 C.n=m+17Vc D.
C.n=m+17Vc D.  <
<  <
<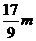
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com