
 读世界某区域略图,回答8-10题。
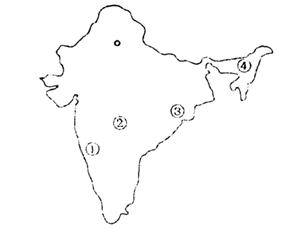
读世界某区域略图,回答8-10题。
8.该国大量进口粮食的主要原因是
A.多水旱灾害 B.人口众多
C.耕地面积小 D.土壤贫瘠
9.若该国从美国大量进口粮食,合理的运输线应经过
A.苏伊士运河 B.巴拿马运河
C.马六甲海峡 D.合恩角
10.有关图上数码所在地的正确说法是
A.①地盛产黄麻
B.①地降水量比②③④地都多
C.③地铁、锰资源丰富
D.④地土壤呈碱性
依据图3中信息回答6-7题(图中圆圈大小表示贸易总额多少,
白色部分表示出口,黑色部分表示进口。)
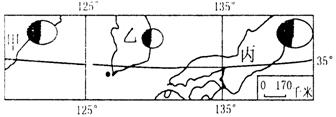
图3
6.下列关于甲、乙、丙三国的说法正确的是
A.甲、乙、丙三国的贸易进出口构成均为进口大于出口
B.三国出口产品都以农副产品为主
C.甲、丙间贸易额大于甲、乙间贸易额
D.甲、乙、丙三国之间都有陆地部分相连
7.甲、乙、丙三国,图中所示区域地理特征相似的是
A.粮食作物都以水稻为主 B.均有本国最大的工业基地
C.均为雨热同期 D.都有本国最大港口
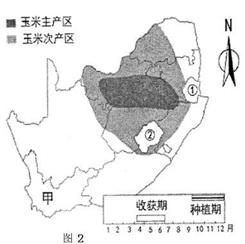 下图2显示的是某国家( 图中①②不属该国领土
) 玉米生产区的分布和种植、收获玉米的时间。该国在黄金和钻石等矿产品发现之前,就曾经是个以农业为主的国家。据此并读图完成 3-5 题。
下图2显示的是某国家( 图中①②不属该国领土
) 玉米生产区的分布和种植、收获玉米的时间。该国在黄金和钻石等矿产品发现之前,就曾经是个以农业为主的国家。据此并读图完成 3-5 题。
3. 依提供信息可知,该国王米产区主要分布在
A. 平原地形区 B. 高原地形区
C. 丘陵地形区 D. 盆地地形区
4. 该因甲省区的气候有别于玉米主要产区的气候,当收获玉米
时期甲省区主要收割或采摘的是
A. 小麦 B. 棉花 C. 葡萄 D. 甘蔗
5. 该国重点防治的环境问题是
A. 森林锐减 B. 蛙虫灾害
C. 水土流失 D. 大气污染
图1为“美国本土小麦区和玉米带分布示意图”。读图完成1-2题。
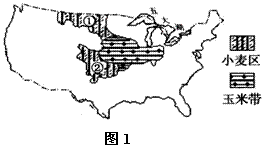
1.图中阴影地区主要农业地域类型是
A.季风水田农业 B.混合农业 C.大牧场放牧业 D.商品谷物农业
2.与①小麦区相比,②小麦区农业生产的主要有利因素是
A.地形 B.热量 C.政策 D.市场
21. 某化学课外研究小组拟对一种焰火原料(由两种短周期中的常见金属元素的单质组成的合金粉末)进行探究。请完成下列探究报告。
某化学课外研究小组拟对一种焰火原料(由两种短周期中的常见金属元素的单质组成的合金粉末)进行探究。请完成下列探究报告。
 [探究目的]探究该焰火原料的组成
[探究目的]探究该焰火原料的组成
 [资料检索]
[资料检索]
①
 Mg2+检验的方法:取2滴待检液,加入2滴2mol·L-1NaOH溶液,再加入2滴镁试剂(I)染料(对硝基苯偶氮苯二酚)。若出现沉淀并吸附镁试剂(I)染料呈天蓝色,表示待测液中含有Mg2+。注:Ag+、Cu2+、Fe3+、NH4+会妨碍Mg2+的检测
Mg2+检验的方法:取2滴待检液,加入2滴2mol·L-1NaOH溶液,再加入2滴镁试剂(I)染料(对硝基苯偶氮苯二酚)。若出现沉淀并吸附镁试剂(I)染料呈天蓝色,表示待测液中含有Mg2+。注:Ag+、Cu2+、Fe3+、NH4+会妨碍Mg2+的检测
②
 Mg(OH)2可溶于浓的氯化铵溶液,其他的常见不溶性碱难溶于氯化铵溶液
Mg(OH)2可溶于浓的氯化铵溶液,其他的常见不溶性碱难溶于氯化铵溶液
③
 很多合金是金属互化物,有确定的化学组成。
很多合金是金属互化物,有确定的化学组成。
 [探究思路]①确定该焰火原料所含金属种类;②测定该火焰原料的化学式
[探究思路]①确定该焰火原料所含金属种类;②测定该火焰原料的化学式
 [实验探究](1)甲同学进行了初步试验,实验步骤和实验现象如下。请填写下表。
[实验探究](1)甲同学进行了初步试验,实验步骤和实验现象如下。请填写下表。
 试验序号 试验序号 |
实验步骤 |
实验现象 |
结论 |
|
①
|
取少量该焰火原料, 加入冷水 |
无明显现象 |
|
|
② |
取少量该焰火原料, 加入稀盐酸 |
完全溶解,有大量气体 产生、溶液呈无色 |
|
(2)乙同学取甲同学第②组实验的溶液,加入镁试剂(I)染料,未见天蓝色物质。他得出合金中不含镁离子的结论。乙同学的结论 ,(选填“正确”或“错误”)你的理由是 。
(3)丙同学设计实验方案,确定焰火原料中的金属种类,实验记录如下
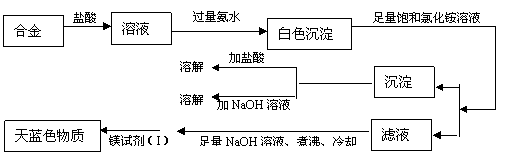
由丙同学的实验记录可知该焰火原料是由 和 两种金属组成的合金;
实验中滤液加入足量氢氧化钠溶液后需煮沸的理由是 。
(4)丁同学利用丙同学的结论,设计如下图所示的实验步骤,确定合金组成。

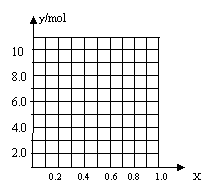 问题讨论:
问题讨论:
①能确定合金组成的数据组有 (填写选项字母)。
A.m、n B. m、y C.n、y
②若合金中相对原子质量较小的金属的物质的量分数为x,
金属总物质的量为7mol,试在右图中作出y随x变化的曲线;
③当y=8.5mol时,该合金是一种金属互化物,其化学式为
。
20.硫酸铜是一种应用极其广泛的化工原料。以下是某工厂用含铁废铜为原料生产胆矾(CuSO4·5H2O)的生产流程示意图:
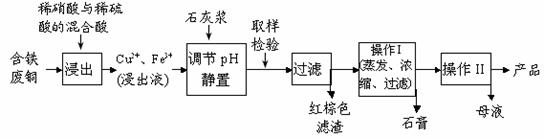
胆矾和石膏在不同温度下的溶解度(g/100g水)见下表。
|
温度(℃) |
20 |
40 |
60 |
80 |
100 |
|
石膏 |
0.32 |
0.26 |
0.15 |
0.11 |
0.07 |
|
胆矾 |
32 |
44.6 |
61.8 |
83.8 |
114 |
请回答下列问题:
(1)红棕色滤渣的主要成分是 ;
(2)写出浸出过程中生成硫酸铜的化学方程式 ;
(3)操作I的操作温度应该控制在 ℃左右;
(4)从溶液中分离出硫酸铜晶体的操作II应为 、洗涤、干燥;
(5)反应产物中的NO可以循环使用,试仅用一个化学方程式表示NO转化为HNO3 。
19. 铁和铝是两种重要的金属,它们的单质及化合物有着各自的性质。
铁和铝是两种重要的金属,它们的单质及化合物有着各自的性质。
 (1)在一定温度下,氧化铁可以与一氧化碳发生反应:
(1)在一定温度下,氧化铁可以与一氧化碳发生反应:

 ①该反应的平衡常数表达式为:K=
①该反应的平衡常数表达式为:K=
 ②该温度下,在2L盛有
②该温度下,在2L盛有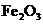 粉末的密闭容器中通入CO气体,10min后,生成了单
粉末的密闭容器中通入CO气体,10min后,生成了单 质铁11.2g。则10min内CO的平均反应速率为
质铁11.2g。则10min内CO的平均反应速率为
 (2)请用上述反应中某种气体的有关物理量来说明该反应已达到平衡状态:
(2)请用上述反应中某种气体的有关物理量来说明该反应已达到平衡状态:
 ①
②
①
②
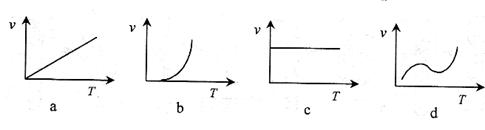
 (3)某些金属氧化物粉末和Al粉在镁条的引燃下可以发生铝热反应。下列反应速率(v)
(3)某些金属氧化物粉末和Al粉在镁条的引燃下可以发生铝热反应。下列反应速率(v) 和温度(T)的关系示意图中与铝热反应最接近的是
。
和温度(T)的关系示意图中与铝热反应最接近的是
。

 (4)写出氢氧化铝在水中发生酸式电离的电离方程式:
(4)写出氢氧化铝在水中发生酸式电离的电离方程式:
 欲使上述体系中
欲使上述体系中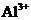 浓度增加,可加入的物质是
。
浓度增加,可加入的物质是
。
18.以富含硫酸亚铁的工业废液为原料生产氧化铁的工艺如下(部分操作和条件略);
I 从废液中提纯并结晶出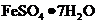 。
。
II将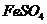 溶液与稍过量的
溶液与稍过量的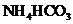 溶液混合,得到含
溶液混合,得到含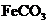 的浊液
的浊液
IV 将浊液过滤,用90°C热水洗涤沉淀,干燥后得到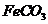 固体
固体
V锻烧碳酸亚铁,得到到氧化铁固体
已知: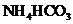 在热水中分解
在热水中分解
(1)I中,加足量的铁屑除去废液中的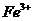 ,该反应的离子方程式是
,该反应的离子方程式是
(2)II中,需加一定量硫酸,运用化学平衡原理简述硫酸的作用
(3)III中,生成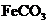 的离子方程式是
。若
的离子方程式是
。若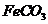 浊液长时间暴露在空气中,会有部分固体表面变为红褐色,该变化的化学方程式是
。
浊液长时间暴露在空气中,会有部分固体表面变为红褐色,该变化的化学方程式是
。
(4)IV中,通过检验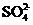 来判断沉淀是否洗涤干净。检验
来判断沉淀是否洗涤干净。检验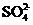 操作是 。
操作是 。
(5)已知煅烧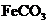 的化学方程式是
的化学方程式是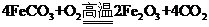 ,现煅烧464.0kg的
,现煅烧464.0kg的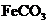 ,得到316.8kg产品,若产品中杂质只有
,得到316.8kg产品,若产品中杂质只有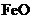 ,则该产品中氧化铁的质量是
______kg(摩尔质量/g·
,则该产品中氧化铁的质量是
______kg(摩尔质量/g·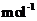 ;
;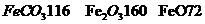 )
)
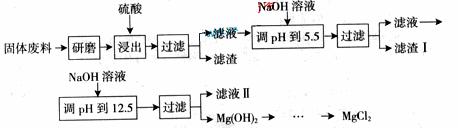
17.  某工厂生产硼砂过程中产生的固体废料,主要含有MgCO3、MgSiO3、 CaMg(CO3)2、Al2O3和Fe2O3等,回收其中镁的工艺流程如下:
某工厂生产硼砂过程中产生的固体废料,主要含有MgCO3、MgSiO3、 CaMg(CO3)2、Al2O3和Fe2O3等,回收其中镁的工艺流程如下:

|
沉淀物 |
Fe(OH)3 |
Al(OH)3 |
Mg(OH)2 |
|
PH |
3.2 |
5.2 |
12.4 |
 部分阳离子以氢氧化物形式完全沉淀时溶液的pH见上表,请回答下列问题:
部分阳离子以氢氧化物形式完全沉淀时溶液的pH见上表,请回答下列问题:
 (1)“浸出”步骤中,为提高镁的浸出率,可采取的措施有
(要求写出两条)。
(1)“浸出”步骤中,为提高镁的浸出率,可采取的措施有
(要求写出两条)。
 (2)滤渣I的主要成分有 。
(2)滤渣I的主要成分有 。
 (3)从滤渣Ⅱ中可回收利用的主要物质有 。
(3)从滤渣Ⅱ中可回收利用的主要物质有 。
 (4)Mg(ClO3)2在农业上可用作脱叶剂、催熟剂,可采用复分解反应制备:
(4)Mg(ClO3)2在农业上可用作脱叶剂、催熟剂,可采用复分解反应制备:
 MgCl2+2NaClO3===Mg(ClO3)2+2NaCl
MgCl2+2NaClO3===Mg(ClO3)2+2NaCl
 已知四种化合物的溶解度(S)随温度(T)变化曲线如下图所示:
已知四种化合物的溶解度(S)随温度(T)变化曲线如下图所示:

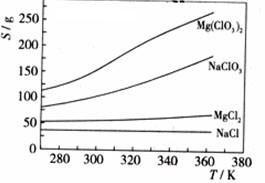
 ①将反应物按化学反应方程式计量数比混合制备Mg(ClO3)2。简述可制备Mg(ClO3)2的原因:
。
①将反应物按化学反应方程式计量数比混合制备Mg(ClO3)2。简述可制备Mg(ClO3)2的原因:
。
 ②按①中条件进行制备实验。在冷却降温析出Mg(ClO3)2过程中,常伴有NaCl析出,原因是:
。除去产品中该杂质的方法是:
。
②按①中条件进行制备实验。在冷却降温析出Mg(ClO3)2过程中,常伴有NaCl析出,原因是:
。除去产品中该杂质的方法是:
。
16.下图所示各物质是由1-20号元素中部分元素组成的单质或其化合物,图中部分反应条件未列出。已知C、H是无色有刺激性气味的气体,D是一种黄绿色的气体单质,物质J可用于饮水消毒。反应②和④是化工生产中的重要反应,反应⑤是实验室制备气体C的重要方法。
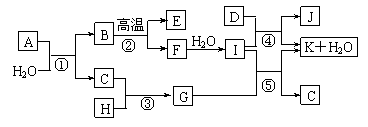
请回答下列问题:
⑴物质E的电子式是____________;物质J的名称为 。
⑵反应⑤的化学方程式为___________________________________________。
⑶反应③的现象为___________________________________________。
⑷物质A由三种元素组成,1molA与水反应可生成1molB和2molC,A的化学式为________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com