
9.下列化学反应中,为使平衡体系析出更多的银,可采取的措施是
Ag++ Fe2+  Ag(固体)+ Fe3+(正反应放热)
A . 常温下加压 B . 增加Fe3+的浓度
C . 增加Fe2+的浓度 D. 移去一些析出的银
Ag(固体)+ Fe3+(正反应放热)
A . 常温下加压 B . 增加Fe3+的浓度
C . 增加Fe2+的浓度 D. 移去一些析出的银
8.下列事实不能用勒夏特列原理解释的是 A.光照氯水,颜色变浅
B.实验室中常用排饱和食盐水的方法收集氯气
C.工业上生产硫酸的过程中使用过量的空气以提高二氧化硫的利用率
D.压缩H2与I2(g)反应的平衡混合气体,颜色变深
7. 在一密闭烧瓶中,在25℃时存在着平衡:2NO2  N2O4(正反应放热)。把烧瓶置于100℃的水中,则下列几项性质中不会改变的是
①颜色 ②平均相对分子质量 ③质量 ④压强 ⑤密度
A.③和⑤ B .②和④ C. ④和⑤ D .①和③
N2O4(正反应放热)。把烧瓶置于100℃的水中,则下列几项性质中不会改变的是
①颜色 ②平均相对分子质量 ③质量 ④压强 ⑤密度
A.③和⑤ B .②和④ C. ④和⑤ D .①和③
6.密闭容器中存在化学反应: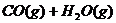

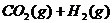 当反应容器中充入1molCO和1mol水蒸气,在一定条件下达到平衡时生成了0.67molCO2,当充入的水蒸气改为4mol,其它条件不变,平衡时生成的CO2的物质的量可能为( )
当反应容器中充入1molCO和1mol水蒸气,在一定条件下达到平衡时生成了0.67molCO2,当充入的水蒸气改为4mol,其它条件不变,平衡时生成的CO2的物质的量可能为( )
A.0.5 mol B.1mol C. 0.95 mol D. 0. 67mol
5. 在化学平衡状态的体系中,如果下列物理量发生变化,其中一定能表明平衡移动的是 A. 反应物的转化率 B. 反应混和物的浓度 C . 正、逆反应速率 D. 反应混和物的压强
4. 四氯化硅还原法是当前制备较高纯度硅的一种方法,有关反应的化学方程式为:SiCl4 + 2H2 4HCl
+ Si, 下列说法不合理的是
A.反应制得的硅可用于制造半导体材料
B.增大压强有利于加快上述反应的化学反应速率
C.四氯化硅可以由粗硅与氯气通过化合反应制得
D.混入少量空气对上述反应无影响
4HCl
+ Si, 下列说法不合理的是
A.反应制得的硅可用于制造半导体材料
B.增大压强有利于加快上述反应的化学反应速率
C.四氯化硅可以由粗硅与氯气通过化合反应制得
D.混入少量空气对上述反应无影响
3. 对已达到平衡的反应:2X(g)+Y(g) 2Z(g),减小压强时,下列说法正确的是
A.逆反应速率增大,正反应速率减小,平衡向逆反应方向移动
B.逆反应速率减小,正反应速率增大,平衡向正反应方向移动
C.正、逆反应速率都减小,平衡向逆反应方向移动
D.正、逆反应速率都增大,平衡向正反应方向移动
2Z(g),减小压强时,下列说法正确的是
A.逆反应速率增大,正反应速率减小,平衡向逆反应方向移动
B.逆反应速率减小,正反应速率增大,平衡向正反应方向移动
C.正、逆反应速率都减小,平衡向逆反应方向移动
D.正、逆反应速率都增大,平衡向正反应方向移动
2. 能使碳酸钙的分解速率显著增大的措施是 A .升高温度 B .增加少量的CaCO3 固体 C.加入MnO2 D. 增大压强
1.下列说法正确的是 A.可逆反应的特征是正反应速率和逆反应速率相等 B.在其他条件不变时,使用催化剂只能改变反应速率,而不能改变化学平衡状态 C.在其他条件不变时,升高温度可以使平衡向放热反应方向移动 D.在其他条件不变时,增大压强一定会破坏气体反应的平衡状态
12、故人西辞黄鹤楼,烟花三月下扬州。--李白《送孟浩然之广陵》
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com