
7、若直线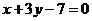 ,
,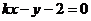 和x轴、y轴围成的四边形有外接圆,则实数k 等于
( )
和x轴、y轴围成的四边形有外接圆,则实数k 等于
( )
A.1 B.2 C.3 D.4
6、设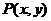 是曲线C:
是曲线C: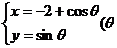 为参数,
为参数,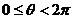 )上任意一点,则
)上任意一点,则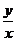 的取值范围是
( )
的取值范围是
( )
A.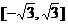 B.
B.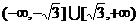
C.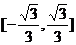 D.
D.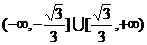
5、方程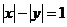 的图象是 ( )
的图象是 ( )
4、下列说法正确的是 ( )
A.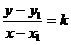 是过点
是过点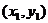 且斜率为
且斜率为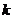 的直线.
的直线.
B.在x轴和y轴上的截距分别是a、b的直线方程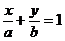 .
.
C.直线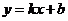 与y轴的交点到原点的距离是b.
与y轴的交点到原点的距离是b.
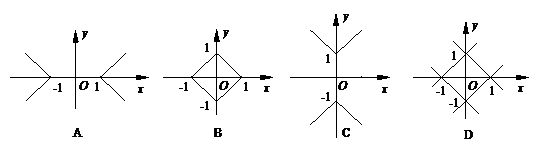 D.不与坐标轴平行或重合的直线方程一定可以写成两点式或斜截式.
D.不与坐标轴平行或重合的直线方程一定可以写成两点式或斜截式.
3、圆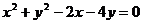 与圆
与圆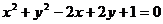 的位置关系是 ( )
的位置关系是 ( )
A.相离 B.相外切 C.相交 D.相内切
2、当 时,直线
时,直线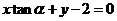 的倾斜角是
( )A.
的倾斜角是
( )A.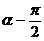 B.
B.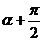 C.
C.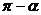 D.
D.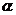
1、直线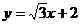 到直线
到直线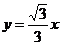 的角是
( )
的角是
( )
A.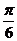 B.
B.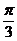 C.
C.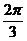 D.
D.
23.(8分) 在一个容积固定的反应器中,有一可左右滑动的密封隔板,两侧进行如图所示的反应(均加有适量的新型固体催化剂,其体积可忽略不计)
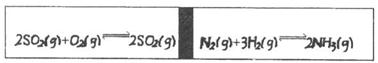 (1)若开始时左侧投入2molSO2、1molO2,右侧投入1molN2、4molH2,达到平衡后(两侧温度相同),隔板是否可能处于中央
(填“可能或不可能”)
(2)起始时投入2molSO2、1molO2;1molN2、2molH2,达到平衡后,隔板仍处于中央,则SO2的转化率和N2的转化率之比为 (填数字)
(1)若开始时左侧投入2molSO2、1molO2,右侧投入1molN2、4molH2,达到平衡后(两侧温度相同),隔板是否可能处于中央
(填“可能或不可能”)
(2)起始时投入2molSO2、1molO2;1molN2、2molH2,达到平衡后,隔板仍处于中央,则SO2的转化率和N2的转化率之比为 (填数字)
(3)若起始时投入2molSO2、1molO2,欲用简单方法粗略测定平衡时SO2的转化率,则可将左侧的平衡混合气体中通入足量的 (填序号) A.氢氧化钠溶液 B.氯化钡溶液
C.98.3%的浓硫酸 D.硝酸钡混合溶液
(4)若起始时投入2molSO2、1molO2;1molN2、amolH2、0.1molNH3,起始时右侧体积小于左侧体积,当a值在一定范围内变化时,均可通过调节反应器温度,使左右两侧反应都达到平衡,且平衡时隔板处于中央,此时SO2的转化率与N2的转化率之比为5:1,求a的取值范围
2009年重庆一中高2011级月考
22.(15分) CH3OH(g)+H2O(g) CO2(g)+3H2(g);该反应的正反应为吸热反应,请根据题目要求回答下列问题:
CO2(g)+3H2(g);该反应的正反应为吸热反应,请根据题目要求回答下列问题:
(1)在其它条件不变的情况下降低温度,则逆反应速率 (填“增大”或“减小”或“不变”,下同);在其它条件不变的情况下加压,则正反应速率 。 (2)一定条件下,向体积为2L的密闭容器中充入1molCH3OH(g)和3molH2O(g),20s后,测得混合气体的压强是反应前的1.2倍,则用甲醇表示该反应的速率为 。
(3)判断该可逆反应达到平衡状态的依据是(填序号) 。 A v正(CH3OH)=v正(CO2) B 混合气体的密度不变 C 混合气体的平均相对分子质量不变 D CH3OH、H2O、CO2、H2的浓度都不再发生变化 (4)在一定条件下,当该反应处于化学平衡状态时,下列操作可使化学平衡向逆反应方向移动的是 (填序号)。 A.升高温度 B.降低温度 C.增大压强 D.减小压强 E.加入催化剂 F.移出水蒸气
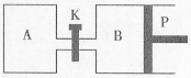 (5)右图中P是可自由平行滑动的活塞,关闭K,在相同温度时,向A容器中充入1molCH3OH(g)和2molH2O(g),向B容器中充入1.2molCH3OH(g) 和2.4molH2O(g),两容器分别发生上述反应。
已知起始时容器A和B的体积均为aL。试回答:
①反应达到平衡时容器B的体积为1.5aL,容器B中CH3OH转化率为 ,
(5)右图中P是可自由平行滑动的活塞,关闭K,在相同温度时,向A容器中充入1molCH3OH(g)和2molH2O(g),向B容器中充入1.2molCH3OH(g) 和2.4molH2O(g),两容器分别发生上述反应。
已知起始时容器A和B的体积均为aL。试回答:
①反应达到平衡时容器B的体积为1.5aL,容器B中CH3OH转化率为 ,
A、B两容器中H2O(g)的体积百分含量的大小关系为:B(填“>”、“<”、“=”) A。 ②若打开K,一段时间后重新达到平衡,容器B的体积为 L(连通管中气体体积忽略不计,且不考虑温度的影响)。
21.(14分)(1)合成氨工业对化学工业和
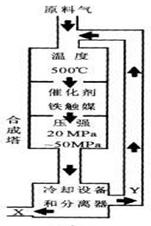 国防工业具有重要意义。工业合成氨生产示
国防工业具有重要意义。工业合成氨生产示
意图如右图所示。 ① X的化学式为 ;
② 图中条件选定的主要原因是
(选填字母序号) ;
A.温度和压强对化学平衡影响
B.铁触媒在该温度时活性大
C.工业生产受动力、材料、设备等条件的限制
③ 改变反应条件,会使平衡发生移动。右图中
表示随条件改变,氨气的百分含量的变化趋势。
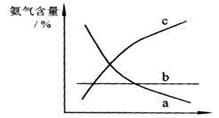 当横坐标为压强时,变化趋势正确的是(选填字母代号)
,当横坐标为温度时,
当横坐标为压强时,变化趋势正确的是(选填字母代号)
,当横坐标为温度时,
变化趋势正确的是(选填字母序号) 。 (2)常温下氨气极易溶于水,其水溶液可以导电。用方程式表示氨气溶于水的过程中存在的可逆过程 ; (3)氨气具有还原性,在铜的催化作用下,氨气和氟气反应生成A和B两种物质。A为铵盐,B在标准状况下为气态。在此反应中,若每反应1体积氨气,同时反应0.75体积氟气;若每反应8.96L氨气(标准状况),同时生成0.3molA。 ①写出氨气和氟气反应的化学方程式 ; ②在标准状况下,每生成1 mol B,转移电子的物质的量为 mol。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com