
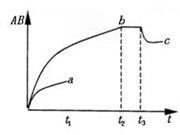
18. 反应A2 + B2  2AB;在不同温度和压强改变的条件
2AB;在不同温度和压强改变的条件
下,产物AB和AB%的生成情况如图,a为500℃时的情况;b为300℃时的情况,c为反应在300℃时从时间t3开始向容器
中加压的情况,则下列叙述正确的是 A.A2、B2及AB均为气体,正反应放热; B. AB为气体,A2、B2中有一种为非气体,正反应吸热
C.AB为气体,A2、B2中至少有一种为非气体,正反应放热
D.AB为固体,A2、B2中有一种为非气体,正反应吸热
第Ⅱ卷(共56分)
17. 现有下列三个图像:
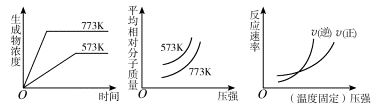 下列反应中全部符合上述图像的反应是
A.N2(g) + 3H2(g)
下列反应中全部符合上述图像的反应是
A.N2(g) + 3H2(g)  2NH3(g);(正反应放热)
B.2SO3(g)
2NH3(g);(正反应放热)
B.2SO3(g)  2SO2(g) + O2(g);(正反应吸热)
C.4NH3(g) + 5O2(g)
2SO2(g) + O2(g);(正反应吸热)
C.4NH3(g) + 5O2(g)  4NO(g) + 6H2O(g);(正反应放热)
D.H2(g) + CO(g)
4NO(g) + 6H2O(g);(正反应放热)
D.H2(g) + CO(g)  C(s) + H2O(g);(正反应吸热)
C(s) + H2O(g);(正反应吸热)
16.T℃时,将气体X与气体Y置于一密闭容器中,反应生成气体Z,反应过程中各物质的浓度变 化如图(I)所示。保持其他条件不变,在T1、T2两种温度下,Y的体积分数变化如图(Ⅱ)所示。
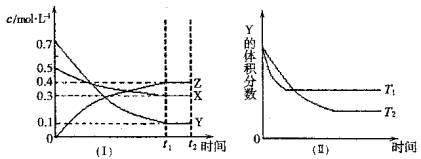
下列结论正确的是 A.t2时,保持其它条件和物质状态不变,增加压强,化学平衡向逆反应方向移动 B.T℃时,若各物质起始浓度为:0.4 mol/L X、0.4 mol/L Y、0.2 mol/L Z。保持其他条件不变,达到平衡时Z的浓度为0.4 mol/L C.图(Ⅱ)中T1>T2,则正反应是吸热反应 D.其他条件不变,升高温度,正、逆反应速率均增大,且X的转化率增大
15.某温度下,在容积固定的密闭容器中发生可逆反应:A(g)+2 B(g) 2 R(g) (正反应放热) 。平衡时,容器中各物质的浓度比为c(A)∶c(B)∶c(R)=1∶1∶6。若往容器中再充入0.1 mol A、0.1 mol B、0.6 mol R。下列叙述正确的是:
A.充入时,反应速率v正增大,v逆减小
B.达到新的平衡时,容器内温度下降
C.达到新的平衡时,反应混合物中A、B的体积分数增加
D.达到新的平衡时,c(B)∶c(R)<1∶6
2 R(g) (正反应放热) 。平衡时,容器中各物质的浓度比为c(A)∶c(B)∶c(R)=1∶1∶6。若往容器中再充入0.1 mol A、0.1 mol B、0.6 mol R。下列叙述正确的是:
A.充入时,反应速率v正增大,v逆减小
B.达到新的平衡时,容器内温度下降
C.达到新的平衡时,反应混合物中A、B的体积分数增加
D.达到新的平衡时,c(B)∶c(R)<1∶6
14.下列关于纯净物、混合物、强电解质、弱电解质和非电解质的正确组合是
|
|
纯净物 |
混合物 |
强电解质 |
弱电解质 |
非电解质 |
|
A |
盐酸 |
醋酸 |
碳酸 |
氨水 |
氯气 |
|
B |
纯碱 |
碘酒 |
苛性钾 |
CH3COOH |
干冰 |
|
C |
石灰石 |
空气 |
硫酸 |
磷酸 |
水 |
|
D |
烧碱 |
天然气 |
氯化钠 |
硝酸钠 |
蔗糖 |
13.实验室将I2溶于KI溶液中,配制浓度较大的碘水,主要是因为发生了反应: I2(aq)+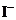 (aq)
(aq)
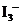 (aq)上述平衡体系中,
(aq)上述平衡体系中,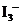 的物质的量浓度c(
的物质的量浓度c(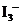 )与温度T的关系如右图所示(曲线上的任何一点都表示平衡状态),下列说法不正确的是
A.该反应的正反应是吸热反应
B.A点与C点的化学反应速率VA < VC
C.在反应进行到D点时, V正 > V逆
D.A点与B点相比,B点的c(I2)大
)与温度T的关系如右图所示(曲线上的任何一点都表示平衡状态),下列说法不正确的是
A.该反应的正反应是吸热反应
B.A点与C点的化学反应速率VA < VC
C.在反应进行到D点时, V正 > V逆
D.A点与B点相比,B点的c(I2)大
12.下列说法错误的是
A.对于反应C(s) + CO2
(g)  2CO(g) (正反应吸热),升高温度会加快化学反应速率
B.合成氨反应中,当3v(NH3)正=2v(H2)逆时,反应达到平衡
C.对于反应PCl5(g)
2CO(g) (正反应吸热),升高温度会加快化学反应速率
B.合成氨反应中,当3v(NH3)正=2v(H2)逆时,反应达到平衡
C.对于反应PCl5(g)  PCl3(g) + Cl2(g),达到平衡后,若保持温度容积不变,又加入一定量的PCl5,则该平衡向正方向移动,但平衡时PCl5的转化率减小
D.将nmol H2(g)、n mol I2(g)和2n mol H2 (g)、2n mol I2(g)分别充入两个等温等容的容
PCl3(g) + Cl2(g),达到平衡后,若保持温度容积不变,又加入一定量的PCl5,则该平衡向正方向移动,但平衡时PCl5的转化率减小
D.将nmol H2(g)、n mol I2(g)和2n mol H2 (g)、2n mol I2(g)分别充入两个等温等容的容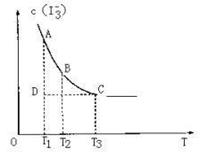 器中,平衡时H2的转化率前者小于后者
器中,平衡时H2的转化率前者小于后者
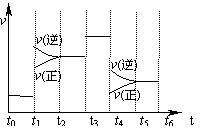
11.N2(g) + 3H2(g)  2NH3 (g) (正反应放热) ,在某一时间段中反应速率与反应过程的曲线关系如右图。下列说法正确的是
2NH3 (g) (正反应放热) ,在某一时间段中反应速率与反应过程的曲线关系如右图。下列说法正确的是
A.氨气的体积分数最高的一段时间为t5 - t6 B.t2-t3和t3-t4时间段氨气的体积分数相等 C.t1时刻改变的条件是降低温度 D.t4-t5时间段平衡向正反应方向移动
10. 在0.1mol·L-1 CH3COOH溶液中存在如下电离平衡:CH3COOH
在0.1mol·L-1 CH3COOH溶液中存在如下电离平衡:CH3COOH  CH3COO-+H+ 对于该平衡,下列叙述正确的是
A. 加入水时,平衡向逆反应方向移动
B . 加入少量NaOH固体,平衡向正反应方向移动
C . 加入少量0.1mol·L-1 HCl溶液,溶液中c(H+)减小
D . 加入小量CH3COONa固体,平衡向正反应方向移动
CH3COO-+H+ 对于该平衡,下列叙述正确的是
A. 加入水时,平衡向逆反应方向移动
B . 加入少量NaOH固体,平衡向正反应方向移动
C . 加入少量0.1mol·L-1 HCl溶液,溶液中c(H+)减小
D . 加入小量CH3COONa固体,平衡向正反应方向移动
9.下列化学反应中,为使平衡体系析出更多的银,可采取的措施是
Ag++ Fe2+  Ag(固体)+ Fe3+(正反应放热)
A . 常温下加压 B . 增加Fe3+的浓度
C . 增加Fe2+的浓度 D. 移去一些析出的银
Ag(固体)+ Fe3+(正反应放热)
A . 常温下加压 B . 增加Fe3+的浓度
C . 增加Fe2+的浓度 D. 移去一些析出的银
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com