
6.李鸿章在给友人的信中说:“中国积弱,由于患贫。西洋方圆千里,数百里之国,岁入财赋动以万计,无非取资于煤铁五金之矿、铁路、电报信局、丁口等税。”这表明李鸿章
A.认识到中国贫穷的根源 B.主张抵制列强的经济侵略
C.主张变革社会经济体制 D.认识到“求富”的重要性
5.林则徐被誉为近代中国“开眼看世界”的第一人,主要是因为他
A.领导禁烟运动,维护民族利益
B.最早主张在中国发展资本主义
C.提倡“经世致用”,引导人们摆脱理学束缚
D.积极搜集西方资料,仿制西方战船
4.《辛丑条约》签订后,中国半殖民地半封建社会统治秩序完全确立,主要是指
A.清政府彻底成为列强侵略工具 B.列强直接控制了中国的内政外交
C.中国封建自然经济完全解体 D.中国完全卷入资本主义世界市场
3.中日签订《马关条约》所引发的历史现象有
①列强加紧对华资本输出 ②维新思潮转变为政治运动
③革命派和保皇派的论战 ④列强争夺中国的斗争加剧
A.①②③ B.①②④ C.②③④ D.①③④
2.“应如何定立交界,由两国派出信任大员秉公查勘。……在塔尔巴哈台会齐商办,……将所指各交界作记绘图……仍会同具文,画押用印,当为补续此约之条。”根据此条款约定,中俄签订了
A.《瑷珲条约》 B.《北京条约》
C.《勘分西北界约记》 D.《伊犁条约》
1.在下列不平等条约中,涉及列强在华传教权的有
①《望厦条约》 ②《黄埔条约》 ③《天津条约》 ④《北京条约》
A.①②③ B.①②④ C.②③④ D.①③④
23.(8分) 在一个容积固定的反应器中,有一可左右滑动的密封隔板,两侧进行如图所示的反应(均加有适量的新型固体催化剂,其体积可忽略不计)
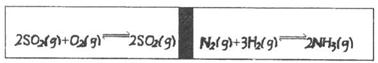 (1)若开始时左侧投入2molSO2、1molO2,右侧投入1molN2、4molH2,达到平衡后(两侧温度相同),隔板是否可能处于中央
(填“可能或不可能”)
(2)起始时投入2molSO2、1molO2;1molN2、2molH2,达到平衡后,隔板仍处于中央,则SO2的转化率和N2的转化率之比为 (填数字)
(1)若开始时左侧投入2molSO2、1molO2,右侧投入1molN2、4molH2,达到平衡后(两侧温度相同),隔板是否可能处于中央
(填“可能或不可能”)
(2)起始时投入2molSO2、1molO2;1molN2、2molH2,达到平衡后,隔板仍处于中央,则SO2的转化率和N2的转化率之比为 (填数字)
(3)若起始时投入2molSO2、1molO2,欲用简单方法粗略测定平衡时SO2的转化率,则可将左侧的平衡混合气体中通入足量的 (填序号) A.氢氧化钠溶液 B.氯化钡溶液
C.98.3%的浓硫酸 D.硝酸钡混合溶液
(4)若起始时投入2molSO2、1molO2;1molN2、amolH2、0.1molNH3,起始时右侧体积小于左侧体积,当a值在一定范围内变化时,均可通过调节反应器温度,使左右两侧反应都达到平衡,且平衡时隔板处于中央,此时SO2的转化率与N2的转化率之比为5:1,求a的取值范围
2009年重庆一中高2011级月考
22.(15分) CH3OH(g)+H2O(g) CO2(g)+3H2(g);该反应的正反应为吸热反应,请根据题目要求回答下列问题:
CO2(g)+3H2(g);该反应的正反应为吸热反应,请根据题目要求回答下列问题:
(1)在其它条件不变的情况下降低温度,则逆反应速率 (填“增大”或“减小”或“不变”,下同);在其它条件不变的情况下加压,则正反应速率 。 (2)一定条件下,向体积为2L的密闭容器中充入1molCH3OH(g)和3molH2O(g),20s后,测得混合气体的压强是反应前的1.2倍,则用甲醇表示该反应的速率为 。
(3)判断该可逆反应达到平衡状态的依据是(填序号) 。 A v正(CH3OH)=v正(CO2) B 混合气体的密度不变 C 混合气体的平均相对分子质量不变 D CH3OH、H2O、CO2、H2的浓度都不再发生变化 (4)在一定条件下,当该反应处于化学平衡状态时,下列操作可使化学平衡向逆反应方向移动的是 (填序号)。 A.升高温度 B.降低温度 C.增大压强 D.减小压强 E.加入催化剂 F.移出水蒸气
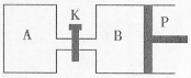 (5)右图中P是可自由平行滑动的活塞,关闭K,在相同温度时,向A容器中充入1molCH3OH(g)和2molH2O(g),向B容器中充入1.2molCH3OH(g) 和2.4molH2O(g),两容器分别发生上述反应。
已知起始时容器A和B的体积均为aL。试回答:
①反应达到平衡时容器B的体积为1.5aL,容器B中CH3OH转化率为 ,
(5)右图中P是可自由平行滑动的活塞,关闭K,在相同温度时,向A容器中充入1molCH3OH(g)和2molH2O(g),向B容器中充入1.2molCH3OH(g) 和2.4molH2O(g),两容器分别发生上述反应。
已知起始时容器A和B的体积均为aL。试回答:
①反应达到平衡时容器B的体积为1.5aL,容器B中CH3OH转化率为 ,
A、B两容器中H2O(g)的体积百分含量的大小关系为:B(填“>”、“<”、“=”) A。 ②若打开K,一段时间后重新达到平衡,容器B的体积为 L(连通管中气体体积忽略不计,且不考虑温度的影响)。
21.(14分)(1)合成氨工业对化学工业和
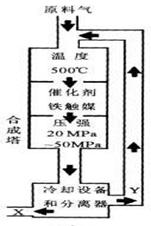 国防工业具有重要意义。工业合成氨生产示
国防工业具有重要意义。工业合成氨生产示
意图如右图所示。 ① X的化学式为 ;
② 图中条件选定的主要原因是
(选填字母序号) ;
A.温度和压强对化学平衡影响
B.铁触媒在该温度时活性大
C.工业生产受动力、材料、设备等条件的限制
③ 改变反应条件,会使平衡发生移动。右图中
表示随条件改变,氨气的百分含量的变化趋势。
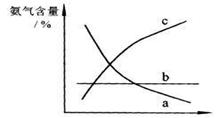 当横坐标为压强时,变化趋势正确的是(选填字母代号)
,当横坐标为温度时,
当横坐标为压强时,变化趋势正确的是(选填字母代号)
,当横坐标为温度时,
变化趋势正确的是(选填字母序号) 。 (2)常温下氨气极易溶于水,其水溶液可以导电。用方程式表示氨气溶于水的过程中存在的可逆过程 ; (3)氨气具有还原性,在铜的催化作用下,氨气和氟气反应生成A和B两种物质。A为铵盐,B在标准状况下为气态。在此反应中,若每反应1体积氨气,同时反应0.75体积氟气;若每反应8.96L氨气(标准状况),同时生成0.3molA。 ①写出氨气和氟气反应的化学方程式 ; ②在标准状况下,每生成1 mol B,转移电子的物质的量为 mol。
19. (9分) 在体积不变的密闭容器中进行如下反应:mA(g) + nB(g)
(9分) 在体积不变的密闭容器中进行如下反应:mA(g) + nB(g)  pC(g),反应经5分钟达到平衡,测得此时A的浓度减小了a mol/L,而C的浓度增加了2a/3 mol/L,又知平均反应速率:v (C) =2v (B)。
pC(g),反应经5分钟达到平衡,测得此时A的浓度减小了a mol/L,而C的浓度增加了2a/3 mol/L,又知平均反应速率:v (C) =2v (B)。
(1)m = _______,n = ________,p = ________。
(2)压强一定时,C的百分含量与温度、时间(T表示温度,
t表示时间)的关系如右图所示。由此可知,该反应为___________
(填“吸热”或“放热”)反应。
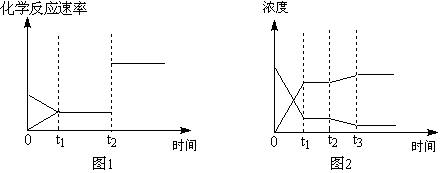
(3)以上图1、图2均表示该反应在t1时达到平衡,在t2时改变某条件发生变化的曲线。
试判断,图1中t2时改变的条件是______________________________;图2中t2时改变的条件是______________________________。 20. (10分) 在一固定容积的密闭容器中,保持一定温度,在一定条件下进行以下反应:A(g)+2B(g)
20. (10分) 在一固定容积的密闭容器中,保持一定温度,在一定条件下进行以下反应:A(g)+2B(g)  3C(g),已知加入1molA和3molB且达到平衡后,生成了a molC。
(1)达到平衡时,C在反应混合气中的体积分数是 (用含字母a的代数式表示)。
3C(g),已知加入1molA和3molB且达到平衡后,生成了a molC。
(1)达到平衡时,C在反应混合气中的体积分数是 (用含字母a的代数式表示)。
(2)若继续向原混合物的容器中通入少量氦气后(设氦气和A、B、C都不反应),化学平衡(填字母) ;
A、向正反应方向移动 B、向逆反应方向移动 C、平衡不移动 (3)在相同实验条件下,若在同一容器中改为加入2molA和6 mol B,达到平衡后,C的物质的量为 mol(用含字母a的代数式表示)。此时C在反应混合气中的体积分数与原平衡相比 (选填“增大”“减小”或“不变”)。 (4)在相同实验条件下,若在同一容器中改为加入2 mol A和8 mol B,若要求平衡后C在反应混合气中体积分数仍与原平衡相同,则还应加入C mol。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com