
17、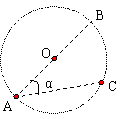 平面内有匀强电场,场强方向与圆面平行。带正电的微粒(不计重力)从A点出发,以相同的初动能在圆内向各个方向运动,当微粒从C点离开圆面时动能最大。图中AB是圆的直径,α=30°,则平面内的电场线方向为( )
平面内有匀强电场,场强方向与圆面平行。带正电的微粒(不计重力)从A点出发,以相同的初动能在圆内向各个方向运动,当微粒从C点离开圆面时动能最大。图中AB是圆的直径,α=30°,则平面内的电场线方向为( )
A.沿A→B方向 B.沿A→C方向
C.沿O→C方向 D.沿B→C方向
16、在均匀介质中选取平衡位置在同一直线上的9个质点,相邻两质点的距离均为L,如图(a)所示.一列横波沿该直线向右传播,t=0时到达质点1,质点1开始向下运动,经过时间Δt第一次出现如图(b)所示的波形.则该波的( ) 
(A)周期为Δt,波长为8L.
(B)周期为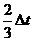 ,波长为8L.
,波长为8L.
(C)周期为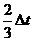 ,波速为
,波速为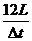 (D)周期为Δt,波速为
(D)周期为Δt,波速为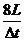



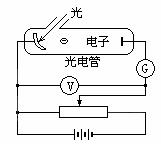
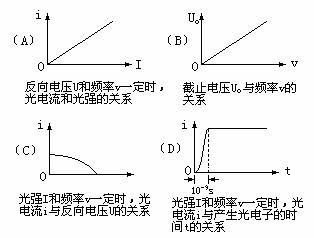
15、研究光电效应规律的实验装置如图所示,以频率为 v的光照射光电管阴极 K时,有光电子产生。由于光电管 K、A间加的是反向电压,光电子从阴极 K发射后将向阳极 A作减速运动。光电流 I由图中电流计 G测出,反向电压 U由电压表测出,当电流计示数恰好为零时,电压表的示数称为反向截止电压 U0。在下列表示光电效应实验规律的图象中,错误的是( )
14、分别以p、V、T表示气体的压强、体积、温度。一定质量的理想气体,其初始状态表示为(p0、V0、T0)。若分别经历如下两种变化过程:

①从(p0、V0、T0)变为(p1、V1、T1)的过程中,温度保持不变(T1=T0);
②从(p0、V0、T0)变为(p2、V2、T2)的过程中,既不吸热,也不放热
在上述两种变化过程中,如果V1=V2>V0,则 (
)
(
)


13.向饱和Na2CO3溶液中通入足量CO2,下列说法不正确的是( )
A.溶液中有Na2CO3•10H2O晶体析出 B.溶液的pH减小
C.溶液中发生的离子反应为:CO2+H2O+CO32- =2HCO3-
D.溶液中Na+的物质的量减小
12.肼(N2H4)是一种常用的火箭燃料,对应的氧化剂通常用过氧化氢,如果火箭推进器中盛有液态的肼和液态过氧化氢,当它们混合反应时立即产生大量的氮气和水蒸气,同时放出大量的热。已知0.4 mol液态肼与足量液态过氧化氢发生反应,可放出256.6 kJ的热量,下列热化学方程式正确的是
A.N2H4(l) + 2H2O2(l) = N2(g) + 4H2O(l) △H=-256.6kJ/mol
B.N2H4(l) + 2H2O2(l) = N2(g) + 4H2O(g) △H=-641.5kJ/mol
C.N2H4(l) + 2H2O2(g) = N2(g) + 4H2O(g) △H=-641.5kJ/mol
D.N2H4(l) + 2H2O2(l) = N2(g) + 4H2O(g) △H= + 641.5kJ/mol
11.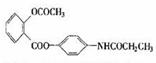 某种解热镇痛药的结构简式为
某种解热镇痛药的结构简式为
当它完全水解时,可得到的产物有
A.2种 B.3种 C.4种 D.5种
10.在100 mL 0.10 mol·L-1的AgNO3溶液中加入100 mL溶有2.08 g BaCl2的溶液,再加入100 mL溶有0.010 mol CuSO4·5H2O的溶液,充分反应。下列说法中正确的是
A.最终得到白色沉淀和无色溶液
B.最终得到的白色沉淀是等物质的量的两种化合物的混合物
C.在最终的溶液中n(Cl-)=0.02 mol D.在最终的溶液中c(Cu2+)=0.01 mol·L-1
9.下列离子方程式书写正确的是( )
A.澄清石灰水与少量小苏打溶液混合:
Ca2+ + 2OH- + 2 HCO3- = CaCO3↓+ CO32- + 2H2O
B.氯化铝溶液中加入过量的氨水:Al3+ + 4NH3·H2O = AlO2-↓+ 4NH4++2H2O
C.向NH4HSO4稀溶液中逐滴加入Ba(OH)2稀溶液至刚好沉淀完全:
Ba2+ + 2OH- + NH4+ + H+ + SO42- = BaSO4↓+ NH3·H2O + H2O
D.漂白粉溶液中通入少量SO2气体:Ca2+ + 2ClO- + SO2 + H2O = CaSO3↓+2HclO
8.已知S2O8n-具有强氧化性, S2O8n-离子在一定条件下可把Mn2+氧化成MnO4-离子,若反应后S2O8n-离子变成SO42-离子; 又知反应中氧化剂与还原剂的离子数之比为5:2则S2O8n-中的n值和S元素的化合价是 ( )
A.2, +6 B.2, +7 C.4 ,+7 D.4 , +4
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com