
学习内能的知识后,大多数学生对这三个物理量(温度、 内能、热量)的概念及相互关系不能正确理解,为帮助学生理解和应用,把三者的区别和联系总结如下:
1. 温度表示物体的冷热程度,从分子运动理论的观点来看,温度是分子热运动激烈程度的标志,对同一物体而言,温度只能说“是多少”或“达到多少”,不能说“有”“没有”或“含有”等。
温度、内能和热量是热学中三个重要的物理量。在中考中经常以概念的理解与应用,去考查这部分内容,一般常见于选择与填空题。
14.(14分)在2008年初我国南方遭遇的冰雪灾害中,使用了一种融雪剂,其主要成分的化学式为XY2,X、Y均为周期表前20号元素,其阳离子和阴离子的电子层结构相同,且1molXY2含有54mol电子。
⑴、该融雪剂的化学式是____________________;X与氢元素形成的化合物的电子是_______________。
⑵、元素D、E原子的最外层电子数是其电子层数的2倍,D与Y相邻,则D的离子结构示意图是__________;D与E能形成一种非极性分子,该分子的结构式为___________________;D所在族元素的氢化物中,沸点最低的是___________________。
⑶、元素W与Y同周期,其单质是原子晶体;元素Z的单质分子Z2中由3个共价键;W与Z能形成一种新型无机非金属材料,其化学式是___________________。
⑷、元素R与Y同主族,其氢化物能用于刻蚀玻璃,R2与NaOH溶液反应的产物之一是OR2,该反应的离子方程式为_______________________________________________。
13.(10分)无机过氧化合物的科学研究开始于18世纪初,人们相继制得了过氧化钡、过氧化钠、过氧化钾、过氧化氢等,目前无机过氧化合物逐渐成为无机化学的一个分支,其中过氧化氢是用途最广的过氧化物。试回答下列问题。
⑴Na2O2、K2O2、CaO2以及BaO2都可与酸作用生成过氧化氢,目前实验室制取过氧化氢可通过上述某种过氧化物与适量稀硫酸作用,过滤即可制得。最适合的过氧化物是 (写电子式)。
⑵过氧化氢是一种绿色氧化剂,写出在酸性条件下H2O2氧化氯化亚铁的离子反应方程式: 。
⑶与过氧化氢具有相同电子总数且属于非极性性分子的有 (写化学式)。
⑷纯的过氧化氢常用作火箭燃料的氧化剂,已知0.4mol液态肼(N2H4)与足量的液态过氧化氢反应,生成N2和H2O(g),放出256.6kJ的热量。则该反应的热化学方程式为
。
12.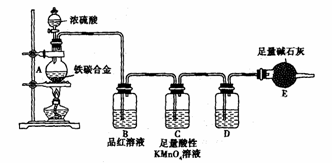 (18分)现有某铁碳合金,某化学兴趣小组为了测定铁碳合金中铁的质量分数,并探究浓硫酸的某些性质,设计了下图所示的实验装置和实验方案(夹持仪器已省略),请你参与此项活动并回答相应问题。(由实验装置引起的实验误差忽略不计)。
(18分)现有某铁碳合金,某化学兴趣小组为了测定铁碳合金中铁的质量分数,并探究浓硫酸的某些性质,设计了下图所示的实验装置和实验方案(夹持仪器已省略),请你参与此项活动并回答相应问题。(由实验装置引起的实验误差忽略不计)。
Ⅰ.探究浓硫酸的某些性质
(1)称量E的质量;按照图示连接装置,检查装置的气密性。简述检验发生装置气密性的方法______________________________________
___________________________________________________________________。
(2)将m g铁碳合金样品放入A中,再加入适量的浓硫酸。仪器A的名称为______。未点燃酒精灯前,A、B均无明显现象,其原因是:________________________
____________________________________________________________________。
(3)点燃酒精灯一段时间后,A、B中可观察到明显的现象。
写出A中碳发生反应的化学方程式______________________________________。
B中的现象是 。
(4)随着反应的进行,A中还可能发生某些离子反应。写出相应的离子方程式 (只写一个)_________________________________________________________。
(5)反应一段时间后,从A中逸出气体的速率仍然较快,除因温度较高,反应放热外,还可能的原因是_________________________________________________。
Ⅱ.测定铁的质量分数
 (6)待A中不再逸出气体时,停止加热,拆下E并称重。E增重b g。铁碳合金中铁的质量分数为________________________________________(写表达式),
(6)待A中不再逸出气体时,停止加热,拆下E并称重。E增重b g。铁碳合金中铁的质量分数为________________________________________(写表达式),
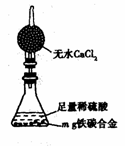
(7)某同学认为上述方法较复杂,使用右图所示的装置和其他常用实验仪器测定某些数据即可。为了快速准确的计算出铁的质量分数,最简便的实验操作是 (填写序号)。
A.用排水法测定H2的体积
B.反应结束后,过滤、洗涤、干燥、称量残渣的质量
C.测定反应前后装置和药品的总质量
11.(18分)浓H2SO4和木炭在加热时发生反应的化学方程式是:
2H2SO4(浓)+C  CO2↑+2H2O+2SO2↑
CO2↑+2H2O+2SO2↑
请从下图中选用所需的仪器(可重复选用)组成一套进行该反应并要检出反应产物的装置。现提供浓H2SO4、木炭和酸性KMnO4溶液,其他固、液试剂自选。(连接和固定仪器所用的玻璃管、胶管、铁夹、铁架台及加热装置等均略去)

将所选的仪器连接顺序由上至下依次填入下表,并写出该仪器中应加试剂的名称及其作用。
|
选用的仪器 (填字母) |
加入的试剂 |
作用 |
|
|
   |
   |
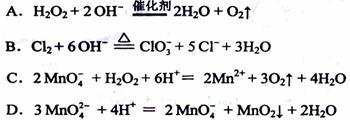
10.下列离子方程式正确的是:
9. 第7周期为不完全周期,若将来这一周期元素全部填满,则下列有关第7周期元素的推论可能正确的是( )
A. 第7周期排满时有32种元素
B. 第7周期排满时最后一种元素的原子序数是118,其单质不与任何物质发生化学反应
C. 第7周期第VIIA族元素的原子序数为117,是一种非金属元素
D. 第7周期第IIIA族元素的氢氧化物与氢氧化铝具有相似的化学性质
8.常温下单质硫主要以S8形式存在。加热时,S8会转化为S6、S4、S2等。当温度达到750℃时,硫蒸汽主要以S2形式存在(占92%)。下列说法正确的是( )
A.S8转化为S6、S4、S2属于物理变化 B.不论哪种硫分子,完全燃烧都生成SO2
C.常温条件下单质硫为原子晶体 D.把硫单质在空气中加热到750℃即得S2
7.质量分数不等的两种硫酸溶液等质量混合时,所得硫酸溶液的质量分数为a%,而等体积混合后所得硫酸溶液的质量分数为b%;质量分数不等的两种酒精溶液等质量混合时,所得酒精溶液的质量分数为a%,而等体积混合后所得酒精溶液的质量分数为c%。则a、b、c的大小关系正确的是 ( )
A.a > b > c B.b > a > c C.c > a > b D.c > b > a
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com