
7. 过直线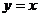 上一点
上一点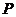 作圆
作圆 :
: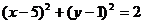 的两条切线
的两条切线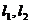 ,切点分别为
,切点分别为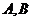 ,
,
则四边形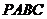 面积的最小值为 ( ▲ )
面积的最小值为 ( ▲ )
A.2 B.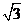 C.
C.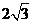 D.4
D.4
6.若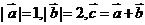 ,且
,且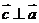 ,则向量
,则向量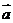 与
与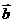 的夹角为
( ▲ )
的夹角为
( ▲ )
A.30° B.60° C.120° D.150°
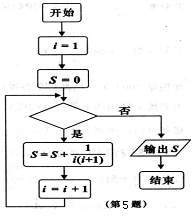
5.一个算法的程序框图如图所示,若该程序输出的结果为 ,
,
则判断框中应填入的条件是 ( ▲ )
A.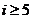 B.
B.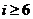 C.
C.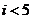 D.
D.
4.已知直线 及两个平面
及两个平面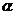 、
、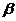 ,下列命题正确的是 ( ▲
)
,下列命题正确的是 ( ▲
)
A.若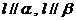 ,则
,则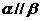 B.若
B.若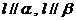 ,则
,则
C.若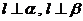 , 则
, 则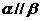 D.若
D.若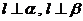 ,则
,则
3.“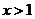 ”是“
”是“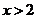 ”的
( ▲
)
”的
( ▲
)
 A.充分而不必要条件 B.必要而不充分条件
A.充分而不必要条件 B.必要而不充分条件
C.充分必要条件 D.既不充分也不必要条件
2.在复平面内,复数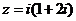 对应的点位于
(
▲ )
对应的点位于
(
▲ )
A.第一象限 B.第二象限 C.第三象限 D.第四象限
1.已知全集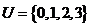 ,集合
,集合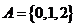 ,
,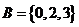 ,则
,则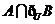 等于( ▲
)
等于( ▲
)
A.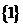 B.
B.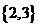 C.
C.  D.
D. 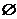
26.(新课标高考题)(08山东卷)氮是地球上极为丰富的元素。
(1)Li3N晶体中氮以N3-存在,基态N3-的电子排布式为 。
(2)N≡N的键能为942 kJ·mol-1,N-N单键的键能为247 kJ·mol-3,计算说明N2中的
键比
键稳定(填“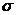 ”“
”“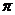 ”)。
”)。
(3)(CH3)3NH+和AlCl-4可形成离子液体。离子液体由阴、阳离子组成,熔点低于100℃,其挥发性一般比有机溶剂 (填“大”或“小”),可用作 (填代号)。
 a、助燃剂
b、“绿色”溶剂
a、助燃剂
b、“绿色”溶剂
c、复合材料 d、绝热材料
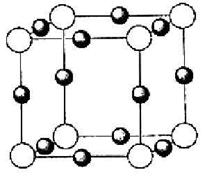
(4)X*中所有电子正好充满K、L、M三个电子层,它与N3-形成
的晶体结构如图所示。X的元素符号是 ,与同一个
N3-相连的X*有 个。
25.(新课标高考题)(08上海卷)(A)四种短周期元素的性质或结构信息如下表,请根据信息回答下列问题:

(1)B元素在周期表中的位置是_________________________,写出A原子的电子排布式__________________。
(2)写出C单质与水反应的化学方程式____________________________________________。A与C形成的化合物溶于水后,溶液的pH__________7(填“大于”、“等于”或“小于”)。
(3)D元素最高价氧化物晶体的硬度________(填“大”、“小”),其理由是____________________________。
(4)A、B两元素非金属性较强的是(写元素符号)__________。写出能证明这一结论的一个实验事实_____________________________________________________。
24.(07天津卷)U、V、W、X、Y、Z是原子序数依次增大的六种常见元素。Y的单质在W2中燃烧的产物可使品红溶液褪色。Z和W元素形成的化合物Z3W4具有磁性。U的单质在W2中燃烧可生成UW和UW2两种气体。X的单质是一种金属,该金属在UW2中剧烈燃烧生成黑、白两种固体。
请回答下列问题:
(1)V的单质分子的结构式为______________;XW的电子式为__________________;Z元素在周期表中的位置是_________。
(2)U元素形成的同素异形体的晶体类型可能是(填序号)________________。
①原子晶体 ②离子晶体 ③分子晶体 ④金属晶体
(3)U、V、W形成的10电子氢化物中,U、V的氢化物沸点较低的是(写化学式)__________;V、W的氢化物分子结合H+能力较强的是(写化学式)__________,用一个离子方程式加以证明___________________________________。
(4)YW2气体通入BaCl2和HNO3的混合溶液,生成白色沉淀和无色气体VW,有关反应的离子方程式为__________________。
由此可知VW和YW2还原性较强的是(写化学式)____________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com