
例8.含n g硝酸的稀溶液恰好和m g铁粉充分反应,铁与硝酸均无剩余,若硝酸还原产物只有NO,n∶m不可能是 ( )
A. 2∶1 B. 4∶
[解析]:将金属每失去1mol电子所需金属的质量称为摩尔电子质量。由题意,生成0.5molH2,金属失去的电子即为1mol,即合金的平均摩尔电子质量为
八、极端假设法
例7.由两种金属组成的合金10g投入足量的稀硫酸中,反应完全后得到氢气11.2L(标准状况下),此合金可能是 ( )
A.镁铝合金 B.镁铁合金 C.铝铁合金 D.镁锌合金
Fe ~ H2↑ ,FeS ~ H2S↑;即气体的物质的量等于铁的物质的量。n(Fe)= =0.75mol,v(↑)= 0.75mol×
=0.75mol,v(↑)= 0.75mol×
七、摩尔电子质量法
[解析]:在铁与硫的反应后,无论何种物过量,与最终的气体量无关。因为:
例6. 16g硫粉和42 g铁粉,混合并在隔绝空气情况下加热,当完全反应后,再加入过量的盐酸,生成的气体在标准状况下的体积为 ( )
而铁最终全部转化为FeCl3,n(Cl)=0.56L ÷22.4L/mol×2+0.7mol=0.75mol,n(Fe)= ,m(Fe)=0.25mol×56g•mol?1=14 g,则
,m(Fe)=0.25mol×56g•mol?1=14 g,则 ,故选B。
,故选B。
六、关系式法
[解析]:铁的氧化物中含Fe和O两种元素,由题意,反应后,HCl中的H全在水中,O元素全部转化为水中的O,由关系式:2HCl~ H2O ~O,得:n(O)=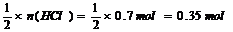 ,m(O)=0.35mol×
,m(O)=0.35mol×
A.72.4% B.71.4% C.79.0% D.63.6%
例5.将几种铁的氧化物的混合物加入100mL、7mol•L?1的盐酸中。氧化物恰好完全溶解,在所得的溶液中通入0.56L(标况)氯气时,恰好使溶液中的Fe2+完全转化为Fe3+,则该混合物中铁元素的质量分数为 ( )
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com