
33.[物理选修3-4模块]
(1)如图所示,质点O在垂直x轴方向上做简谐振动,形成了沿x轴传播的横波。在t=0时刻质点O开始向上运动,经0.2s第一次形成图示波形,由此判断在t=2.5s时刻,质点A、B的运动情况是( )
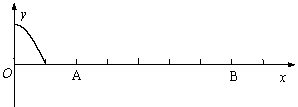 A.A点位于x轴的下方。
A.A点位于x轴的下方。
B.B点位于x轴的上方。
C.A点正往上运动。
D.B点正往上运动。
(2).如图所示,透明介质球的半径为R,光线DC平行直径AB射到介质球的C点,DC与AB的距离H=0.8R。
(1)试证明:DC光线进入介质球后,第一次到达介质球的界面时,在界面上不会发生全反射.(要求作图说明理由)
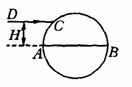 (2)若DC光进入介质球后,第二次到达介质球的界而时,从球内折射出的光线与入射光线平行,求介质的折射率.
(2)若DC光进入介质球后,第二次到达介质球的界而时,从球内折射出的光线与入射光线平行,求介质的折射率.
32.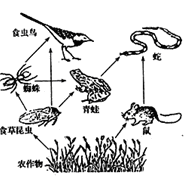 (4分)我国是一个农业大国,在农业生产上取得了举世瞩目的成就。但我国的农业也面临着许多问题,如生物多样性的破坏和环境污染等。某校研究性小组和对某农业生态系统的各种生物进行了认真调查分析,并绘出了右图所示的食物网。
(4分)我国是一个农业大国,在农业生产上取得了举世瞩目的成就。但我国的农业也面临着许多问题,如生物多样性的破坏和环境污染等。某校研究性小组和对某农业生态系统的各种生物进行了认真调查分析,并绘出了右图所示的食物网。
请据图回答:
(1)该食物网中青蛙和蜘蛛的关系是______________。
(2)该生态系统容易遭到破坏的原因是_____________。
(3)夏季农民经常在农田里除草、灭虫。请从生态
系统的能量流动角度,说明这样做目的是__________
。,
(4)信息传递在生态系统最中有着重要的作用,举出两个人们利用信息传递进行无污染的生物防治害虫的实例 。
从物理和化学的两道题中任选一题做答。如果两道都做,只按第一题计分。
31.(16分)现在在墨西哥爆发的猪流感是由A型流感病毒引起的猪呼吸道传染病,初步研究检测出这种病毒是A型流感病毒,携带有H1N1亚型猪流感病毒毒株,包含有禽流感、猪流感和人流感三种流感病毒的核糖核酸基因片断,同时拥有亚洲猪流感和非洲猪流感病毒特征。路透社援引美国科学家的研究成果报道,称这种新型流感病毒为猪流感,是因为科学家曾在患者体内检测出H1N1亚型猪流感病毒毒株,但这种新型流感病毒具有病毒杂交特性。根据所学知识回答下列问题:
(1)科学家认为H1N1型猪流感病毒变异速度可能很快,可能超出人们的想象。流感病毒很容易发生变异,从遗传物质的角度来看是因为_________________________ 。
(2)侵入到猪体内的猪流感病毒在免疫学上属于 ,生物体往往先通过 的作
用阻止病毒的散播,再通过 的作用予以消灭。
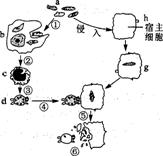 (3)右图所示为某种免疫过程示意图,
(3)右图所示为某种免疫过程示意图,
①试写出b细胞和c细胞d细胞的名称:
b细胞
c细胞
d细胞
②在该抗原刺激机体产生以上免疫过程时,能否同时刺激机体产生其他特异性免疫?若能,请说明免疫类型。 。
30.(12分)夏季校园的浅水池塘中均匀分布着开黄花(完全花,有雌蕊和雄蕊)的多年生草本植物水毛茛,它的叶裸露在空气中的呈扁平状,浸在水中的叶呈丝状;水毛茛全株有毒,为一般鱼类等水生动物所不食。生物小组的同学拟在池塘中放养专食水毛茛的转基因小金鱼,经过实地调查和科学计算,他们共放了X尾小金鱼,认为这是该池塘能平衡喂养的最大数量。
(1)运用你所学的知识,分析他们是如何进行调查和计算小金鱼数量的?
A.进行池塘内水毛茛的种群密度的取样调查,计算出水毛茛的总生物量;
B.__________________________________________________________________;
C.__________________________________________________________________。
(2)为了快速增加水毛茛的种群数量,生物小组的同学用其丝状叶进行植物组织培养,一次获得1500株幼苗。组织培养应使用___________(液体∕固体)培养基;幼苗的叶为___________,这一现象说明_______________________________________。
(3)次年夏季,发现众多开黄花的水毛茛中有一枝开的是白花,经请教专家确定为控制花色的基因发生突变,产生了等位基因。请你设计一个可行的植物杂交育种实验(用遗传图解和必要的文字表示),以获得能稳定遗传的白花水毛茛(代表基因型的字母自设)。
29. (6分)一般来说,细胞周期中的分裂间期和分裂期相比,持续时间短的时期是_______;动物细胞培养时,如果缺少氨基酸的供应,细胞一般会停在细胞周期的_______________,假定体细胞的染色体数是10,将体细胞放入含有3H-胸腺嘧啶的培养液中培养,请推测其中一个细胞进行一次DNA复制后,该细胞分裂后期将有___________条染色体被标记。
28.(15分) 能源短缺是人类社会面临的重大问题。甲醇是一种可再生能源,具有广泛的开发和应用前景。
(1)工业上一般采用下列两种反应合成甲醇:
反应I:
CO(g) + 2H2(g)  CH3OH(g) ΔH1
CH3OH(g) ΔH1
反应II: CO2(g) + 3H2(g)  CH3OH(g) +
H2O(g) ΔH2
CH3OH(g) +
H2O(g) ΔH2
① 上述反应符合“原子经济”原则的是 (填“I”或“Ⅱ”)。
② 下表所列数据是反应I在不同温度下的化学平衡常数(K)。
|
温度 |
250℃ |
300℃ |
350℃ |
|
K |
2.041 |
0.270 |
0.012 |
由表中数据判断ΔH1 0 (填“>”、“=”或“<”)。
③ 某温度下,将2 mol CO和6 mol H2充入2L的密闭容器中,充分反应,达到平衡后,测得c(CO)= 0.2 mol/L,则CO的转化率为 。
(2)已知在常温常压下:
① 2CH3OH(l) + 3O2(g) = 2CO2(g) + 4H2O(g) ΔH = -1275.6 kJ/mol
② 2CO (g)+ O2(g) = 2CO2(g) ΔH = -566.0 kJ/mol
③ H2O(g) = H2O(l) ΔH = -44.0 kJ/mol
请计算1 mol甲醇不完全燃烧生成1 mol一氧化碳和液态水放出的热量为
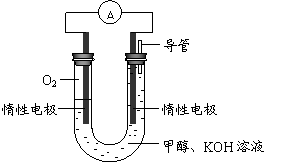 (3)某实验小组依据甲醇燃烧的反应原理,
(3)某实验小组依据甲醇燃烧的反应原理,
设计如右图所示的电池装置。
① 该电池正极的电极反应为
。
② 工作一段时间后,测得溶液的
pH减小,该电池总反应的化学方程式为
。
27.(14分)
A、B、C、D、E均为中学化学的常见单质或化合物,它们之间的反应关系如图所示:

(1)若A是短周期中原子半径最大的元素构成的单质,E既可溶于盐酸又可溶于NaOH溶液,E溶于NaOH溶液的离子方程式是 ;工业上冶炼A的化学反应方程式是 。
(2)若C是既含有极性键又含有非极性键的四原子分子,则实验室制取C的化学方程式是 ;1 mol C完全燃烧生成液态水时放热1300 kJ·mol-1,则C完全燃烧的热化学方程式是 。A与盐B的溶液反应时只生成气体C、碳酸钙沉淀和水,则B的化学式是 。
26.(14分)某研究性学习小组查阅资料得知,漂白粉与硫酸反应可以制得氯气,化学方程式为:Ca(ClO)2+CaCl2+2H2SO4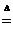 2CaSO4+2Cl2↑+2H2O
。他们设计了如下制取氯气并验证其性质的实验。
2CaSO4+2Cl2↑+2H2O
。他们设计了如下制取氯气并验证其性质的实验。
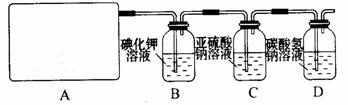
试回答:
(1)该实验中A部分的装置是 (填写装置的序号)。

(2)请你设计一个实验,证明洗气瓶C中的Na2SO3已经被氧化(简述实验步骤):
。
(3)写出D装置中发生反应的离子方程式 。
(4)该实验存在明显的缺陷,请你提出改进的方法 。
25.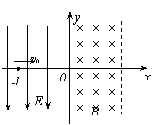 (15)如图所示,坐标空间中有场强为E的匀强电场和磁感应强度为B的匀强磁场,Y轴为两种场的分界面,图中虚线为磁场区域的右边界,现有一质量为m,电荷量为-q的带电粒子从电场中坐标位置(-L,0)处,以初速度v0沿x轴正方向开始运动,且已知L = (重力不计),试求:使带电粒子能穿越磁场区域而不再返回电场中,磁场的宽度d 应满足的条件.
(15)如图所示,坐标空间中有场强为E的匀强电场和磁感应强度为B的匀强磁场,Y轴为两种场的分界面,图中虚线为磁场区域的右边界,现有一质量为m,电荷量为-q的带电粒子从电场中坐标位置(-L,0)处,以初速度v0沿x轴正方向开始运动,且已知L = (重力不计),试求:使带电粒子能穿越磁场区域而不再返回电场中,磁场的宽度d 应满足的条件.
24.(12分)一质量为m,带电-Q的点电荷用绝缘细线悬挂,置于电场之中,平衡时与竖直方向成θ角。
(1)若电场为水平方向的,求场强。
(2)保持θ角不变,求最小的场强。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com