
27.(12分)下表是元素周期表的一部分,回答下列问题:
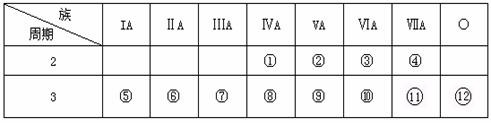
(1)在这些元素中,________(用元素符号填写,下同)是最活泼的非金属元素; ________是最不活泼的元素。
(2)这些元素的最高价氧化物的对应水化物中__________酸性最强;能形成两性氢氧化物的元素是________。
(3)从⑤到 的元素中,_______原子半径最小,写出③形成的氢化物的结构式 。
的元素中,_______原子半径最小,写出③形成的氢化物的结构式 。
(4)⑥、⑧、⑩的最高价氧化物固态时分别属于_________、__________、__________晶体。
(5)比较⑤与⑥的化学性质,_________更活泼,试用实验证明(简述简单操作、主要现象
和结论) 。
26.(11分)热化学方程式,不仅能表示反应和生成物,而且能反映化学反应过程中的的能量变化。试根据条件,回答下列问题:
(1)氢气在氧气在燃烧生成水的热化学方程式,完成下列热化学方程式:
2H2(g)+O2(g)=2H2O(l) ΔH1 =-571.6 kJ·mol-1;
H2(g)+1/2O2(g)=H2O(g) ΔH2 =-241.8 kJ·mol-1
①H2(g)+1/2O2(g)=H2O(l) ΔH3 = kJ·mol-1
② H2(g)+ O2(g)= H2O(g) ΔH4=-483.6 kJ·mol-1
③2H2O(l)=2H2(g)+O2 (g) ΔH5 = kJ·mol-1
(2)ΔH1与ΔH4存在差异的原因是:
(3)由⑵可知书写热化学方程式时一定要注意:
(4)已知每千克汽油(以C7H16表示,呈液态)燃烧生成二氧化碳和液态水时约放热46 000 kJ。请写出汽油燃烧的热化学方程式 ;
等质量的氢气与汽油燃烧, 放出的热量多,氢气被公认为21世纪替代矿物燃料的理想能源,试简述氢气作为能源的三个主要优点:
①______________________________;②_______________________________;
③____________________________________。
25.(6分)现有①CaCl2 ②金刚石 ③NH4Cl ④干冰 ⑤H2SO4 ⑥碘片六种物质,按下列要求回答:(填序号)
熔化或汽化时不需要破坏化学键的是________,熔化时需要破坏共价键的是________,属于离子化合物的是___________________。
24.若短周期中的两种元素可以形成原子个数比为2:1的化合物,则这两种元素的原子序数之差不可能是 ( )
A.3 B.4 C.5 D.6
23.某温度下将N2和H2充入一恒容的密闭容器中,发生可逆反应:N2 + 3H2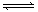 2NH3
2NH3
某一时刻用下列各组内两种物质表示的该反应速率,其中正确的是 ( )
A.v(N2) = 0.01 mol/(L·s),v(H2) = 0.02 mol/(L·s),
B.v(H2) = 0.02 mol/(L·s),v(NH3) = 1.2 mol/(L·min),
C.v(N2) = 0.01 mol/(L·s),v(NH3) = 1.2 mol/(L·min),
D.v(H2) = 0.06 mol/(L·s),v(NH3) = 0.4 mol/(L·min)
22.
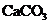 与稀盐酸反应(放热反应)生成
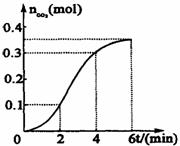
与稀盐酸反应(放热反应)生成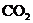 的量与反应时间的关系如下图所示.下列结论不正确的 ( )
的量与反应时间的关系如下图所示.下列结论不正确的 ( )
A.反应开始2分钟内平均反应速率最大
B.反应4分钟后平均反应速率最小
C.反应2-4分钟内温度对反应速率的影响比浓度大
D.反应在第2min到第4min间生成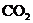 的平均反应
的平均反应
速率最大
21.A、B、C、D、E是同一周期的五种主族元素,A和B的最高价氧化物对应的水化物均呈碱性,且碱性B>A,C和D的气态氢化物的稳定性C>D;E是这五种元素中原子半径最小的元素,则它们的原子序数由大到小的顺序是 ( )
A.A、B、C、D、E B.B、A、D、C、E
C.E、C、D、B、A D.E、C、D、A、B
20.C+CO2
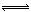 2CO(正反应吸热),反应速率为v1:N2+3H2
2CO(正反应吸热),反应速率为v1:N2+3H2 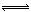 2NH3(正反应放热),反应速率为v2。对于上述反应,当温度降低时,v1和v2的变化情况是
( )
2NH3(正反应放热),反应速率为v2。对于上述反应,当温度降低时,v1和v2的变化情况是
( )
A.同时增大 B.同时减小
C.v1增加,v2减小 D.v1减小,v2增大
19.下列各表中的数字代表的是元素的原子序数。表中数字所对应的元素与它们在周期表中的位置相符的是 ( )
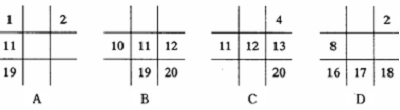
18.下列变化中,不需要破坏化学键的是 ( )
A.氯化氢溶于水 B.加热使冰融化
C.加热使氧化镁熔化 D.氯化钠溶于水
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com