
3. 设集合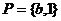 ,
,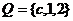 ,
,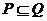 , 若
, 若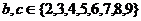 ,则 b = c的概率是A
,则 b = c的概率是A 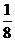 B
B 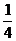 C
C  D
D
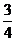
2.已知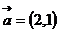 ,
,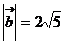 ,且
,且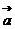 ∥
∥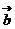 ,则
,则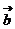 为( )
为( )
A、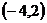 B、
B、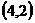 C、
C、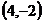 或
或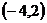 D、
D、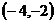 或
或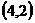
1. 不等式1<x<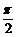 成立是不等式(x-1)tanx>0成立的
成立是不等式(x-1)tanx>0成立的
A.充分不必要条件 B.必要不充分条件
C.充要条件 D.非充分非必要条件
22.[题文](每空3分,共9分)在50mL amol/L的硝酸溶液中,加入6.4gCu,全部溶解,假设 硝酸的还原产物只有NO2和NO,将反应后溶液用蒸馏水稀释至100mL时测得c(NO
硝酸的还原产物只有NO2和NO,将反应后溶液用蒸馏水稀释至100mL时测得c(NO )=3mol/L,
)=3mol/L,
(1)稀释后溶液c(H+)=_____ mol
mol /L。
/L。
(2)若a=9,则生成的气体中NO2的物质的量为____mol。
(3)治理氮氧化物污染的方法之一是用NaOH溶液进行吸收,反应原理如下:
NO2+NO+2NaOH=2NaNO3+H2O
2NO2+2NaOH=NaNO3+NaNO2+H2O
若将上述的NO2和NO的混合气体通入1mol/L的NaOH恰好被吸收,则NaOH溶液的体积为______mL。
[答案](1)1 (2)0.125 (3)150
[解析]
[标题]炎德·英才大联考三湘名校2010届高三月考试卷(一)
[结束]
21.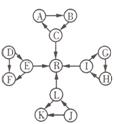 [题文](每空2分,共8分)某化学兴趣小组在探究常见物质转化时,发现部分物质存在如图所示的三角转化关系(部分反应
[题文](每空2分,共8分)某化学兴趣小组在探究常见物质转化时,发现部分物质存在如图所示的三角转化关系(部分反应 物或生成物已略去):
物或生成物已略去):
已知:①图中每个小三角形的三种物质中至少含有一种相同元素,K与L含有完全相同的元素;②D、J为固体单质,R为气体单质,其余物质为常见化合物;③A能使品红溶液褪色,也能使澄清石灰变浑浊,C的浓溶液与固体J在加热条件下反应生成A、L以及水;④E为淡黄色化合物,E与L或水反应都能生成R;⑤I为氧化物,I与F或C都 能反应;G和L反应生成白色胶状沉淀H,H具有较强的吸附性。根据以上信息,
能反应;G和L反应生成白色胶状沉淀H,H具有较强的吸附性。根据以上信息, 回答下列问题:
回答下列问题:
(1)写出下列反应的化学方程式:
①D→F:________________________________。
②L→R:________________________________。
( 2)写出下列反应的离子方程式:
2)写出下列反应的离子方程式:
①G中通入过量CO2:__________________________。
②I→G:________________________________。
[答案](1)①2Na+2H2O =2NaOH+H2↑ ②2Na2O2+2CO2=2Na2CO3+O2
=2NaOH+H2↑ ②2Na2O2+2CO2=2Na2CO3+O2
(2)①AlO +CO2+2H2O=Al(OH)3↓+HCO
+CO2+2H2O=Al(OH)3↓+HCO ②Al2O3+2OH
②Al2O3+2OH -=2 AlO
-=2 AlO +H2O
+H2O
[解析]
[标题]炎德·英才大联考三湘名校2010届高三月考试卷(一)
[结束]
20.[题文](每空2分,共12分)某校化学研究性学习小组的同学在学习了金属的知识后,为了解Cu的常见化合物性质,运用类比学习的思想提出 如下的问题,探究。请你协助该小组的同学完成下列研究。
如下的问题,探究。请你协助该小组的同学完成下列研究。
[提出问题]
①Cu的金属活泼性小于Al,Al(OH)3具有两性,Cu(OH)2也具有两性吗?
②通常情况下,+2价Fe的稳定性小于+3价Fe,+1价Cu的稳定性也小于+2价Cu吗?③CuO能被H2、CO等还原,也 能被NH3还原吗?
能被NH3还原吗?
[实验方案]
(1)解决问题①需用到的药品有:CuSO4溶液、_________(填试剂),同时进行相关实验。
(2)解决问题②的实验步骤和现象如下:取98g Cu(OH)2固体,加热至80℃-100℃时,得到黑色固体粉末,继续加热到1000℃以上,黑色粉末全部变成红色粉末A。冷却后称量A的质量为72g。向A中加入适量的稀硫酸,得到蓝色溶液,同时观察到容器还有红色固体存在。据些可推得,A的化学式为_____。
(3)为解决问题③,设计的实验装置为(夹持及尾气处理装置未画出):
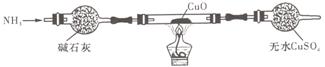
实验中观察到CuO变为红色物质,无水CuSO4变____色。同时生成一种对大气无污染的气体。
[实验结论]
(1)Cu(OH)2具有两性,证明Cu(OH)2具有两性的实验现象应是____________________________________。
(2)根据“实验方案(2)”,得出的+1价Cu和+2价Cu稳定性大小的结论是__________________________________。
[问题讨论]
(1)有同学认为NH3与CuO反应生成的 红色物质是Cu,也有同学认为NH3与CuO反应生成的红色物质
红色物质是Cu,也有同学认为NH3与CuO反应生成的红色物质 是Cu和A的混合物。请你设计一个简单的实验检验NH3与CuO反应中生成的红色物质中是否含有A______________________________________________________。
是Cu和A的混合物。请你设计一个简单的实验检验NH3与CuO反应中生成的红色物质中是否含有A______________________________________________________。
[答案][实验方案](1)HCl溶液、NaOH溶液 (2)Cu2O (3)蓝
[实验结论](1)Cu(OH)2既能溶于盐酸,又能溶于NaOH溶液
(2)在高于1000℃时,+1价Cu比+2价Cu稳定;在溶液中+2价Cu比+1价Cu稳定。
[问题讨论](1)取NH3与CuO反应中生成的红色物质少许,加入稀H2SO4,若溶液出现蓝色,说明红色物质中含有A,反之则无。
[解析]
[标题]炎德·英才大联考三湘名校2010届高三月考试卷(一)
[结束]
19. [题文](每空1分,共9分)纯碱、烧碱等是重要的化工原料。
[题文](每空1分,共9分)纯碱、烧碱等是重要的化工原料。
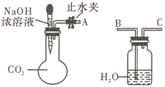
(1)利用如图所示装置可证明二氧化碳与烧碱溶液发生了
反应。将A与B连接,打开止水夹,将胶头滴管中的液体
挤入烧瓶,此时的实验现象是______________________。若其
它操作不变,将A与C连接,可观察到的现象是__________________________________________。
 (2)向100mL 2mol/L的NaOH溶液中通入一定量的CO2,结晶,得到9.3g白色固体,该白色固体
(2)向100mL 2mol/L的NaOH溶液中通入一定量的CO2,结晶,得到9.3g白色固体,该白色固体 的组成是_______(写化学式)。设计实验确认该白色固体中存在的阴离子,试完成下列方案:
的组成是_______(写化学式)。设计实验确认该白色固体中存在的阴离子,试完成下列方案:
|
实验操作 |
实验现象 |
结 论 |
|
①取少量白色固体于试管中,加水溶解,再加足量BaCl2溶液 |
|
|
|
②过滤,取2mL滤液于试管中,滴加酚酞 |
溶液变红 |
|
(3)现代工业常以氯化钠为原料制备纯碱,部分工艺流程如下:
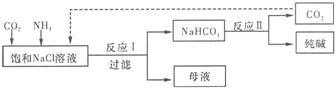
 已知NaHCO3在低温
已知NaHCO3在低温 下溶解度较小。反应Ⅰ为:NaCl+CO2+NH3+H2O
下溶解度较小。反应Ⅰ为:NaCl+CO2+NH3+H2O
NaHCO3↓+NH4Cl,处理母液的两种方法如下:
①向母液中加入石灰乳,可将其中______循环利用,同时得到融雪剂_____。
②向 母液中通入NH3,加入细小食盐颗粒并降温,可得到NH4Cl晶体。
母液中通入NH3,加入细小食盐颗粒并降温,可得到NH4Cl晶体。
试写出通入NH3后,溶解度较小的酸碳酸盐转变为溶解度较大的碳酸盐的离子方程式_________________________________。
[答案](1)水沿导管由广口瓶进入烧瓶。广口瓶中的长导管口有气泡产生
(2)NaOH和Na2CO3
|
实验操作 |
实验现象 |
结 论 |
|
①取少量白色固体于试管中,加水溶解,再加足量BaCl2溶液 |
产生白色沉淀 |
有CO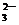 |
|
②过滤,取2mL滤液于试管中,滴加酚酞 |
溶液变红 |
有OH- |
(3)①NH3,CaCl2  ②HCO
②HCO +NH3=NH
+NH3=NH +H2O
+H2O
[解析]
[标题]炎德·英才大联考三湘名校2010届高三月考试卷(一)
[结束]
18.[题文](每空2分,共8分)已知四种强电解质溶液,分别含有下列阴、阳离子中的各一种 ,并且互不重复:NH
,并且互不重复:NH 、Ba2+、Na+、H+、SO
、Ba2+、Na+、H+、SO 、NO
、NO 、OH-、CO
、OH-、CO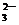 。将这四种溶液分别标记为A、B、C、D,进行如下实验:
。将这四种溶液分别标记为A、B、C、D,进行如下实验:
①在A或D中滴入C,均有沉淀生成
②D和B反应生成的气体能被A吸收
③A和D反应生成的气体能被B吸收
试回答下列问题:
(1)D的化学式是______,判断理由是___________________________________________________________________________。
(2)写出B物质的化学式_____。
(3)写出D和B反应的离子方程式___________________。
[答案](1)(NH4)2CO3,D和A、B都能生成气体,而题给离子中只有H+与CO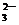 、OH-与NH
、OH-与NH 能反应生成气体,故D只能为(NH4)2CO3。
能反应生成气体,故D只能为(NH4)2CO3。
 (2)NaOH (3)NH
(2)NaOH (3)NH +OH- NH3↑+H2O
+OH- NH3↑+H2O
[解析]
[标题]炎德·英才大联考三湘名校2010届高三月考试卷(一)
[结束]
17.[题文](每空1分,共6分)科学家在研究化学物质时,常常对物质进行分类,以便对同类物质的组成和性能进行 深入的研究。下列各组物质中有一种物质与其它物质不属于同一类,请
深入的研究。下列各组物质中有一种物质与其它物质不属于同一类,请 将其挑出来。
将其挑出来。
|
物质组 |
不属于同类物质 |
|
(1)Mg、O2、I2、NO |
|
|
(2)NaOH、Na2CO3、CH4、CaO |
|
|
(3)HClO、H2SO4、NH3·H2O、H2SiO3 |
|
( 4)CO、SO2、CO2、SO3 4)CO、SO2、CO2、SO3 |
|
|
(5)Ca(HCO3)2、Na2CO3、AgNO3、BaSO4 |
|
|
(6)水、液氯、氨水、水银 |
|
[答案]
|
物质组 |
不属于同类物质 |
|
(1)Mg、O2、I2、NO |
NO |
|
(2)NaOH、Na2CO3、CH4、CaO |
CH4 |
|
(3)HClO、H2SO4、NH3·H2O、H2SiO3 |
NH3·H2O |
|
(4)CO、SO2、CO2、SO3 |
CO |
|
(5)Ca(HCO3)2、Na2CO3、AgNO3、BaSO4 |
BaSO4或Ca(HCO3)2 |
(6)水、液氯、 氨水、水银 氨水、水银 |
氨水 |
[解析]
[标题]炎德·英才大联考三湘名校2010届高三月考试卷(一)
[结束]
16. [题文]硝酸与金属反应时,还原产物可能是NO2、NO、N2O、N2或NH
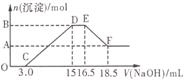
[题文]硝酸与金属反应时,还原产物可能是NO2、NO、N2O、N2或NH 中的一种或几种。现有一定量的Al粉和Fe粉的混合物与100mL稀硝酸充分反应,反应过程中无任何气体放出。在反应结束后的溶液中逐滴加入4mol/L的NaOH溶液,加入NaOH溶液的体积与产生沉淀的物质的量的关系如图,则下列说法中不正确的是
中的一种或几种。现有一定量的Al粉和Fe粉的混合物与100mL稀硝酸充分反应,反应过程中无任何气体放出。在反应结束后的溶液中逐滴加入4mol/L的NaOH溶液,加入NaOH溶液的体积与产生沉淀的物质的量的关系如图,则下列说法中不正确的是
A.与HNO3反应后,Fe元素的化合价为+3
B.D→E段反应的离子方程式为:NH +OH-=NH3·H2O
+OH-=NH3·H2O
C.纵坐标A点数值为0.008
D.纵坐标B点数值为0.012
[答案]D
[解析]
[标题]炎德·英才大联考三湘名校2010届高三月考试卷(一)
[结束]
第Ⅱ卷 非选择题(共52分)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com