
6.共价键、离子键、金属键和分子间作用力都是构成物质的微粒间的相互作用,含有上述两种相互作用力的晶体是 
A.SiO2晶体 B.干冰 C.NaCl晶体 D.镁铝合金
5.下列各组给定原子序数的元素,不能形成原子数之比为1∶1稳定化合物的是
A.3和17
B.1和8
C.1和6
D.7和12
4.下列叙述正确的是
A.在氧化还原反应中一定有一种元素的化合价升高,另一种元素的化合价降低
B.阴离子都只有还原性
C.与强酸、强碱都反应的物质只有两性氧化物或两性氢氧化物
D.分子晶体中都存在范德华力,可能不存在共价键
3.工业上冶炼金属一般用热分解法、还原法和电解法,不同的金属应选用不同的冶炼方法。选择的主要依据是 
A.金属的熔点高低
B.金属在自然界中的存在形式

C.金属离子得电子的能力 D.金属的利用价值
2.除去NaHCO3溶液中混有的少量Na2CO3可采取的方法是
A.通入二氧化碳气体
B.加入氢氧化钡溶液
C.加入澄清石灰水
D.加入稀盐酸
1.下列化工生产过程的反应原理,不涉及氧化还原反应的是
A.氯碱工业 B.从海水中提取镁
C.高炉炼铁 D.侯德榜制碱
25.环保检测中,有害气体的浓度常用1L气体样品中含有害气体的毫克值(mg/L)来表示,如对某气体样品中所含CO的浓度进行测定,其方法和步骤如下:
①首先将2.00L的气体样品通过盛有I2O5固体的加热管,反应后生成CO2和I2;
②用30.0mL 5.00×10-3mol·L-1的硫代硫酸钠溶液吸收所产生的碘,发生的反应为:
I2+2S2O2-3=2I-+S4O2-6;
③将②中溶液取出1/5,加入1.00mL 1.00×10-2mol·L-1碘水,正好将所取溶液中过量的硫代硫酸钠完全氧化。
(1)写出步骤①中CO通过盛I2O5加热管的有关反应化学方程式。
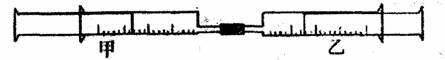 24.如图所示,将甲、乙两个装有不同物质的针筒用导管连接起来,将乙针筒内的物质压到甲针筒内,进行下表所列的不同实验(气体在同温同压下测定)。试回答下列问题:
24.如图所示,将甲、乙两个装有不同物质的针筒用导管连接起来,将乙针筒内的物质压到甲针筒内,进行下表所列的不同实验(气体在同温同压下测定)。试回答下列问题:
|
实验序号 |
甲针筒内物质 |
乙针筒内物质 |
甲针筒的现象 |
|
1 |
10mLFeSO4溶液 |
10mLNH3 |
生成白色沉淀,后变色 |
|
2 |
20mLH2S |
10mL SO2 |
|
|
3 |
30mLNO2(主要) |
10mL H2O(l) |
剩余无色气体,活塞自动向内压缩 |
|
4 |
15mL Cl2 |
30mL NH3 |
|
(1)实验1中,沉淀最终变为______色,写出沉淀变色的化学方程式__________________。
(2)实验2甲针筒内的现象是:有___________生成,活塞________移动(填向外、向内、不)。反应后甲针筒内有少量的残留气体,正确的处理方法是将其通入______溶液中。
(3)实验3中,甲中的30mL气体是NO2和N2O4的混合气体,那么甲中最后剩余的无色气体是__ __,写出NO2与H2O反应的化学方程式为_________________。
(4)实验4中,已知:3Cl2+2NH3 ==N2+6HCl。甲针筒出活塞有移动,针筒内有白烟产生外,气体的颜色变为___________。最后针筒内剩余气体的体积约为_______mL。
22.氮及其化合物在生活、生产和科技等方面有重要的应用。请回答下列问题:
(1)氮元素基态原子的价电子排布式为 。
(2)在氮气分子中,氮原子之间存在着 个σ键和 个π键;
(3)氮、氧、氟是周期表中相邻的三种元素,比较:(填“大于”、“小于”或“等于”)
①氮原子的第一电离能 (填“大于”、“小于”或“等于”)氧原子的第一电离能;
②N2分子中氮氮键的键长 (填“大于”、“小于”或“等于”)F2分子中氟氟键的键长;
(4)氮元素的氢化物(NH3)是一种易液化的气体,请阐述原因是 ;
(5)配合物[Cu(NH3)4]Cl2中含有4个配位键,若用2个N2H4代替其中的2个NH3,得到的配合物[Cu(NH3)2(N2H4)2]Cl2中含有配位键的个数为 。
 23.V、W、X、Y、Z是由周期表中1~20号部分元素组成的5种化合物,其中V、W、X、Z均由两种元素组成,上述5种化合物涉及的所有元素的原子序数之和等于35。它们之间的反应关系如下图:
23.V、W、X、Y、Z是由周期表中1~20号部分元素组成的5种化合物,其中V、W、X、Z均由两种元素组成,上述5种化合物涉及的所有元素的原子序数之和等于35。它们之间的反应关系如下图:
(1)V的电子式是 、W的化学式是 、X的结构式是 、Y的俗名是 、Z的结构简式是 。
(2)由上述5种化合物中2种化合物反应可生成一种新化合物,它包含了5种化合物中的所有元素,生成该化合物的化学方程式是 :
21.某反应的反应物和产物如下:
KMnO4+ KI+ H2SO4→ MnSO4+ I2+ KIO3+ K2SO4+ H2O
(1)该反应的氧化剂是 ;
(2)如果该反应议程式中I2和KIO3的系数都是5,则:
①KMnO4的系数是 ;
②配平上面的化学方程式,将系数填在相关物质前方的空格处,并在方程式上标出电子转移的方向和数目。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com