

16.A、B、C、D四种短周期元素的原子半径依次减小,A与C的核电荷数之比为3:4,D能分别与A、B、C形成电子总数相等的分子X、Y、Z。下列叙述正确的是 
A.X、Y、Z的稳定性逐渐减弱
B.A、B、C、D只能形成5种单质
C.Y、X、Z三种化合物的熔沸点逐渐升高
D.自然界中存在多种由A、B、C、D四种元素组成的化合物
15.早在1807年化学家戴维用电解熔融氢氧化钠制得钠4NaOH(熔) 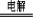 4Na + O2↑+ 2H2O;后来盖·吕萨克用铁与熔融氢氧化钠作用也制得钠,反应原理为:
4Na + O2↑+ 2H2O;后来盖·吕萨克用铁与熔融氢氧化钠作用也制得钠,反应原理为:

3Fe+4NaOH Fe3O4+2H2↑十4Na↑。
Fe3O4+2H2↑十4Na↑。 下列有关说法正确的是
下列有关说法正确的是

A.电解熔融氢氧化钠制钠,阳极发生电极反应为: 2OH--2e-=H2↑+O2↑
2OH--2e-=H2↑+O2↑

B.盖·吕萨克法制钠原理是利用铁的还原性比钠强

C.若戴维法与盖·吕萨克法制得等量的钠,则两反应中转移的电子总数也相同

D.目前工业上常用电解熔融氯化钠法制钠,电解槽中石墨极为阳极,铁为阴极
14.在第n电子层中,当它作为原子的最外层时容纳电子数最多与第(n-1)层相同; 当它作为原子的次外层时,其电子数比(n-1)层多10个,则对此电子层的判断正确的是

A.必为K层 B.只能是L层
C.只能是M层 D.可以是任意层
13.将等物质的量的镁和铝混合,取等质量的该混合物四份,分别加到足量的下列溶液中,充分反应后,放出氢气最多的是 
A.3mol·L-1 HCl B.4mol·L-1 HNO3 
C.8mol·L-1 NaOH D.18mol·L-1 H2SO4
12.已知反应 10AgF + 5Cl2
+ 5H2O = 9AgCl + AgClO3 +10HF+O2,则有1mol O2生成时,反应中所转移的电子为 
A.4mol B.9mol C.10mol D.5mol 
11.两种元素原子的核外电子层数之比与最外层电子数之比相等,则在周期表的前
10号元素中,满足上述关系的元素共有

A. 1对 B. 2对
C.
3对 D. 4对
10.用NA表示阿伏加德罗常数的值,下列叙述正确的是
A.1 mol臭氧中含有的氧原子数为NA
B.标准状况下,2.24 L D2O中含有的电子数为NA
C.0.1 mol甲烷所含质子数为NA
D.原子数均为NA的14C和14N中所含的中子数相等
9.X、Y均为元素周期表中前20号元素,其简单离子的电子层结构相同,下列说法正确的是
A.由mXa+与nYb-,得m+a=n-b
B.X2-的还原性一定大于Y-
C.X、Y一定不是同周期元素
D.若X的原子半径大于Y,则气态氢化物的稳定性HmX一定大于HnY
8.下列有关金属的工业制法中正确的是 
A.制钛:用金属钠置换氯化钛(TiCl4)溶液中的钛 
B.炼铁:用焦炭和空气反应产生的CO在高温下还原铁矿石中的铁 
C.制钠:用海水为原料制得精盐,再电解纯净的NaCl溶液 
D.炼铜:用黄铜矿经电解精炼得到纯度为99.9%的铜
7.下列各组离子在给定条件下能大量共存的是
A.能使酚酞试液变红的溶液中:Na+、Cl-、SO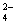 、Fe3+
、Fe3+
B.c(H+)=1.0×10–13mol·L-1的溶液中:Na+、SO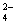 、Al(OH)4-、CO
、Al(OH)4-、CO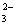

C.c(H+):c(OH-)=105:1的溶液中:K+、HCO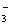 、Cl-、Na+
、Cl-、Na+
D.强酸性溶液中:NH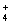 、I-、Fe2+、NO
、I-、Fe2+、NO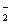

湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com