
30.(16分)化学兴趣小组发现,往CuSO4溶液中加入一定浓度的Na2CO3溶液得到的蓝色沉淀,若加入NaOH溶液则得到浅绿色沉淀。为此,小组同学对沉淀成份作了如下探究:
I.探究蓝色沉淀的成份
[猜想]:蓝色沉淀①可能是CuCO3;②可能是Cu(OH)2;③是两者的混合物。
[设计方案]:小组同学利用下列装置通过实验测定其组成
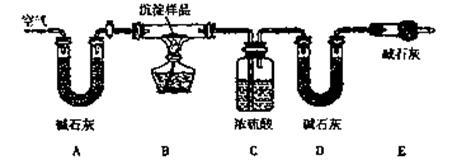
[问题与讨论]
(1)写出②猜想的依据 。
(2)装置A中碱石灰的作用是 。
(3)检查装置气密性并装好药品后,点燃酒精灯前应进行的操作是 。
(4)若沉淀样品的质量为mg。装置C质量增加了ng,则沉淀中CuCO2的质量分数为 。
II.通过查找资料得知,该浅绿色沉淀物可能是溶解度最小的碱式硫酸铜(化学式为CUSO4·3Cu(OH)2)。请你设计一个实验,证明浊液中的浅绿色沉淀物中是否含有硫酸根离子的方法 。
23. 铅蓄电池是常见的二次电池。是池两极材料分别是指铅、二氧化铅,电解液是硫酸溶液。铅蓄电池在充、放电时发生如右反应:PbO2+2H2SO4+Pb
2PbSO4+2H2O。下列叙述正确的是( )
铅蓄电池是常见的二次电池。是池两极材料分别是指铅、二氧化铅,电解液是硫酸溶液。铅蓄电池在充、放电时发生如右反应:PbO2+2H2SO4+Pb
2PbSO4+2H2O。下列叙述正确的是( )
A.电池工作时Pb2-向负极迁移
B.放电时负极反应为Pb+SO2-4=pbSO4+2e-
C.用该电池解饱和食盐水产生0.5molCl2消耗硫酸1mol
D.充电时PbO2电极与电源负极相连
第Ⅱ卷
22. 下列反应的离子方程式书写正确的是 ( )
下列反应的离子方程式书写正确的是 ( )
A.将NaOH固体加入热的浓NH4HSO3溶液中:NH+4+OH- NH3↑+H2O
B.Fe3O4与过量的稀HNO3反应:Fe3O4+8H+====Fe-2+2Fe3++4H2O
C.Na2CO3稀溶液中通入少量CO2:CO2-3+CO2+H2O===2HCO-3
 D.Na2S溶液呈碱性:S2+H2O HS-+OH-
D.Na2S溶液呈碱性:S2+H2O HS-+OH-
12.下列有关实验设计科学正确的是 ( )
|
编号 |
实验目的 |
实验设计 |
|
A |
测定氨气的体积 |
通过盛饱和NaCl溶液的洗气瓶 |
|
B |
提取溴水中溴单质 |
在分液漏斗中加入酒精萃取后分液 |
|
C |
比较S和Cl元素的非金属性 |
测定Na2SO2和NaClO溶液的pH |
|
D |
验证SO2漂白性和还原性 |
将SO2通入晶红溶液、KMnO4溶液 |
11.下列说法正确的是 ( )
A.在KI溶液中加入氯化银,一段时间后沉淀变成黄色,说明同温度下K(AgI)<K(AgCl)
B.0.1mol·L-1的NaHCO3溶液:c(H+)+c(H2CO3)=2c(CO2-3)+c(OH-)
C.中和pH与体积都相同的盐酸和醋酸,消耗NaOH的物质的量之比是1:1
D.NaHCO3溶液与NaAlO2溶液混合产生白色沉淀,说明酸性:HCO-2<Al(OH)2
10.短周期元素A、B、C的原子序数依次递增,其原子的最外层电子数之和为9,A与C同主族,B原子最内层电子数为最外层电子数的2倍,下列有关叙述正确的是 ( )
A.A与C可形成离子化合物
B.A的氢化物的稳定性小于C的氢化物的稳定性
C.原子半径A<B<C
D.B的氧化物可能含有共价键
9.下列说法正确的是 ( )
A.工业上用C还原Al2O2产生Al
B.氯水能使红色花瓣褪色
C.常温下,硅与浓HNO3反应放出NO2
D.Fe(OH)2溶于NaOH溶液
8.下列说法错误的是 ( )
A.乙醇和乙酸都可以由玉米等含糖类物质制取
B.煤的气化可以得到水煤气
C.鸡蛋清中加入CuSO4溶液产生盐析
D.石油分离可获得汽油、煤油和柴油
7.设阿伏德罗常数(NA)的数值为nA,下列说法正确的是 ( )
A.100ml 1mol·L-1氧化镁溶液中含Cl-数目为2nA
B.10g氖气的体积约为11.2L
C.5.6g铁与足量的氯气反应失去电子0.2NA
D.1mol甲基(-CH3)的电子数目为9nA
28.(14分) 实验室有如下图所示的仪器:
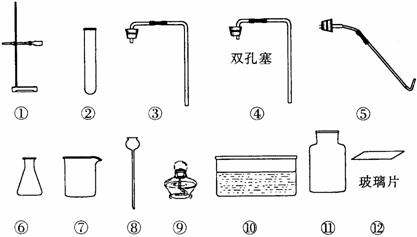
(1) 写出下列仪器的名称:
⑥ ,⑧ ;
(2) 实验室用加热高锰酸钾的方法制取并用排水法收集几瓶O2气体,若已选用了①、②、⑤、⑨、⑩,还应选用的两种仪器是(填编号): ,
发生反应的化学方程式是: ;
(3) 实验室制取氧气有以下主要操作步骤:①加热②把药品装入试管后固定在铁架台上③检查装置的气密性④熄灭酒精灯⑤用排水法收集气体⑥从水槽中取出导管。正确的操作顺序是(写序号)___ _;
(4) 若要制取3.2g氧气,请计算:
①高锰酸钾(KMnO4)的相对分子质量为 ,
②要制取3.2g的氧气,需要高锰酸钾的质量为 ;
(5)某同学为了探究催化剂的量对化学反应速率的影响,利用上图中的仪器做了二氧化锰催化过氧化氢分解的一组实验:
①二氧化锰催化过氧化氢分解的化学方程式为 ;
②有关实验数据如下表:
|
实验组别 |
第1组 |
第2组 |
第3组 |
第4组 |
第5组 |
第6组 |
|
MnO2粉末的用量(g) |
0.1 |
0.3 |
0.5 |
0.7 |
0.9 |
1.1 |
|
10%的H2O2溶液的用量(mL) |
30 |
30 |
30 |
30 |
30 |
30 |
|
收集等体积O2所用时间(S) |
17 |
7 |
4 |
2 |
2 |
2 |
通过对以上实验数据的分析,该实验可以得出的结论是:
Ⅰ ;
Ⅱ 。29.(12分)甲、乙两同学在实验室里进行实验探究,老师提醒他们,实验室的氢氧化钠溶液可能已变质。于是,甲、乙两同学就分别进行了以下实验:
甲:取少量氢氧化钠溶液样品于洁净的试管中,加入稀盐酸,发现有无色气泡产生。
结论:该氢氧化钠溶液已完全变质;
乙:(在甲同学实验的基础上)取少量氢氧化钠溶液样品于洁净的试管中,加入几滴酚酞溶液,发现溶液变红色。结论:该氢氧化钠溶液部分变质。
请回答:
(1)导致氢氧化钠溶液变质的气体是____________(填化学式);
(2)甲的结论__________ (填“正确”或“不正确”),反应的化学方程式为____________;
(3)乙的结论不正确,原因是___________________________________________________;
(4)请你设计一个实验证明上述氢氧化钠溶液部分变质:
|
实验步骤 |
实验现象 |
有关的化学方程式和结论 |
|
|
|
|
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com