
8.定义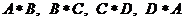 的运算分别对应下图中的(1)、(2)、(3)、(4),那么下图中的(5)、(6)所对应的运算结果可能是
的运算分别对应下图中的(1)、(2)、(3)、(4),那么下图中的(5)、(6)所对应的运算结果可能是

(1) (2) (3) (4) (5) (6)
A、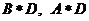 B、
B、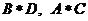 C、
C、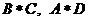 D、
D、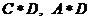
7. 如果命题P(n)对于n=k(k∈N*)时成立,则它对n=k+2也成立。又若P(n)对于n=2时成立,则下列结论正确的是( )
A.P(n)对于所有的正整数n成立 B.P(n)对于所有的正偶数n成立
C.P(n)对于所有的正奇数n成立 D.P(n)对于所有大于1的正整数n成立
6.设函数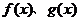 在
在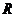 上可导,且导函数
上可导,且导函数 ,则当
,则当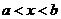 时,下列不等式:(1)
时,下列不等式:(1)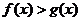 (2)
(2)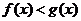 (3)
(3)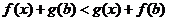 (4)
(4) 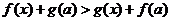 正确的有(
)个
正确的有(
)个
A.4 B.3 C.2 D.1
5.已知条件p: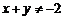 ,条件q:x、y不都为 – 1,则p是q的( )条件
,条件q:x、y不都为 – 1,则p是q的( )条件
A.充分非必要 B.必要非充分 C.充要 D.既不充分也不必要
4.下列命题是真命题的是( )
A.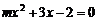 是一元二次方程 B.抛物线
是一元二次方程 B.抛物线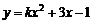 与x轴至少有一个交点
与x轴至少有一个交点
C.互相包含的两个集合相等 D.空集是任何集合的真子集
3. “x > 5”的一个必要不充分的条件是( )
A. x > 6 B.x > 3 C.x < 6 D.x > 100
2.已知复数z1 (m∈R),z 2
(m∈R),z 2 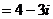 , 若z1·z 2为实数,则m的值为( )
, 若z1·z 2为实数,则m的值为( )
A.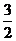 B
B 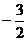 C.
C.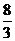 D.
D.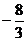
1.已知集合A={y | y= x2 - 4x +3,x∈R},B={y | y= - x2 - 2x +2,x∈R}则A∩B等于( )
A.Φ B.R C.{-1,3} D.[-1,3]
21.选做题 本题有A、B两题,分别对应于“物质结构与性质”和“实验化学”二个选修课程模块的内容,每题12分。请选择其中一题作答,并把所选题目对应字母后的方框涂黑。若两题都作答,将按A题评分。
A.《物质结构与性质》
均由两种短周期元素组成的A、B、C、D化合物分子,都含有18个电子,它们分子中所含原子的数目依次为2、3、4、6。A和C分子中的原子个数比为1∶1,B和D分子中的原子个数比为1∶2。D可作为火箭推进剂的燃料。
请回答下列问题:
(1)A、B、C、D分子中相对原子质量较大的四种元素第一电离能由大到小排列的顺序为 (用元素符号回答)。
(2)A与HF相比,其熔、沸点较低,原因是 。
(3)B分子的空间构型为 形,该分子属于 分子。(填“极性”或“非极性”)
 (4)C为一种绿色氧化剂,有广泛应用。请写出Cu、稀H2SO4与C反应制备硫酸铜的离子方程式
,该反应中反应物Cu原子的基态电子排布式为
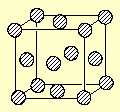
。铜晶体中铜原子的堆积方式为面心立方堆积,右图是铜晶体一个晶胞的示意图,则晶胞中含
个铜原子。
(4)C为一种绿色氧化剂,有广泛应用。请写出Cu、稀H2SO4与C反应制备硫酸铜的离子方程式
,该反应中反应物Cu原子的基态电子排布式为
。铜晶体中铜原子的堆积方式为面心立方堆积,右图是铜晶体一个晶胞的示意图,则晶胞中含
个铜原子。
(5)D分子中心原子的杂化方式是 ,由该原子组成的单质分子中包含
个π键,与该单质分子互为等电子体的常见分子的分子式为 。
B.《实验化学》
乙酰水杨酸(阿斯匹林)是一种常用的解热镇痛、抗风湿类药物,广泛应用于临床治疗和预防心脑血管疾病,近年来还不断发现它的新用途,它可由水杨酸和乙酸酐反应得到。
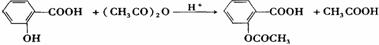
在生成乙酰水杨酸的同时,水杨酸分子间也能发生缩合反应,生成少量聚合物(副产物)。合成乙酰水杨酸的实验步骤如下:
① 向150mL干燥锥形瓶中加入2g水杨酸、5mL乙酸酐和5滴浓硫酸,振荡,待其溶解后,控制温度在85-90℃条件下反应5-10min。然后冷却,即有乙酰水杨酸晶体析出。
② 减压过滤,用滤液淋洗锥形瓶,直至所有晶体被收集到布氏漏斗中。抽滤时用少量冷水洗涤晶体几次,继续抽滤,尽量将溶剂抽干。然后将粗产品转移至表面皿上,在空气中风干。
③ 将粗产品置于100mL烧杯中,搅拌并缓慢加入25mL饱和碳酸氢钠溶液,加完后继续搅拌2-3分钟,直到没有二氧化碳气体产生为止。过滤,用5-10mL蒸馏水洗涤沉淀,合并滤液于烧杯中,不断搅拌,慢慢加入15mL 4mol•L -1盐酸,将烧杯置于冷水中冷却,即有晶体析出。抽滤,用冷水洗涤晶体1-2次,再抽干水分,即得产品。
请回答下列问题:
(1)通常乙酸酐在使用前需重新蒸馏,原因是 。
(2)第①步中,要控制反应温度在85-90℃,应采用_________ 加热方法,水杨酸与乙酸酐的反应过程中,浓硫酸的作用是 。
(3) 在第②步中,用冷水洗涤晶体,其目的是___________________________;
洗涤方法是 。
(4) 第③步中,加入碳酸氢钠的作用是____________________
加入盐酸的作用是________________________
江苏省南通四中2010届高三第三次调研考试
20.(10分) Na2S2O3·5H2O(俗称海波)是照相业常用的一种定影剂。工业上制得的Na2S2O3·5H2O晶体中可能含有Na2SO3。为测定某海波样品的成分,称取三份质量不同的该样品,分别加入相同浓度的硫酸溶液30 mL,充分反应(Na2S2O3+H2SO4=Na2SO4+SO2↑+S↓+H2O)后滤出硫,微热滤液使SO2全部逸出。测得有关实验数据如下表(气体体积已换算为标准状况)。
|
|
第一份 |
第二份 |
第三份 |
|
样品的质量/g |
6.830 |
13.660 |
30.000 |
|
二氧化硫气体的体积/L |
0.672 |
1.344 |
2.688 |
|
硫的质量/g |
0.800 |
1.600 |
3.200 |
试计算:
(1)所用硫酸溶液的物质的量浓度为 。
(2)样品中n(Na2S2O3·5H2O):n(Na2SO3)= 。
(3)某环境监测小组用上述海波样品配制含Na2S2O3 0.100 mol·L-1的海波溶液,并利用它测定某工厂废水中Ba2+的浓度。他们取废水50.00 mL,控制适当的酸度加入足量的K2Cr2O7溶液,得BaCrO4沉淀;沉淀经洗涤、过滤后,用适量的稀盐酸溶解,此时CrO42-全部转化为Cr2O72-;再加过量KI溶液,充分反应后,用上述配制的海波溶液进行滴定,反应完全时,测得消耗海波溶液的体积为36.00 mL。已知有关反应的离子方程式为:
①Cr2O72-
+ 6I- + 14H+ 2Cr3+ + 3I2 + 7H2O
②I2 + 2S2O32-
2I- + S4O62-
③I2 +
SO32- + H2O 2I- + SO42-
+ 2H+
则滴定过程中可用 作指示剂。计算该工厂废水中Ba2+的物质的量浓度。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com