
33.(8分)[化学-有机化学基础]
菠萝酯(结构简式如下)是一种具有菠萝香气的食用香料,
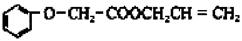
其的合成路线如下:
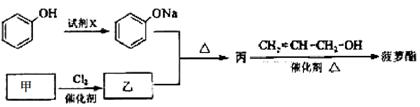
提示:

(1)有机物乙中所含有的官能团是_________
(2)上述合成菠萝酯的过程中,下列反应类型中未涉及到的是___________。
A.取代反应 B.加成反应 C.消去反应 D.中和反应
(3)菠萝酯有多种同分异构体,写出同时满足下列三个条件的同分异构体的结构简式。(写出其中的一种即可)
①能使溴的四氯化碳溶液褪色,遇FeCl3溶液不显紫色
②除苯环外无其他环状基团
③能与NaOH溶液反应,且1mol该同分异构体最多能与2molNaOH反应
_______________________________________________________________________
(4)写出由丙→菠萝酯的化学化学方程式。
_____________________________________________________________________。
32. (8分)[化学-物质结构与性质]
(8分)[化学-物质结构与性质]
我国在青藏高原发现大储量可燃冰。可燃冰的晶体结构模型如下:
(1)C、N、O三种元素第一电离能由
大到小的排列顺序是____>______>_____(填元素符号),
H2O分子中O原子的杂化方式为___________。
(2)“可燃冰”晶体内部存在的作用力有_____________。
(3)下列有关“可燃冰”的说法中,不正确的是_____________。
A.“可燃冰”的存在说明甲烷易溶于水
B.“可燃冰”属于分子晶体,熔点较低
C.相同条件下,“可燃冰”的密度比冰的大
D.“可燃冰”只能在低温、高压环境下稳定存在
(4)晶体中平均每46个水分子构成8个笼,每个笼可容纳1个CH4分子或1个H2O分子,每8个笼中有6个容纳CH4分子, 2个笼填充H2O分子,则“可燃冰”(天然气水合物)的平均组成可表示为_____________。
31.(8分)[化学-化学与技术]
海洋是化学资源宝库,海洋资源的综合利用具有广阔的前景。
回答下列问题:
(1)蒸馏法是人类最早使用的淡化海水的方法,技术和工艺比较完备,但常规蒸馏法法也存在较大缺陷,请说明常规蒸馏法淡化海水的最大缺陷。
①___________________________②_______________________________
(2)离子交换法也是常用的水处理技术。聚丙烯酸钠是一种离子交换树脂,写出聚丙烯酸钠单体的结构简式 。
(3)目前从海水中提取溴的常用流程如下(苦卤,海水蒸发结晶分离出食盐的母液):
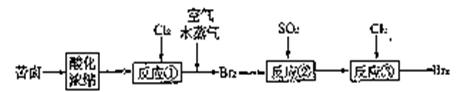
从反应③后的溶液中分离出单质溴的方法是 。
(4)海水提镁过程中,与石灰窑和盐酸厂有着紧密的联系,试说明海水提镁与盐酸厂之间的必然联系。__________________________________________________________
29.(12分)
高纯铜(纯度可达99.99%)广泛应用于电器工业。某粗铜样品中含Fe、Ni、Ag、Au等四种金属杂质,可用电解法进行精炼制得高纯铜。
(1)请在下图1中标明电极材料和电解质溶液的名称。

(2)已知Ni的金属活动性介于Fe和Sn之间。则精炼完成后,在阳极底部的沉积物中可回收到的金属为__________(填化学式)。
(3)若在实验室中完成此实验,可用铅蓄电池做电源。铅蓄电池的电池总反应式为:
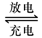
Pb+PbO2+4H++2SO42- 2PbSO4+2H2O
在完全放电耗尽PbO2和Pb时,若按上图2所示连接进行充电,充电一段时间后,则在A电极上生成__________(填化学式),B电极上生成________(填化学式);充电完毕,铅蓄电池的正极是________极(填“A”或“B”)
 (4)电解完毕后,某兴趣小组欲对电解液中的离子
(4)电解完毕后,某兴趣小组欲对电解液中的离子
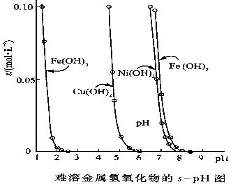
进行分离,他们通过查阅资料,得知相关氢氧
化物在不同pH下的溶解度曲线如右图。
①结合右图分析,相同温度下Ksp[Cu(OH)2]、
Ksp[Ni(OH)2]、Ksp[Fe(OH)2]由大到小的顺
序为__________________________
②分离过程中,使上述溶液的pH逐渐增加,则
溶液中的Cu2+、Fe3+和Ni2+沉淀的先后顺序依次
为 。
|
某化学小组拟采用如下装置(夹持和加热仪器已略去)来电解饱和食盐水,并用电解产生的H2还原CuO粉末来测定Cu的相对原子质量,同时检验氯气的氧化性。

(1)为完成上述实验,正确的连接顺序为A连_______;B连_______(填写连接的字母)。
(2)对硬质玻璃管里的氧化铜粉末加热前,需要的操作为 。
(3)若检验氯气的氧化性,则乙装置的a瓶中溶液可以是 ,对应的现象为 。
(4)丙装置的c瓶中盛放的试剂为 ,作用是_______________________。
(5)为测定Cu的相对原子质量,设计了如下甲、乙两个实验方案
精确测量硬质玻璃管的质量为a g, 放入CuO后,精确测量硬质玻璃管和CuO的总质量为b g , 实验完毕后设计方案求算Cu的相对原子质量
甲方案:通过精确测量硬质玻璃管和Cu粉的总质量为c g, 进而确定Cu的相对原子质量。
乙方案:通过精确测定生成水的质量d g,进而确定Cu的相对原子质量。
①请你分析并回答: 方案测得结果更准确。你认为不合理的方案的不足之处在 。
②若按甲方案测定的数据计算,Cu的相对原子质量 。
选做部分
28.(15分)NH3和CO是重要的化工原料气。
(1)一定条件下,CO与H2反应可制得甲醇:
CO+2H2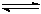 CH3OH
CH3OH
图1表示该反应进行过程中的能量变化(曲线a未使用催化剂,曲线b使用催化剂)。图2表示一定温度下,在体积为2L的密闭容器中加入4mol H2和一定量的CO后,CO和CH3OH(g)的浓度随时间变化情况。
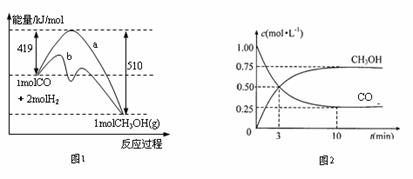
①根据上图1,写出在该条件下CO制备甲醇的热化学反应方程式
②根据上图2计算该该温度下,反应CO(g)+2H2(g) 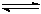 CH3OH(g)的平衡常数为
CH3OH(g)的平衡常数为
③图2所示的具体反应,若在温度保持不变、恒压情况下(体积可变)达到平衡,则H2的平衡转化率将 (填“增大”、“减小”或“不变”)。
(2)已知:a.常温下,CH3COOH和NH3·H2O的电离平衡常数均为1.74×10-5
b.CH3COOH + NaHCO3=CH3COONa+ CO2↑+ H2O
则NH4HCO3溶液呈______性(填“酸”、“碱”或“中”),溶液中浓度最大的离子是______,其次是_______(以上填化学式)。
(3)室温下,向一定量的稀氨水中逐滴加入浓度相同的稀盐酸,直至盐酸过量。
①当溶液中离子浓度关系满足c(NH4+)<c(Cl-)时,则反应的情况可能为
A. 盐酸不足,氨水剩余 B. 氨水与盐酸恰好完全反应 C. 盐酸过量
②实验过程中,H2O的电离程度先_______后________(填“增大”、“减小”或“不变”)。
27.(16分)
请根据下图回答相关问题:

(1)光合色素分布于a中 结构上,提取后通常用 分离;光合色素中既能捕捉光能又能将光能转化为电能的是 。如果白天高温干燥,气孔关闭,将首先影响a中的 反应。
(2)如果在b的土壤中浇过多的水,将首先影响细胞呼吸的第 阶段,进而会产生 对植物器官造成毒害作用。
(3)在一定强度的光照下,若叶肉细胞从周围空气吸收的O2为32mg/小时,那么在一小时内叶肉细胞中的有机物总量将 (减少、不变或增加)。
(4)顶端优势的产生主要受生长素的影响,但近年来发现,外施细胞分裂素给受抑制的侧芽,侧芽就能恢复生长(即顶端优势解除)。请以侧芽生长状况为观测指标,利用以下提供的材料用具,补充完善实验,证明顶端优势既受生长素的影响,也受细胞分裂素的影响。
材料用具:若干长势相同的完整幼苗;适宜浓度的生长素、细胞分裂素;羊毛脂;剪刀等。
实验步骤及预期结果:
①取20株种类和生长状况相同的幼苗,随机平均分为A、B、C、D四组,经实验处理后,培养相同的时间,观察记录侧芽生长状况。
②A组:不做处理,结果:顶芽优先生长,侧芽受抑制不生长
B组:去掉顶芽,结果:_____________
C组:___________________________________;结果:_________________。
D组:__________________________;结果:_________________。
26.(17分)
内环境稳态是神经调节、体液调节和免疫调节共同作用的结果,是人体进行正常生命活动的必要条件。请结合图解回答下面的问题:(图中A、B、C、D表示器官或细胞;①②③表示物质)

(1)维持机体稳态离不开细胞间的信息传递,动物细胞间进行信息传递的途径有:一是通过 、淋巴因子和 等信息分子通过体液运输并作用于靶细胞来实现;二是通过细胞间的直接接触实现信息传递,如人体在特异性免疫过程中发生的 过程。以上两途径的实现离不开细胞膜表面 的识别作用。
(2)图中A表示 ,大脑皮层直接对A发生作用属于 调节,A通过垂体对B发生作用属于 调节;当③分泌过多时,对A和垂体起 作用;图中C表示 ,它是由 分裂、分化形成的。
(3)长期焦虑和紧张会导致机体免疫力 ,请根据图解分析原因:
。
(4)当H1N1病毒第二次进入机体时,首先对H1N1病毒起免疫作用的物质是 ,对于侵入机体细胞病毒的清除则需要通过 。
(5)发烧时应多喝水,此时血浆渗透压降低,刺激下丘脑中的____________,垂体释放______________减少,引起_____________对水分的重吸收减弱,尿液增加,有利于毒素排出。
25.(18分)
一个质量m=0.1 kg的正方形金属框总电阻R=0.5 Ω,金属框放在表面绝缘的斜面AA′BB′的顶端(金属框上边与AA′重合),自静止开始沿斜面下滑,下滑过程中穿过一段边界与斜面底边BB′平行、宽度为d的匀强磁场后滑至斜面底端(金属框下边与BB′重合),设金属框在下滑过程中的速度为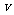 ,与此对应的位移为s,那么
,与此对应的位移为s,那么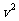 -s图象如图所示,已知匀强磁场方向垂直斜面向上,金属框与斜面间的动摩擦因数μ=0.5,取g=10m/s2,sin53°=0.8; cos53°=0.6。
-s图象如图所示,已知匀强磁场方向垂直斜面向上,金属框与斜面间的动摩擦因数μ=0.5,取g=10m/s2,sin53°=0.8; cos53°=0.6。
(1)根据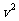 一s图象所提供的信息,计算出金属框从斜面顶端滑至底端所需的时间
一s图象所提供的信息,计算出金属框从斜面顶端滑至底端所需的时间
(2)求出斜面AA′BB′的倾斜角θ
(3)求匀强磁场的磁感强度B的大小
(4)现用平行斜面沿斜面向上的恒力F作用在金属框上,使金属框从斜面底端BB′(金属框下边与BB′重合)由静止开始沿斜面向上运动,匀速通过磁场区域后到达斜面顶端(金属框上边与AA′重合)。试计算恒力F做功的最小值。

24.(15分)
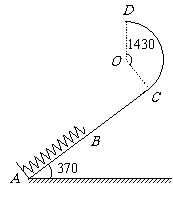
如图所示,在倾角为370的斜面上,一劲度系数k=100N/m的轻弹簧一端固定在A点,自然状态时另一端位于B点。斜面上方有一半径R=0.2m、圆心角等于143°的竖直圆弧形光滑轨道与斜面相切于C处,圆弧轨道的最高点为D。斜面AB段光滑,BC段粗糙且长度为0.4m。现将一质量为1kg的小物块从C点由静止释放,小物块将弹簧压缩了0.2m后速度减为零(不计小物块到达B处与弹簧碰撞时的能量损失)。已知弹簧弹性势能表达式Ek= kx2,其中k为弹簧的劲度系数,x为弹簧的形变量,重力加速度取g=10m/s2,sin370=0.6,cos370=0.8。(计算结果可保留根号)求:
kx2,其中k为弹簧的劲度系数,x为弹簧的形变量,重力加速度取g=10m/s2,sin370=0.6,cos370=0.8。(计算结果可保留根号)求:
⑴小物块与斜面BC段间的动摩擦因数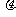
⑵小物块第一次返回BC面上时,冲到的最远位置
 ⑶若用小物块将弹簧压缩,然后释放,要使小物块在CD段圆弧轨道上运动且不脱离圆弧轨道,则压缩时压缩量应满足的条件
⑶若用小物块将弹簧压缩,然后释放,要使小物块在CD段圆弧轨道上运动且不脱离圆弧轨道,则压缩时压缩量应满足的条件
23.(12分)
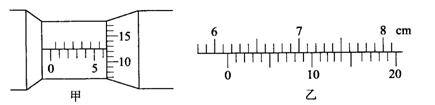
(1)如图所示,螺旋测微器的示数为 mm;游标卡尺的示数为 cm.
(2)为了测量一节干电池的电动势和内阻,实验室提供的实验器材如下:
A.待测干电池(电动势约为1.5V,内电阻约为5Ω)
B.电压表V(0-2V)
C.电阻箱R1(0-99.9Ω)
D.滑动变阻器R2(0-200Ω,lA)
E.开关S和导线若干
①在现有器材的条件下,请你选择合适的实验器材,
并设计出一种测量干电池电动势和内阻的方案,在方框中画出实验电路图;
②利用你设计的实验方案连接好电路,在闭合开关、进行实验前,应注意 ;
③如果要求用图象法处理你设计的实验数据,通过作出有关物理量的线性图象,能求出电动势E和内阻r,则较适合的线性函数表达式是 (设电压表的示数为U,电阻箱的读数为R).
④利用你设计的电路进行实验,产生系统误差的主要原因是:
.
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com