
28.(8分)某一反应体系有反应物和生成物共五种物质:
O2、H2CrO4、Cr(OH)3、H2O、H2O2
已知该反应中H2O2只发生如下过程:H2O2→ O2
(1)该反应中的还原剂是 。
(2)该反应中,发生还原反应的过程是 → 。
(3)写出该反应的化学方程式,并标出电子转移的方向和数目
。
(4)如反应转移了0.3mol电子,则产生的气体在标准状况下体积为 。
27.(12分)(1)向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至中性,写出发生反应的离子方程式:________________________________________.在以上中性溶液中,继续滴加Ba(OH)2溶液,写出此步反应的离子方程式:___________________________.
(2)向Ba(OH)2溶液中,逐滴加入NaHSO4溶液至恰好不再生成沉淀为止,写出反应的离子方程式: ________________________________________.在以上溶液中,继续滴加NaHSO4溶液,写出此步反应的离子方程式:
________________________________________.
(3)向Ba(OH)2溶液中,逐滴加入明矾溶液至溶液中Ba2+恰好完全沉淀,其反应的离子方程式为 ________________________________________.
在上述溶液中,继续滴加明矾溶液,请写出此步反应的离子方程式:_________________.
26.(10分)下图中的每一方框表示有关的一种反应物或生成物,其中A、C为无色气体
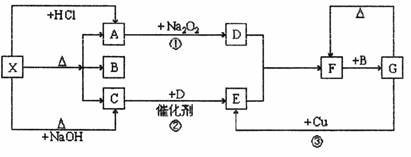
请填写下列空白:
(1)物质X可以是 ,F是 (写分子式)
(2)写出反应③的离子方程式 ③
(3)在反应①中,1mol Na2O2完全反应,转移电子 mol,生成的D全部进入反应②,可以生成E mol。
25.(8分)欲配制500 mL0.2 mol·L-1的碳酸钠溶液,回答下列问题:
(1)通过计算可知,应用托盘天平称取 g碳酸钠。
(2)称量的操作顺序为(填序号)
A、调天平零点 B、游码归零 C、向小烧杯中加碳酸钠 D、称量空烧杯
E、向右盘加砝码并将游码移到所需位置 F、将砝码归盒 G、记录称量结果
(3)若砝码和药品位置放颠倒(假设称量时未用烧杯),天平平衡时,实际称得碳酸钠的质量是 。
(4)下列操作使所配溶液浓度偏高的是 。
A、若称取28.6g Na2CO3·10H2O进行配制 B、称量时用了生锈的砝码
C、往容量瓶转移溶液时,有少量液体溅出 D、碳酸钠中含有不溶性杂质
E、未洗涤溶解Na2CO3的烧杯 F、定容时仰视刻度线
G、小烧杯洗净后未干燥即用来称量 H、容量瓶未干燥即用来配制溶液
24.下列各组试剂在溶液中反应,当两种试剂的量发生改变时,不能用同一离子方程式表示的是 ( )
A.氯化镁、氢氧化钠 B.硫酸钠、氢氧化钡
C.氯化铝、氨水 D.溴化亚铁、氯水
第Ⅱ卷(非选择题,共52分)
23.下列反应中生成物总能量高于反应物总能量的是 ( )
A. 碳酸钙受热分解 B.乙醇燃烧
C. 铝粉与氧化铁粉末反应 D.氧化钙溶于水
22.设N 为阿德罗常数。下列说法正确的是
( )
为阿德罗常数。下列说法正确的是
( )
A.2 L 1mol/L NH Cl溶液含NH
Cl溶液含NH 和Cl
和Cl 均为2 N
均为2 N
B.在常温常压下,22g二氧化碳含有共有电子对总数为2 N
C.0.1 molOH 的质子数与0.1molH
的质子数与0.1molH O的电子数均为N
O的电子数均为N
D.在标准状况下,11.2L辛烷中的碳原子数为4 N
21.下列离子方程式中,正确的是 ( )
A.碳酸钙与盐酸混合2H +CO
+CO =CO
=CO ↑+H
↑+H O
O
B.向氯化铁溶液中加入铁粉Fe +Fe=2Fe
+Fe=2Fe
C.亚硫酸钠溶液与稀硫酸混合2H +SO
+SO =SO
=SO ↑+H
↑+H O
O
D.二氧化锰与浓盐酸混合后加热MnO +4H
+4H +4Cl
+4Cl =MnCl
=MnCl +Cl
+Cl ↑+2H
↑+2H O
O
20.进行化学实验时必须要有安全意识。有下列做法
①金属钠着火.立即用沙子覆盖②不慎将酸溅到手上,应立即用大量水冲洗,然后敷上 NaHCO3 ③温度计摔坏导致水银散落到地面上,迅速用硫磺粉覆盖④皮肤上沾有苯酚时立即用浓氢氧化钠溶液擦洗,再用水洗。其中正确的是: ( )
A.①② B.①③④ C.②③④ D.①②③
19.若以 和
和 分别表示浓度为
分别表示浓度为 和
和 氨水的质量分数,且知2a=b,则下列推断正确的是(氨水的密度比纯水的小)
( )
氨水的质量分数,且知2a=b,则下列推断正确的是(氨水的密度比纯水的小)
( )
A. B.
B. C.
C. D.
D.
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com