
(二)为了进行一项医学测试,A、B和C3名成年人禁食12h,然后摄入含100g葡萄糖的溶液。在摄入葡萄糖前和之后的4h内,定时测定各人血浆内的葡萄糖和胰岛素水平。结果如图所示。A是唯一健康的人,B和C两人均患有糖尿病。(注:血糖测定的单位:mmoL/L=18mg/dL)

血浆内的葡萄糖反应曲线 血浆内的胰岛素反应曲线
(1)解释A摄入葡萄糖后,血浆内的葡萄糖水平为什么先上升,继而下降?
(2)分析导致B、C有不同反应可能的原因。
31.(26分)(一)已知玉米为雌雄同株的异花植物,雄花着生在植株顶端的雄穗上,雌花着生在茎秆中部叶腋间的雌穗上。现有两种性状:籽粒果皮的黄色和白色,籽粒口感的甜与非甜。
(1)让白色果皮玉米接受黄果皮玉米的花粉, 所结籽粒果皮的表现型是_____________。
(2)纯种的甜玉米与纯种的非甜玉米实行间行种植,收获时发现,在甜玉米的果穗上结有非甜玉米的种子,但在非甜玉米的果穗上找不到甜玉米的籽粒。已知甜与非甜是胚乳的性状,若用A和a表示相关基因,试写出非甜玉米植株上所结籽粒的胚乳基因型 。
(3)试用能稳定遗传的白玉米和黄玉米为亲本,设计一个实验方案,预期结果,证明果皮的颜色性状是细胞质遗传还是细胞核遗传?
|
|
 DCPIP(蓝色)+H2O DCPIP-H2(无色)+O2
DCPIP(蓝色)+H2O DCPIP-H2(无色)+O2
为验证光合作用所需的条件,现提供如下材料和用品:离体叶绿体、0.5mol/L蔗糖溶液、1%DCPIP溶液、蒸馏水、量筒、锡箔纸、试管若干、离心机。请依据“希尔反应”涉及的实验原理,补充完整下面的实验设计,并回答下列问题:
(1)方法步骤:
第一步:离体叶绿体溶解于0.5mol/L蔗糖溶液制备成叶绿体悬浮液;
第二步:选取3支试管,编上1号、2号和3号。
第三步:向1号试管中加入1% DCPIP溶液 0.5mL和叶绿体悬浮液5mL,给予光照处理。
……
第四步:将上述试管放置在温度等其他条件相同且适宜的环境中一段时间。
第五步:一段时间后,对各试管用离心机离心5分钟,观察试管内上层清液的颜色。
(2)可能的实验结果及相应的结论:
①观察结果:离心后三支试管内上层清液的颜色分别是 ;
为什么不直接观察试管内的溶液颜色而是要在离心后观察上清液的颜色?
。
②实验结论:光合作用的条件是 。
14.2008年举行的北京奥运会将大量采用有利于保护环境的新技术,如场馆周围80%~90%的路灯将利用太阳能发电,90%的洗浴热水将采用全玻真空太阳能集热技术. 太阳能是由于太阳内部高温、高压条件下的轻核聚变反应产生的,其核反应方程之一是( )
A. N+
N+ He→
He→ O+
O+ H B.4
H B.4 H →
H → He +2
He +2 e
e
C. U+
U+ n→
n→ Xe+
Xe+ Sr+10
Sr+10 n D.
n D. U→
U→ Th+
Th+ He
He
15.对于一定质量的理想气体,下列说法正确的是 ( )
A.若压强增大,则外界对气体一定做正功
B.若与外界没有发生热量交换,则气体内能一定不变
C.若绝热压缩气体,则它的内能一定增加
D.当压强不变而体积和温度变化时,单位时间内与器壁单位面积碰撞的分子数一定不
变
16.如图所示,两平行细光束a、b从空气中垂直射入直角玻璃三棱镜的AB面,对应的折射光线为 、
、 ,且
,且 、
、 有发散的趋势,则下列说法正确的是 ( )
有发散的趋势,则下列说法正确的是 ( )
 A.b光束在棱镜中传播速度较大
A.b光束在棱镜中传播速度较大
B.若b光束能使某金属产生光电效应,则a光束也一
定能使该金属产生光电效应
C.在相同的条件下做双缝干涉实验,b光束对应的干
涉条纹间的距离较大
D.在其它条件不变的情况下,当顶角A增大时,折
射光束 先消失
先消失
 17.如图所示,轻质弹簧下挂了一个质量为m的小球,将小球从弹簧原长位置由静止开始释放,则小球从最高点运动到最低点的过程中 ( )
17.如图所示,轻质弹簧下挂了一个质量为m的小球,将小球从弹簧原长位置由静止开始释放,则小球从最高点运动到最低点的过程中 ( )
A.速度先增大后减小
B.加速度一直增大
C.小球在最低点时弹簧的弹力大小为2mg
D.弹簧弹力对小球一直做负功
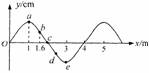 18.如图所示是一列简谐横波在t=0时刻的波形图. 质点c在t=3s时第1次到达波峰,此时质点e恰好在平衡位置且向下运动,则下列说法正确的是 ( )
18.如图所示是一列简谐横波在t=0时刻的波形图. 质点c在t=3s时第1次到达波峰,此时质点e恰好在平衡位置且向下运动,则下列说法正确的是 ( )
A.这列波的波速为1m/s,频率为0.25Hz
B.这列波向右传播
C.t=3s时质点d向上运动
D.t=0.4s时b质点恰好回到平衡位置
19. 某同学在研究电容器、电感对恒定电流与交变电流的影响时,采用了如图所示的电路,其中L1、L2是两个完全相同的灯泡,直流电压与交流电压的有效值相等. 把开关拔到3、4,电路稳定后两个灯泡的发光亮度相同,则该同学在下列操作中能观察到的实验现象是
( )
某同学在研究电容器、电感对恒定电流与交变电流的影响时,采用了如图所示的电路,其中L1、L2是两个完全相同的灯泡,直流电压与交流电压的有效值相等. 把开关拔到3、4,电路稳定后两个灯泡的发光亮度相同,则该同学在下列操作中能观察到的实验现象是
( )
A.当开关拔到1、2,稳定后L1亮、L2不亮
B.当开关拔到1、2,稳定后L1、L2的发光亮度相同
C.当开关拔到3、4瞬间,L1立即变亮,而L2慢慢变亮
D.当开关拔到3、4瞬间,L2立即变亮,而L1慢慢变亮
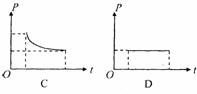
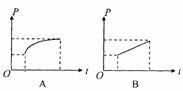
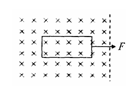 20.如图所示,一个长方形的金属线框电阻为R,放在光滑的水平面上,有界匀强磁场的方向垂直于水平面向下. 线框在水平恒力F的作用下由静止开始向右运动,在线框离开磁场的过程中,拉力F的功率随时间变化的图象不可能的是
( )
20.如图所示,一个长方形的金属线框电阻为R,放在光滑的水平面上,有界匀强磁场的方向垂直于水平面向下. 线框在水平恒力F的作用下由静止开始向右运动,在线框离开磁场的过程中,拉力F的功率随时间变化的图象不可能的是
( )
 21.如图所示为静止在光滑水平面上的质量为M的小车,小车上AB部分是半径为R的四分之一光滑圆弧,BC部分是粗糙的平面. 今把质量为m的小物块从A点静止释放,m与BC分部间的动摩擦因数为μ,最终小物块与小车相对静止于B、C之间的D点,则下列关于BD间距离x的说法正确的是 ( )
21.如图所示为静止在光滑水平面上的质量为M的小车,小车上AB部分是半径为R的四分之一光滑圆弧,BC部分是粗糙的平面. 今把质量为m的小物块从A点静止释放,m与BC分部间的动摩擦因数为μ,最终小物块与小车相对静止于B、C之间的D点,则下列关于BD间距离x的说法正确的是 ( )
A.其他量不变,μ越大,x越大
B.其他量不变,m越大,x越大
C.其他量不变,R越大,x越大
D.其他量不变,M越大,x越大
|
 22.(18分)(1)据图完成下列实验题。
22.(18分)(1)据图完成下列实验题。
用螺旋测微器测量电阻丝的直径,结果如图甲所示,其读数为 mm;某同学用图乙所示装置研究重物的自由落体的运动规律,得到图丙所示的一段纸带,若他测得AB间的距离为s1,BC间的距离为s2,打点计时器打点的时间间隔为T,则打B点时重物的瞬时速度计算式为v= .利用该装置测出的加速度值比当地的重力加速度值略小,其主要原因是 .
(2)为了测定一节干电池的电动势和内电阻,现有下列器材:
待测干电池E(电动势约为1.5V,内阻约为1Ω);
电压表V(量程15V,内阻RV=2kΩ);
电流表G(满偏电流2.0mA,内阻rg=150Ω);
电流表A(量程0.6A,内阻未知);
滑动变阻器R1(0~20Ω,2A);
滑动变阻器R2(0~1000Ω,1A);
定值电阻R3=900Ω;
开关和导线若干。
①为了尽量准确地进行测量,也为了操作方便,实验中应选用的滑动变阻器是 .
②请在图甲方框中画出实验电路原理图,并标注上各器材的代号。
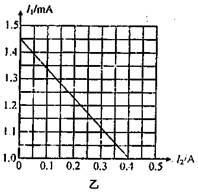 ③图乙为某同学根据正确的电路图进行实验操作以后作出的I1-I2图像(I1为电流表G的示数,I2为电流表A的示数),由该图像可求出被测干电池的电动势E=
V,内电阻r=
Ω(计算结果保留三位有效数字)
③图乙为某同学根据正确的电路图进行实验操作以后作出的I1-I2图像(I1为电流表G的示数,I2为电流表A的示数),由该图像可求出被测干电池的电动势E=
V,内电阻r=
Ω(计算结果保留三位有效数字)
甲
23.(14分)北京航天飞行控制中心在2007年11月5日11时37分对“嫦娥一号”卫星实施了第一次近月制动,成功“刹车”后的卫星被月球捕获,进入了环月轨道。11月6日,第二次近月制动使卫星速度进一步降低,并进入了一个周期为T1的椭圆轨道。11月7日,第三次近月制动后,卫星进入了一个周期为T2、离月球表面高度为h的圆形轨道。“嫦娥一号”将在这条工作轨道上开展时间为T3的探测活动。已知月球的半径是R,试求月球的质量和它的平均密度.
24.(18分)如图所示,在y轴右侧-2L≤y≤2L的带状区域存在着相互垂直的匀强磁场和匀强电场,电场沿y轴正方向,磁场垂直xOy平面向外. 在原点O左侧有一粒子源不断地发射相同的带电粒子,粒子的初速度恒定,射入有场区域后恰好沿x轴正方向做直线运动. 若撤去电场只存在磁场,粒子从b(L,2L)点射出有场区域;若撤去磁场只存在电场,粒子将从a点射出有场区域(不计粒子的重力和粒子间的相互作用).
(1)试判断该粒子带何种电荷?
 (2)求a点的坐标.
(2)求a点的坐标.
25.(22分)一质量m=0.1kg的正方形金属框总电阻R=0.5Ω,金属框从表面绝缘且光滑的斜面顶端(金属框上端与AA′重合)由静止开始沿斜面下滑,下滑过程中穿过一段边界与斜面底边BB′平行、贡度与线框边长相同的匀强磁场后滑至斜面底端(金属线框下边与BB′重合)。设金属框在下滑过程中的速度为v,与其对应的位移为s,整个运动过程的v2-s图像如图所示,已知匀强磁场方向垂直斜面向上,取g=10m/s2.
(1)根据v2-s图像所提供的信息,求斜面的倾角θ和匀强磁场的宽度d;
(2)磁场的磁感应强度为多大?
(3)金属框从斜面顶端滑至底端所需的时间为多少?

|
(1)A和C元素;B和D元素各有相似的化学性质,是因为
。
(2)氧与硫处于同一族,性质相似,对应的化合物也有类似的性质,同时有差异,如:H2O与H2S;CH3CH2OH与CH3CH2SH(乙硫醇)等一定相似性。请回答下列问题:
①已知酸性H2O<H2S,试判断乙醇和乙硫醇分别与金属钠反应的剧烈程度
CH3CH2OH CH3CH2SH(填>、<或=)
②CH3CH2Br不仅能与NaOH溶液反应,而且也能与NaHS溶液反应,则化学反应方程式为: 。
(3)在四种元素中A元素还可能与D元素有相似的化学性质,化学上称为对角线规则。请完成下列反应方程式:(已知:镁可以在氮气中燃烧得到氮化镁)
①Li单质也能在氮气中燃烧,其化学反应方程式为: 。
②铍单质与氢氧化钠溶液反应的离子方程式为: 。
27.(15分)现有A、B、C、D、E五种强电解质,它们在水中可电离产生下列离子(各种离子不重复):H+、Na+、Al3+、Ag+、Ba2+、OH-、Cl-、CO 、NO
、NO 、SO
、SO
已知:
①A、B两溶液呈碱性;C、D、E溶液呈酸性。
②A溶液与E溶液反应既有气体又有沉淀产生;A溶液与C溶液反应只有气体产生(沉淀包括微溶物,下同)。
③D溶液与另外四种溶液反应都能产生沉淀。
④在E溶液中逐滴加入B溶液,溶液先出现沉淀,当滴加至过量时,沉淀部分溶解。
试回答下列问题:
(1)A、C的化学式分别为 、 。
(2)A溶液呈酸性的原因 (用离子方程式表示)。
(3)已知:NaOH(aq)+HNO3(aq)=NaNO3(aq)+H2O(l);△H=-akJ·mol-1(a>0)。请写出C与B的稀溶液反应的热化学方程式 。
(4)在100mL 0.1mol·L-1的E溶液中,逐滴加入35mL 2mol·L-1NaOH溶液,最终得到沉淀的物质的量为 。
28.(15分)工业上生产氯气,常用电解槽中电解饱和食盐水,为了避免电解产物之间发生反应,常用阳离子交换膜将电解槽隔成两部分。下图(左图)为电解槽的示意图。
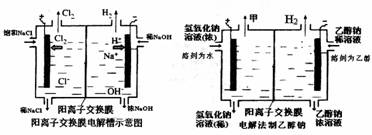
(1)这种阳离子交换膜,只允许溶液中的 通过。(填下列微粒的编号)
①H2 ②Cl2 ③H+ ④Cl- ⑤Na+ ⑥OH-
(2)写出在电解过程中发生的电极方程式
阳极: 。
(3)已知某电解槽每小时加入10%的氢氧化钠溶液10kg,每小时能收集到标况下的氢气896L,而且两边的水不能自由流通。则理论上计算,电解后流出的氢氧化钠溶液的质量分数为 。
(4)某化学课外兴趣小组设计了用电解法制取乙醇钠的工业方法,所用的电解槽如上右图所示,设计要求:①所用的交换膜不能让分子自由通过;②电解过程中消耗的原料是氢氧化钠和乙醇。回答下列问题:
①写出在电解过程中发生的电极方程式
阴极: 。
②最后从乙醇钠的乙醇溶液中分离得到纯净乙醇固体的方法是: 。
29.(15分)某有机化合物A的相对分子质量大于150且小于200。经分析得知,化合物中碳、氢、氧的质量比为:7.5:1.125:3。A具有酸性,是蜂王浆中的有效成分,物质的量为0.0002mol的A需用20.0mL 0.0100mol/L氢氧化钠水溶液来滴定达到滴定终点。
(1)有机化合物A的相对分子质量是 ,该化合物的化学式(分子式)是 。
(2)已知A能使溴的四氯化碳溶液褪色,A发生臭氧化还原水解反应生成B和C,B能发生银镜反应,且能与金属钠或氢氧化钠溶液反应。
信息提示:在一定条件下,烯烃可发生臭氧化还原水解反应,生成羰基化合物,该反应可表示为:

以上反应和B的进一步反应如下图所示。

1molD与适量的碳酸氢钠溶液反应可放出二氧化碳44.8L(标准状况)。若将D与F在浓硫酸作用下加热,可以生成一个化学式(分子式)为C4H4O4的六元环G,该反应的化学方程式是 ,反应类型是 。D与碳酸氢钠反应的化学方程式是 。
(3)经测定,有机化合物C没有支链,分子中没有-CH3。写出有机化合物A的结构简式 。
30.(16分)(一)下图I、Ⅱ、Ⅲ表示高等动植物细胞的部分代谢过程,请据图回答问

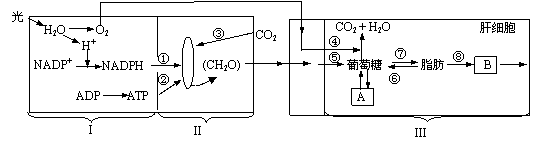
(1)I阶段中生成NADPH的场所为___ ___。I阶段中发生的能量变化是 。
(2)CO2从细胞外到细胞内并参与过程Ⅱ的第一步骤,这一步骤叫做 。如果CO2的供应突然停止,过程Ⅱ中 (物质)会增多。
(3)肝脏是人体非常重要的器官,I、Ⅱ过程生成的糖类通过摄食并消化吸收进入肝细胞后,既可被氧化分解,也可通过⑥形成物质[A] (填名称)。
(4)当膳食糖分过高后,还可发生⑦⑧过程,该过程需要肝细胞合成 (填物质名称)参与方可生成[B] (填名称),运出肝脏,否则会造成脂肪肝。
13.有氧化铁和氧化铜的混合物a g,加入2mol/L的硫酸溶液50mL时,恰好完全溶解。若将这种混合物b g在氢气流中加热并充分反应,冷却后剩余固体的质量为 ( )
A. B.
B. C.
C. D.
D.
11. 对于反应2A(g)+B(g) 2C(g),△H=-akJ/mol,(a>0)下列判断正确的是( )
对于反应2A(g)+B(g) 2C(g),△H=-akJ/mol,(a>0)下列判断正确的是( )
A.2体积A和足量B反应,必定生成2体积C,放出a kJ热量
B.若反应容器的容积和温度不变,增大压强,平衡必定向右移动
C.平衡时,A消耗速度必定等于B生成速度的两倍
D.平衡时,A浓度必定等于B浓度的两倍
 12.MOH和ROH两种碱的溶液分别加水稀释时,pH变化如右图所示。下列叙述中正确的是 ( )
12.MOH和ROH两种碱的溶液分别加水稀释时,pH变化如右图所示。下列叙述中正确的是 ( )
A.MOH是一种强碱
B.在x点,MOH完全电离
C.稀释前,c(ROH)=10c(MOH)
D.在x点,c(M+)=c(R+)
9.有关化学实验的基本操作中,正确的是 ( )
A.配制500mL某物质一定物质的量浓度的溶液,可用两个250mL的容量瓶
B.测定某溶液的pH,将干燥的试纸浸入到待测溶液,过一会儿取出,与标准比色卡比较
C.中和热测定实验中以环形铜丝搅拌棒代替环形玻璃搅拌棒会使测定值比理论值偏低
D.检验亚硫酸钠固体是否变质,先将少量样品溶于水中,再加入酸化的硝酸钡溶液
|
 A.Cl2溶于水:Cl2+H2O 2H++Cl-+ClO-
A.Cl2溶于水:Cl2+H2O 2H++Cl-+ClO-
B.氯化亚铁溶液中加入稀硝酸3Fe2++4H++NO =3Fe3++2H2O+NO↑
=3Fe3++2H2O+NO↑
C.苯酚钠溶液中通入少量的CO2
C6H5O-+CO2+H2O→C6H5OH+CO
|
 +OH-=NH3·H2O
+OH-=NH3·H2O7.用NA表示阿伏加德罗常数的数值,下列说法正确的是 ( )
A.标准状况下,11.2L SO3所含的原子数为2NA
B.标准状况下,22.4L 氧气和乙炔混合物所含的分子数为NA
C.0.2mol过氧化氢完全分解转移的电子数目为0.4NA
D.100mL 2.0mol/L的Na2S溶液中阴离子个数小于0.2NA
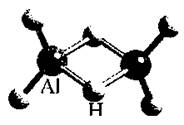 8.科技日报2007年1月30日讯:美、德两国科学家日前成功合成出具有独特化学性质的氢铝化合物(AlH3)n,其结构类似由硼和氢组成的硼烷,有关研究报告发表在最新出版的美国《科学》杂志上。最简单的氢铝化合物为Al2H6,它的熔点为150℃,燃烧热极高。Al2H6球棍模型如右图。下列说法肯定不正确的是 ( )
8.科技日报2007年1月30日讯:美、德两国科学家日前成功合成出具有独特化学性质的氢铝化合物(AlH3)n,其结构类似由硼和氢组成的硼烷,有关研究报告发表在最新出版的美国《科学》杂志上。最简单的氢铝化合物为Al2H6,它的熔点为150℃,燃烧热极高。Al2H6球棍模型如右图。下列说法肯定不正确的是 ( )
A.氢铝化合物可能成为未来的火箭燃料
B.Al2H6在空气中完全燃烧,产物为氧化铝和水
C.Al2H6是离子化合物
D.Al2H6是非极性分子
6.目前环境污染、节能减排问题越来越受到人们的关注,有关环境问题,下列叙述不正确的是 ( )
A.大量使用化石燃料会导致温室效应
B.向燃料煤中加入石灰石,可减少对大气的污染
|
D.在水力发电、火力发电、核能发电和风力发电中,要优先发展火力发电
5.下列有关生物多样性的叙述,正确的是 ( )
A.外来物种的引进,有助于生物多样性的增加
B.种群越大的地区,其生物多样性越大
C.环境污染是我国生物多样性面临威胁的主要原因
D.生物多样性越高的生态系统, 其抵抗力稳定性越高
4.下列关于生物工程相关知识的叙述,正确的项数是 ( )
①植物组织培养过程中愈伤组织的代谢类型是自养需氧型
②B淋巴细胞与骨髓瘤细胞混合,在聚乙二醇的诱导下,融合成的细胞叫做杂交瘤细胞
③若要生产转基因抗病棉花,可将目的基因先导入到土壤农杆菌中,再转入棉花细胞中
④植物体细胞杂交,能克服远源杂交不亲和的障碍,培育出新品种植株
⑤基因治疗是把健康的外源基因导入有基因缺陷的细胞中,达到治疗疾病的目的
⑥在植物体细胞杂交中,可采用质壁分离实验检测制备的原生质体的活性情况
A.2项 B.3项 C.4项 D.5项
3.燕麦颖色的控制涉及两对等位基因。只要有黑色素存在就无法区分有无黄色素,只有在无黑色素的情况下,才能看出有无黄色素。将纯种黑颖燕麦和纯种黄颖燕麦杂交,子一代全为黑颖,子二代共得560株,其中黑颖420株,黄颖105株,白颖35株。则F2黑颖产生的所有配子中不含显性基因的配子所占比例为 ( )
A.1/6 B.1/4 C.1/3 D.1/16
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com