
37.A、B、C、D四种短周期元素,原子序数依次增大;A和C能形成一种分子X或一种+1价阳离子Y;B元素的原子最外层电子数是次外层电子数的2倍;C、D在元素周期表中处于相邻的位置,它们的单质在常温下均为无色气体。试回答下列问题:
(1)A、D元素的名称分别为A D 。
(2)写出Y水解的离子方程式 。
(3)将9g B单质在空气中完全燃烧,将燃烧后的气体缓慢通入1L1 mol·L-1的NaOH溶液中,充分吸收后,最终所得溶液中各离子浓度由大到小的顺序是:
。
(4)在101k Pa时,1gX气体在D单质中充分燃烧,生成一种液态化合物和另一种对环境无污染的稳定物质,放出18.6KJ的热量,该反应的热化学方程式为:
。
[猜题理由]在高考题中通常有两大类:一类是确定“指定几种元素形成化合物”的形式,该类题一般是给出几种元素的原子结构或性质特征,判断它们形成化合物的形式。解此类题的方法思路是:定元素(熟练掌握1-20号元素原子结构示意图或相关的等电子阴阳简单离子,一般出现较多的元素碳、氢、氧、氮、钠、镁、铝,其次是硅、磷、氟、氯、硫、钙),推价态(注意变价、无正价、无负价的特殊元素),想可能(联想中学化学中最常见最典型的物质及化学反应),得化学式(注意化学符号书写的规范);另一类是由“位构性”关系或元素化合物性质推断元素,解该类题的方法思路是:抓住有效的突破口,要灵活运用分析归纳演绎的思维方法,快速准确解答,而且答题时要注意化学用语的规范。
36.有X、Y、Z三种元素,已知:
①X2-、Y-均与Y的气态氢化物分子具有相同的电子数;
②Z与Y可组成化合物ZY3,ZY3溶液遇KSCN溶液呈红色。
请回答下列问题:
(1)Y的最高价氧化物对应水化物的化学式是__________。
(2)将ZY3溶液滴入沸水可得到红褐色液体,反应的离子方程式是____________________。
此液体具有的性质是__________(填字母)。
a.光束通过该液体时形成光亮的“通路”
b.插入电极通直流电后,有一极附近液体颜色加深
c.向该液体中加入硝酸银溶液,无沉淀产生
d.将该液体加热、蒸干、灼烧后,有氧化物生成
(3)X单质在空气中燃烧生成一种无色有刺激性气味的气体。
①已知一定条件下,每1mol该气体被O2氧化放热98.0kJ。若2mol该气体与1mol O2在此条件下发生反应,达到平衡时放出的热量是176.4kJ,则该气体的转化率为__________。
②原无色有刺激性气味的气体与含1.5mol Y的一种含氧酸(该酸的某盐常用于实验室制取氧气)的溶液在一定条件下反应.可生成一种强酸和一种氧化物。若有1.5×6.02×1023个电子转移时,该反应的化学方程式是________________________________。
[猜题理由]元素推断题,经典题型。
35.某矿抽出的废液中含有大量的K+、Cl-、Br-,还有少量的Ca2+、Mg2+、SO42-。某研究性学习小组所拟取这种废液来制取较纯净的氯化钾晶体及液溴(Br2),他们设计了如下流程:

可供试剂a、b的选择试剂:饱和Na2CO3溶液、饱和K2CO3溶液、KOH溶液、BaCl2溶液、Ba(NO3)2溶液、H2O2、KMnO4(H+)溶液、稀HNO3。
请根据以上流程,回答相关问题:
(1)试剂a应该选用_______________;
(2)操作①、②、③、④、⑤的名称是_________(填字母)。
A.萃取、过滤、分液、过滤、蒸发结晶 B.萃取、分液、蒸馏、过滤、蒸发结晶
C.分液、萃取、过滤、过滤、蒸发结晶 D.萃取、分液、分液、过滤、蒸发结晶
(3)除去无色液体I中的Ca2+、Mg2+、SO42-离子,选出C所代表的试剂,按滴加顺序依次是 (填化学式)。
(4)调节pH的作用是 ,操作方法是 。
(5)操作⑤中用到的瓷质仪器名称是 。
[猜题理由]2010年化学考纲对化学实验与探究能力的要求:了解并初步实践化学实验研究的一般过程,掌握化学实验的基本方法和技能。课改省份更要求重视学生的实验操作能力,本题综合考查了高中化学的的混合物的分离与提纯的方法,是考查学生基本实验能力的一道好题。
34.自洁面料就是在普通的面料纤维中加入一层薄薄的纳米二氧化钛。含有Fe2O3的钛铁矿(主要成分为FeTiO3)制取纳米级TiO2的流程如下:

(1)Ti的原子序数为22,Ti位于元素周期表中的第________周期,第______族。
(2)步骤①加铁的目的是_________________;步骤②冷却的目的是_______________。
(3)上述制备二氧化钛的过程中,可以利用的副产物是______________;考虑成本和废物综合利用因素,废液中应加入___________________处理。
(4)由金红石制备单质钛,涉及到的步骤为:
TiO2 TiCl4
TiCl4 Ti
Ti
已知:①C(s)+O2(g)==CO2(g) △H= -393.5kJ·mol-1
②2CO(g)+O2(g)==2CO2(g) △H= -5665kJ·mol-1
③TiO2(s)+2Cl2(g)==TiCl4(s)+O2(g) △H= +41kJ·mol-1
则TiO2(s)+ 2Cl2(g)+C(s)==TiCl4(s)+2CO(g)的△H=____________。
反应TiCl4+2Mg == 2MgCl2+Ti 在氩气氛中进行的理由是________________________。
[猜题理由]用框图形式给出工业生产流程,让考生面对自己观察框图,获取所需信息解决问题,这类试题体现了新课程改革的方向。试题有一定难度,考查吸收信息、处理信息等综合分析能力。
33.

请根据上述流程回答下列问题:
(1)试剂A可选用_____(填字母)。
a.稀H2SO4 b.浓H2SO4 c.浓FeCl3溶液 d.浓HNO3
(2)第②步加入H2O2溶液发生的反应的离子方程式为:_____________________________。
(3)第③步中所加试剂B为________(填化学式)。调节溶液的pH合适的范围是__________。
(4)操作⑤通常加H2SO4调节pH=1是为了:______________________________________。
(5)本流程中多次用到过滤操作,该操作主要用到的玻璃仪器为: _______________,操作⑥的主要步骤为: 、 。
(6)某同学认为上述流程中所加的试剂A并不理想,需作改进,其理由是______________
__________________________________________________________。请你帮助提出一条改进方案____________ 。
[猜题理由]本题来源于真实的化工工艺,废旧电器的综合得用。以废旧铜器为原料,制备重要工业用盐胆矾为主线,综合考查元素化合物的性质、离子反应、沉淀的生成和溶解、过滤、溶液酸碱性(pH)的应用、盐类水解、重结晶等基础知识;考查学生调控化学实验条件的能力、观察和分析图表的能力。
该类试题特点是极具上海和广东特色的高考题,试题起点高、结构新颖,工业背景的题材多、提问灵活,该类题符合考纲“能够从试题提供的新信息中,准确地提取实质性内容,……的能力”。 通常以选修2《化学与技术》中介绍的工业流程为载体,代替传统的无机框图题,将元素化合物知识放置在真实的化学工业环境中,从而达到考查同学们的综合分析问题的能力以及将新信息和已有信息整合,重组为新信息块的能力。是新课改区高考题的一大亮点。已成为课改省份必考题型之一。
32.2009年12月7日-18日在丹麦首都哥本哈根召开了世界气候大会,商讨《京都议定书》一期承诺到期后的后续方案,即2012年至2020年的全球减排协议,大会倡导“节能减排” 和“低碳经济”,降低大气中CO2的含量及有效地开发利用CO2,引起了各国的普遍重视。过渡排放CO2会造成“温室效应”,科学家正在研究如何将CO2转化为可利用的资源。目前工业上有一种方法是用CO2来生产燃料甲醇。一定条件下发生反应:
 CO2(g)+3H2(g)
CO2(g)+3H2(g) CH3OH(g)+H2O(g),下图表示该反应过程中能量(单位为kJ·mol-1)的变化:
CH3OH(g)+H2O(g),下图表示该反应过程中能量(单位为kJ·mol-1)的变化:
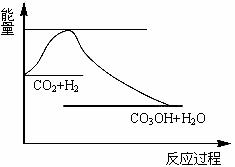
(1)关于该反应的下列说法中,正确的是____________(填字母)。
A.△H>0,△S>0 B.△H>0,△S<0
C.△H<0,△S<0 D.△H<0,△S>0
 (2)为探究反应原理,现进行如下实验,在体积为l L的密闭容器中,充入l mol CO2和3 mol H2,一定条件下发生反应:CO2(g)+3H2(g)
(2)为探究反应原理,现进行如下实验,在体积为l L的密闭容器中,充入l mol CO2和3 mol H2,一定条件下发生反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g),经测得CO2和CH3OH(g)的浓度随时间变化如图所示。
CH3OH(g)+H2O(g),经测得CO2和CH3OH(g)的浓度随时间变化如图所示。
① 从反应开始到平衡,CO2的平均反应速率v(CO2) = 。
② 该反应的平衡常数表达式K= 。
③ 下列措施中能使化学平衡向正反应方向移动的是 (填字母)。
A.升高温度
B.将CH3OH(g)及时液化抽出
C.选择高效催化剂
D.再充入l molCO2和3 molH2
(3)25℃,1.01×105Pa时,16g 液态甲醇完全燃烧,当恢复到原状态时,放出369.2kJ的热量,写出该反应的热化学方程式:___________________________________________。
(4)选用合适的合金为电极,以氢氧化钠、甲醇、水、氧气为原料,可以制成一种以甲醇为原料的燃料电池,此电池的负极应加入或通入的物质有__________ _____;其正极的电极反应式是:_____________________________________。
[猜题理由]化学高考试题中的信息题常常和时事联系很紧密。比如说,1998年山西朔州发生假酒案,当年的全国化学高考题就考了有关甲醇的试题;1999年,我国许多城市禁止汽车使用含铅汽油,当年在全国化学高考试题中考查了有关试题;现代战争中常常用到石墨炸弹。石墨炸弹爆炸时能在方圆几百米范围内撤下大量石墨纤维,造成输电线、电厂设备损坏。1999年在全国高考化学试题中考查了有关试题;1999年欧洲的二噁英事件,2000年的全国化学高考题中就出现了有关二噁英的试题;2003年非典事件,2004年考了预防非典的消毒药物过氧乙酸的试题;2005年苏丹红事件,2005年化学高考考查了有关苏丹红的分子结构及有关试题;再比如高考还考了吗啡,海洛因的分子结构及其有关性质。2006年禽流感是影响全球的大事件,在高考中出现了根据治疗禽流感的药物达菲原料莽草酸的结构的试题。2008年的北京奥运会,又出了祥云火炬的燃料丙烷方面的试题等等。
现在的环境污染问题越来越受到全世界人们的关注和担忧,2009年12月7日-18日在丹麦首都哥本哈根召开了世界气候大会,商讨《京都议定书》一期承诺到期后的后续方案,即2012年至2020年的全球减排协议,大会倡导“节能减排” 和“低碳经济” 的绿色环保主题。 中国宣布了2020年二氧化碳排放量下降40-45%的减排目标,在这一目标的鼓舞下,低碳生活将逐渐成为时代的新时尚,为此我编写此题,预想在2010年的高考试卷中会有体现。
图像类试题一直在高考试题中保留,并且今后还会继续保留。这类题型能够考查学生对图形图像的抽象、概括和分析能力,对图像数据的处理能力。另处,预计今年电化学、化学平衡常数、反应热和熵变的判断将成为某些地区考题的热点,特别是第一届新课标高考的省区,故笔者在设计试题时安排了上述的内容。
30.0.01mol的Na2CO3加入pH=1的100ml H2SO4溶液中,充分反应后向混合液中加入1.22g的BaCl2·xH2O,Ba2+恰好完全沉淀,则x的值是( )
A.8 B.6 C.4 D.2
[猜题理由]化学计算能更好的考查学生的分析问题,解决问题的能力。本题学生只有分析清楚了反应的实际过程才能顺利的得出答案。
29.等量的Na和Al两种金属加入足量的水中,生成26.88L(标准状况下)的气体,则下列描述错误的是( )
A.金属 Al无剩余 B.c (Na+)=c(AlO2-)
C.所得溶液呈碱性 D.Na的物质的量是0.6mol
[猜题理由]Na和Al是中学化学常见的金属,Na具有典型的金属性,Al具有典型的过渡性,另外电子守恒计算也是中学化学的重要内容。
28.在所给的四种溶液中,各种离子能在原溶液中大量共存并形成无色溶液的是( )
A.在c(H+)=10-13mol/L的溶液中:NH4+、Al3+、Fe3+、NO3-
B.pH值为1的溶液:Cu2+、Na+、Mg2+、NO3-
C.水电离出来的c(H+)=10-3mol/L的溶液:K+、HCO3-、Br-、Ba2+
D.溶有NaHSO4的溶液中:K+、SO42-、NO3-、Al3+
[猜题理由]离子共存问题是高考中的常见题型,几乎是每年必考的题型。命题的趋势是:(1)增加限制条件,如强酸性、无色透明、碱性、pH=1、甲基橙呈红色、发生氧化还原反应等;(2)定性中有定量,如:由水电离的c(H+)=10-12mol·L-1的溶液中等等。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com