
17. 某科学家提出了年轻热星体中核聚变的一种理论,其中的两个核反应方程为


方程式中Q1、Q2表示释放的能量,相关的原子核质量见下表:
|
原子核 |
 |
 |
 |
 |
 |
 |
|
质量/u |
1.0078 |
3.0160 |
4.0026 |
12.0000 |
13.0057 |
15.0001 |
则 A.X是 ,Q2>Q1 B.X是
,Q2>Q1 B.X是 ,Q2>Q1
,Q2>Q1
C.X是 ,Q2<Q1 D.X是
,Q2<Q1 D.X是 ,Q2<Q1
,Q2<Q1
16.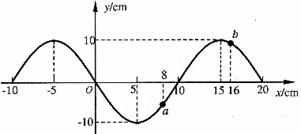 一列简谐横波沿X轴负方向传播,周期为0.2s,某时刻波形如图所示,介质中质点a、b的平衡位置距原点0的距离分别是8cm和16cm,则该时刻有
一列简谐横波沿X轴负方向传播,周期为0.2s,某时刻波形如图所示,介质中质点a、b的平衡位置距原点0的距离分别是8cm和16cm,则该时刻有
A.a质点正在沿y轴的正方向运动
B.b质点的加速度方向沿y轴的正方向
C.该波的波速为1 m/s,故经t=0.08s,
b质点在平衡位置且沿y轴的负方向运动
D.从该时刻起,第一次质点 a的运动状态与该时刻质点b的运动状态相同时,所经历的时
间为t=0.08s
15.2008年9月26日4时04分,“神舟七号”由原来的椭圆轨道最远点变为距地面高度为h(约340 km)的圆形轨道运行.已知飞船的质量为m,地球半径为R,地面处的重力加速度为g,地球自转的角速度为ω,则下列说法正确的是 ( )
A.飞船在圆轨道上运动时,航天员将不受重力作用
B.飞船做匀速圆周运动时,运行速度等于7.9km/s
C.飞船由椭圆轨道变为圆形轨道时,需要在椭圆的远地点处使飞船加速
D.飞船在圆轨道上运动时的动能EK满足 mω2(R+h)2<EK<
mω2(R+h)2<EK< mg(R+h)
mg(R+h)
14.如图一端开口的钢制圆筒在开口端放一活塞,且活塞与筒壁的摩擦及活塞的重量均可不计,现将圆筒开口向下竖直倒立于水中,筒底恰与水面相平时筒静止,若水温逐渐升高时,下列说法中正确的是 ( )
 A.活塞会下移,但筒不动
A.活塞会下移,但筒不动
B.筒会上升,但活塞不动
C.筒内气体体积增大,压强减小
D.筒内气体压强增大,温度升高
13、下列各组离子能在指定溶液中大量共存的是( )
① 含有HCO的溶液中:SO,Na+,NO,MnO,CO
② 水电离的H+浓度为1×10-13mol·L-1的溶液中:Cl-,HCO,NO,NH,S2O
③ 加入Al能放出H2的溶液中:Mg2+,NO3-,C1-,K+,SO
④ 在AlCl3溶液中:NH,NO、I-,Cl-,SO,CO
A. ① ② ③ ④ B. ① C. ① ③ D. ① ② ④
12、锕系元素钍(Th)原子可蜕变为另一元素的原子,并释放出a粒子, →Z+
→Z+ ,关于Z元素的下列推论正确的是
,关于Z元素的下列推论正确的是
A Z的硫酸盐难溶于水
B Z是超铀元素,具有放射性
C Z的最高价氧化物对应的水化物呈酸性
D Z单质不能与水反应
11、下列对有关实验操作、现象或结论的描述正确的是
A 在250mL烧杯中,加入216mL水和24gNaOH固体,配制10%NaOH溶液
B 在 “硫酸铜晶体中结晶水含量的测定”实验操作中至多需要四次称量
C 用酸式滴定管量取用98%,密度为1.84 g/cm3的浓H2SO4配制200mL 2 mol·L-1的稀H2SO4时,先平视后仰视,所得溶液的浓度将偏大
D为测定含有氯化钠的氢氧化钠混合物中氯化钠的含量,采用标准盐酸滴定法,若滴定前滴定管中有气泡滴定后消失,则导致最终测定值偏低
10、已知NO2与N2O4相互转化:2NO2(g)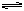 N2O4(g);△H=-24.4kJ/mol在恒温下,将一定量NO2和N2O4(g)的混合气体充入体积为2L的密闭容器中,其中物质的浓度随时间变化
N2O4(g);△H=-24.4kJ/mol在恒温下,将一定量NO2和N2O4(g)的混合气体充入体积为2L的密闭容器中,其中物质的浓度随时间变化
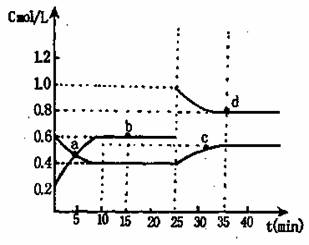 的关系如右图。下列推理分析合理的是 ( )
的关系如右图。下列推理分析合理的是 ( )
A.前10min内,用v(NO2)表示的该反
应速率为0.02mol/L·min
B.反应进行到10min时,体系吸收的热量
为9.76kJ
C.a,b,c,d四点中v正与v逆均相等
D.25min时,导致平衡移动的原因是升温
9、下列溶液中有关微粒的物质的量浓度关系正确的是
A、常温下将醋酸钠、盐酸两溶液混合后,溶液呈中性,则混合后的溶液中:
c(Na+)>c(Cl-)> c(CH3COOH)
B、等物质的量浓度等体积的硫化钠溶液与硫酸氢钾溶液混合
C(Na+)> C(K+)> C(SO42-)> C(HS-)> C(OH-)>C(H+)
C、用pH=3和pH=2的醋酸溶液中和含等量NaOH的溶液所消耗的醋酸溶液的体积分别为Va和Vb,则Va>10Vb
D、pH <7的某二元弱酸的酸式盐NaHA溶液中有c(H+)+2 c(A2-)==c(OH-) +c (H2A)
8、如下图所示的装置,C、D、E、F、X、Y都是惰性电极。将电源接通后,向乙中滴入酚酞溶液,在F极附近显红色。则以下说法正确的是( )
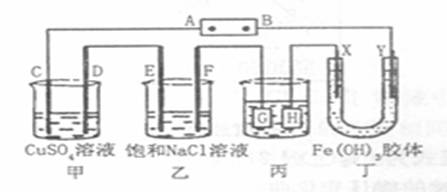
A 电源B极是正极
B 甲乙装置的C、D、E、F电极均有单质生成,其物质的量之比为1:2:2:2
C 欲用丙装置给铜镀银,H应该是银,电镀液是AgNO3溶液
D 装置丁中看到的现象是X极附近红褐色变深
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com