
15、同学们从山上采集到一种石灰石,他们取80克该样品进行煅烧实验(所含杂质
在煅烧过程中不发生变化),测得反应后固体的质量(m)与反应时间(t)的关系如下表:
|
反应时间t∕s |
t0 |
t1 |
t2 |
t3 |
t4 |
t5 |
t6 |
|
反应后固体的质量m∕g |
80 |
75 |
70 |
66 |
62 |
58 |
58 |
请回答下列问题:
(1)当石灰石完全反应后,生成CO2的质量为 g。
(2)求该石灰石中CaCO3的质量分数,写出计算过程。
(3)请在下面坐标图中,画出煅烧时生成气体的质量(m)随时间(t)变化的曲线。
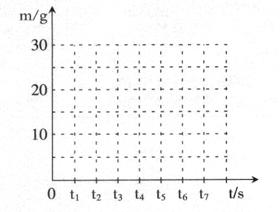
[解析] 本题考查化学方程式的计算的有关知识 根据质量守恒定律可知反应前后固体的变化量为生成二氧化碳气体的质量,80 g -58 g =22 g,然后再根据产生二氧化碳的哦质量求出反应掉的碳酸钙的质量,即可求出石灰石中碳酸钙的质量分数。
[答案] (1)22g
(2)解:设样品中含CaCO3的质量为x

CaCO3 CaO + CO2 ↑
100 44
x 22g
 =
= x =
x = =50g
=50g
石灰石中CaCO3的质量分数=(50g÷80g)×100%=62.5% (1分)
 (3)曲线3分。其中to-t5(气体从0-22g)曲线段正确2分;从t5以后曲线段正确1分。
(3)曲线3分。其中to-t5(气体从0-22g)曲线段正确2分;从t5以后曲线段正确1分。
14、右图是“△△牌发酵粉”的部分信息,课外化学兴趣小组的同学对其进行了如下探究(请你完成相应填空):
 [查阅资料]
[查阅资料]
(1)酒石酸是一种易溶解于水的固体有机酸;
(2)发酵粉能够使面团松软、发泡是因为发酵粉产生了CO2所致;
(3)Na2CO 3受热不分解。
[提出问题]
NaHCO3在发酵粉加水或加热时如何产生CO2?
[猜想]
甲.……
乙.酒石酸与NaHCO3在溶液中反应产生CO2
 丙.NaHCO3加热产生CO2
丙.NaHCO3加热产生CO2
[实验探究]
(1)小明同学取少量NaHCO3粉末于试管中,加入适量水,无气体产生,从而否定了猜想甲,则猜想甲是 。小明又将酒石酸溶液和NaHCO3溶液混合,产生了CO2,从而验证了猜想乙,说明了NaHCO3具有的性质之一是 ;
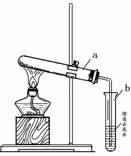
(2)小英同学为探究猜想丙设计了右图所示的实验装置:
小英另取适量NaHCO3粉末加入a试管中,加热,观察到a试管口有水生成,b试管中澄清石灰水变浑浊。b试管中反应的化学方程式为 。
持续加热直至两支试管均不再发生变化时,发现a试管中仍残留有较多白色固体粉末,向该粉末中滴加稀盐酸,有CO2产生,说明该粉末是 。
[小结]
NaHCO3在发酵粉中产生CO2的条件是 ;
NaHCO3受热发生变化的化学方程式为 ;
[解析](1)加入适量水,无气体产生,说明NaHCO3遇水不反应;酒石酸溶液和NaHCO3溶液混合,产生了CO2,说明NaHCO3溶液能能与酸溶液反应;(2)题给信息Na2CO 3受热不分解,向该粉末中滴加稀盐酸,有CO2产生,所以剩余的应是Na2CO 3。
[答案](1)NaHCO3遇水产生二氧化碳,与某些酸反应产生CO2;
(2)Ca(OH)2+CO2=CaCO3↓+H2O;Na2CO3;加水或加热,
2NaHCO3 △ =Na2CO3+CO2↑+H2O。
13、通过海水晾晒可得粗盐,粗盐除NaCl外,还含有MgCl2、CaCl2、Na2SO4

以及泥沙等杂质。以下是制备精盐的实验方案,各步操作流程如下:
(1)在第①步粗盐溶解操作中要用玻璃棒搅拌,作用是 。
(2)第②步操作的目的是除去粗盐中的 (填化学式,下同),第⑥步操作的目的是除去滤液中 。
(3)第⑤步“过滤”操作中得到沉淀的成分有:泥沙、BaSO4、Mg(OH)2、
(填化学式)。
(4)在第③步操作中,选择的除杂的试剂不能用KOH代替NaOH,理由是
。
[解析](1)粗盐溶解操作中用玻璃棒搅拌是为了加快粗盐溶解;(2)因粗盐中含有Na2SO4,第②步操作是加BaCl2的目的是形成BaSO4沉淀,除去溶液中的Na2SO4。在操作步骤③、④中分别加入过量的NaOH、Na2CO3,所以第⑥步加稀盐酸的目的是除去溶液中的NaOH、Na2CO3;(3)因粗盐中含有CaCl2、Na2SO4,所以沉淀中除了泥沙、BaSO4、Mg(OH)2以外,还有CaCO3、BaCO3。(4)在第③步加入过量的NaOH操作中,若选择KOH代替NaOH,会在滤液中引进新的杂质,造成得到精盐不纯。
[答案](1)加快粗盐溶解
(2)Na2SO4 NaOH、Na2CO3
(3)CaCO3、BaCO3
(4)会引进新的杂质KCl
12、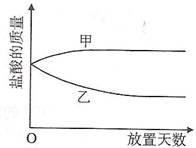 将一定质量的浓盐酸盛于烧杯中,敞口放置在实验室安全之处。
将一定质量的浓盐酸盛于烧杯中,敞口放置在实验室安全之处。
① 浓盐酸的质量和放置天数关系的曲线(见右图)正确的是 (填写“甲”或“乙“)。
② 随着放置天数的增加,浓盐酸的质量发生变化的主要原因是________ _____ ______。
③ 把浓盐酸稀释后可用于去除铁制品表面的铁锈(主要成分为Fe2O3),反应的化学方程式是 。
[解析]浓盐酸有挥发性,由于HCl逸出使盐酸质量减少,所以乙曲线符合题意。
[答案]①乙
②浓盐酸有挥发性,HCl逸出使盐酸质量减少
③6HCl + Fe2O3 === 2FeCl3 + 3H2O
11、程明和王刚不小心将纯碱洒到白醋(其有效成分为醋酸,可用HAc表示)里,发现有大量气泡产生,这使他们对醋酸产生了新认识:醋酸像盐酸一样,能与纯碱反应;此外,他们通过查阅相关资料,还检索到以下信息:①醋酸与盐酸都具有较强挥发性;②醋酸是一种有机酸,具有酸的通性,且其钠盐(NaAc)受热不易分解;③盐酸与纯碱的反应分以下两步进行:
Ⅰ.Na2CO3+HCl===NaHCO3+NaCl;Ⅱ. NaHCO3+HCl===NaCl+H2O+CO2↑
试根据以上信息回答下列问题:
(1)醋酸可以使紫色石蕊试液变 ;
(2)根据信息①可知醋酸应置于阴凉处 保存;
(3)试写出醋酸与纯碱第一步反应的化学方程式: ;
(4)他们向纯碱溶液中滴加醋酸到不再产生气泡后,将所得溶液蒸发结晶,获得了少量白色固体。王刚认为这就是纯净的NaAc,而程明则认为里面含有HAc。你认为 的观点正确,理由是: 。
[解析]HAc属于酸类,具有酸的通性,通过题给信息,可类比HCl写出Na2CO3与Hac反应的第一步化学方程式。
[答案](1)红;
(2)密封
(3)Na2CO3 + HAc== NaHCO3 + NaAc
(4)王刚 由于HAc具有挥发性,在蒸发过程中已经挥发掉
10、有一包化学肥料,可能是硫酸铵、碳酸氢铵、过磷酸钙、氯化钾中的一种。取少量样品,观察到其外观为白色晶体,加水后能全部溶解;另取少量样品与熟石灰混合、研磨,没有刺激性气体放出。这种化肥是( )
A.氯化钾 B.碳酸氢铵 C.硫酸铵 D.过磷酸钙
[解析]过磷酸钙不溶于水,而硫酸铵、碳酸氢铵等铵态氮肥与熟石灰等碱性物质混合会有刺激性气味的氨气放出
[答案]A
9、大理石的主要成分是碳酸钙,在探究大理石性质时,下列有关实验现象和结论的描述中,不正确的是 ( )
A.在大理石的板砖碎片上,滴加稀盐酸有气泡产生
B.大理石与酸反应生成的气体可作灭火剂
C.实验室里可用大理石与稀盐酸来制取二氧化碳
D.大理石雕像不易受酸雨侵蚀
[解析]大理石的主要成分是CaCO3,与盐酸反应产生CO2气体;CO2气体不支持燃烧,也不燃烧,密度比空气大,可用来灭火;大理石雕像容易被酸雨腐蚀。
[答案]D
8、一天,小影惊奇的发现妈妈蒸馒头时用的不是纯碱,而是小苏打,她好奇的问:“为什么不用纯碱而用小苏打?”妈妈说“面团没发酵,不能用纯碱”。通过查阅资料小影发现小苏打的化学式为NaHCO3,是一种常用的膨松剂,加热可转化为纯碱。下列小影相关的推断不合理的是 ( )
A.小苏打是膨松剂是因为能产生二氧化碳气体
B.小苏打受热转化为纯碱是分解反应
C.小苏打属于酸
D.小苏打对人体无害
[解析]小苏打属于盐,受热能转化为纯碱、水和二氧化碳气体。
[答案]C
7、下列有关常见的盐的说法,错误的是 ( )
A.Na2CO3的俗名叫烧碱 B.CaCO3是大理石的主要成分
C.NaCl通常从海水中提取 D.NaHCO3可用于治疗胃酸过多
[解析]Na2CO3的俗名叫纯碱,烧碱是氢氧化钠。大理石的主要成分是CaCO3;海水中有大量的NaCl;NaHCO3能与酸反应,可用于治疗胃酸过多。
[答案]A
6、如图甲、乙两个装置均可通过胶头滴管向锥形瓶中滴加某种液体,达到使气球鼓起起的目的,锥形瓶和胶头滴管放入物质正确的一组是( )
|
序号 |
A |
B |
C |
D |
||||
|
装置名称 |
甲 |
乙 |
甲 |
乙 |
甲 |
乙 |
甲 |
乙 |
|
锥形瓶内物质 |
HCl气体 |
NaCl固体 |
CaCO3 |
固体NaOH |
NH3 |
Cu |
CO2 |
锌粒 |
|
胶头滴管中物质 |
NaOH溶液 |
H2O |
稀盐酸 |
H2O |
H2O |
稀盐酸 |
NaOH溶液 |
稀硫酸 |
[解析] 甲装置气球鼓起,锥形瓶内压强要减小,乙装置气球鼓起,锥形瓶内压强要增大。CO2能与NaOH溶液反应,使乙装置压强减小,锌粒与稀硫酸反应放出氢气,使乙装置压强增大。
[答案]D
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com