
22、 在Fe2(SO4)3溶液中,加入a g Cu,完全溶解后,又加入b g Fe,充分反应后得到c g 残余固体,且a>c,则下列判断不正确的是( )
在Fe2(SO4)3溶液中,加入a g Cu,完全溶解后,又加入b g Fe,充分反应后得到c g 残余固体,且a>c,则下列判断不正确的是( )
A、最后溶液中一定不含Fe3+ B、残余固体可能是Fe、Cu的混合物
C、最后溶液中一定含Fe2+ D、残余固体一定是Cu
21、 下列叙述中错误的或违背化学原理的是
下列叙述中错误的或违背化学原理的是
 A.能形成+7价的含氧酸及其盐的元素不一定是主族元素
A.能形成+7价的含氧酸及其盐的元素不一定是主族元素
 B.等质量的苯和乙烯完全燃烧耗氧量不相等
B.等质量的苯和乙烯完全燃烧耗氧量不相等
 C.用金属钠检验乙醇中是否含有少量水
C.用金属钠检验乙醇中是否含有少量水
 D.“冰,水为之,而寒于水” 说明相同质量的水和冰,水的能量高
D.“冰,水为之,而寒于水” 说明相同质量的水和冰,水的能量高
20、 已知25℃时,AgI饱和溶液中c(Ag+)为1.22×10-8mol/L,AgCl的饱和溶液中c(Ag+)为1.25×10-5mol/L。若在10mL含有KCl和KI各为0.01mol/L的溶液中,加入16 mL0.01mol/LAgNO3溶液,这时溶液中所含溶质的离子浓度大小关系正确的是
已知25℃时,AgI饱和溶液中c(Ag+)为1.22×10-8mol/L,AgCl的饱和溶液中c(Ag+)为1.25×10-5mol/L。若在10mL含有KCl和KI各为0.01mol/L的溶液中,加入16 mL0.01mol/LAgNO3溶液,这时溶液中所含溶质的离子浓度大小关系正确的是
 A.c (K+)>c (NO3-) >c (Ag+) >c (Cl-)>c (I-)
A.c (K+)>c (NO3-) >c (Ag+) >c (Cl-)>c (I-)
 B.c (K+)>c (NO3-) >c (Cl-) >c (Ag+)>c (I-)
B.c (K+)>c (NO3-) >c (Cl-) >c (Ag+)>c (I-)
 C.c (K+)>c (NO3-) >c (Ag+) = c (Cl-) + c (I-)
C.c (K+)>c (NO3-) >c (Ag+) = c (Cl-) + c (I-)
 D. c (NO3-)>c (K+)>c (Ag+) >c (Cl-)>c (I-)
D. c (NO3-)>c (K+)>c (Ag+) >c (Cl-)>c (I-)
19. 下列情况下,可以大量共存的离子组是
下列情况下,可以大量共存的离子组是
 A. 存在大量AlO2-的溶液中:Fe2+、NO3-、SO42-、Na+
A. 存在大量AlO2-的溶液中:Fe2+、NO3-、SO42-、Na+
 B. 由水电离的c(H+) = 1×10-14 mol·L-1的溶液中:Ba2+、K+、Cl-、HCO3-
B. 由水电离的c(H+) = 1×10-14 mol·L-1的溶液中:Ba2+、K+、Cl-、HCO3-
 C. 与铝反应放出大量氢气的溶液中:NH4+、SO42-、CO32-、Na+
C. 与铝反应放出大量氢气的溶液中:NH4+、SO42-、CO32-、Na+
 D. 在c(H+)/ c(OH-)=1012的溶液中:NH4+ 、Al3+、Ca2+、Cl-
D. 在c(H+)/ c(OH-)=1012的溶液中:NH4+ 、Al3+、Ca2+、Cl-
18. 能使H2O
能使H2O 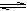 H+ +
OH-电离平衡向电离方向移动,而且所得溶液显酸性的是( )
H+ +
OH-电离平衡向电离方向移动,而且所得溶液显酸性的是( )
 A.将水加热到99℃,使水的pH=6.1 B.向水中滴入稀H2SO4
A.将水加热到99℃,使水的pH=6.1 B.向水中滴入稀H2SO4
 C.向水中加入NaHCO3固体
D.向水中加入AlCl3固体
C.向水中加入NaHCO3固体
D.向水中加入AlCl3固体
17. 设NA为阿伏加德罗常数,下列说法正确的是
设NA为阿伏加德罗常数,下列说法正确的是
 A、18g水中含有的电子数为8NA
A、18g水中含有的电子数为8NA
 B、某气体含有3.01×1023个分子,则该气体所占的体积为11.2 L
B、某气体含有3.01×1023个分子,则该气体所占的体积为11.2 L
 C 、1 L
0.5mol·L-1CuSO4溶液中含有3.01×1023个Cu2+
C 、1 L
0.5mol·L-1CuSO4溶液中含有3.01×1023个Cu2+

 D、2.3g
Na在足量的O2中完全燃烧和与在空气中缓慢反应完全,转移的电子数均为0.1NA
D、2.3g
Na在足量的O2中完全燃烧和与在空气中缓慢反应完全,转移的电子数均为0.1NA
16、 在密闭容器中进行如下反应:X2(g)+Y2
在密闭容器中进行如下反应:X2(g)+Y2 2Z(g),已知X2、Y2、Z的起始浓度分别为0.1mol/L、0.3mol/L、0.2mol/L,在一定条件下,当反应达到平衡时,各物质的浓度有可能是
( )
2Z(g),已知X2、Y2、Z的起始浓度分别为0.1mol/L、0.3mol/L、0.2mol/L,在一定条件下,当反应达到平衡时,各物质的浓度有可能是
( )
 A.Z为0.3mol/L B.Y2为0.4mol/L
A.Z为0.3mol/L B.Y2为0.4mol/L
 C.X2为0.2mol/L D.Z为0.4mol/L
C.X2为0.2mol/L D.Z为0.4mol/L
15. 下列说法中正确的是
( )
下列说法中正确的是
( )
 A.化学反应中反应产物的总能量低于反应物的总能量一定是吸热反应
A.化学反应中反应产物的总能量低于反应物的总能量一定是吸热反应
 B、Ba(OH)2·8H2O与NH4Cl的反应是吸热反应
B、Ba(OH)2·8H2O与NH4Cl的反应是吸热反应
 C、由等体积、等物质的量浓度的一元酸跟氢氧化钠溶液混合后所形成的溶液一定呈中性
C、由等体积、等物质的量浓度的一元酸跟氢氧化钠溶液混合后所形成的溶液一定呈中性
 D、已建立化学平衡的可逆反应,当改变条件使化学反应向正反应方向移动时,反应物转化率一定增大
D、已建立化学平衡的可逆反应,当改变条件使化学反应向正反应方向移动时,反应物转化率一定增大
14.下列现象或反应的原理解释正确的是

13. 金属镍有广泛的用途。粗镍中含有少量杂质Fe、Zn、Cu、Pt,可用电解法制备高纯度的镍(已知:氧化性Fe2+<Ni2+<Cu2+),下列叙述正确的是
金属镍有广泛的用途。粗镍中含有少量杂质Fe、Zn、Cu、Pt,可用电解法制备高纯度的镍(已知:氧化性Fe2+<Ni2+<Cu2+),下列叙述正确的是
 A.阳极发生还原反应,其电极反应式:Ni2+ + 2e- = Ni
A.阳极发生还原反应,其电极反应式:Ni2+ + 2e- = Ni
 B.电解后,电解槽底部的阳极泥中只有Cu和Pt
B.电解后,电解槽底部的阳极泥中只有Cu和Pt
 C.电解后,溶液中存在的阳离子只有Fe2+ 和Zn2+
C.电解后,溶液中存在的阳离子只有Fe2+ 和Zn2+
 D.电解过程中,阳极质量的减少与阴极质量的增加相等
D.电解过程中,阳极质量的减少与阴极质量的增加相等
|
|
现象或反应 |
原理解释 |
|
A. |
铝箔在酒精灯火焰上加热熔化但不滴落 |
铝箔对熔化的铝有较强的吸附作用 |
|
B. |
合成氨反应需在高温条件下进行 |
该反应为吸热反应 |
|
C. |
镀层破损后,镀锡铁比镀锌铁易腐蚀 |
锌比铁活泼,铁锡活泼 |
|
D. |
测定某地区雨水的pH为5.6 |
该雨水一定溶解了SO2 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com