
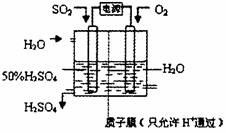
24.(15分)高温裂解法处理工业废硫酸的流程图如下:

废硫酸高温裂解的基本原理可用下列方程按两个阶段进行
H2SO4(1) SO3(g)+H2O(g)△H=+176kJ·mol-1
SO3(g)+H2O(g)△H=+176kJ·mol-1
 2SO3(g)
2SO2(g)+O2(g) △H=+196k·mol-1
2SO3(g)
2SO2(g)+O2(g) △H=+196k·mol-1
为研究废硫酸的雾化和裂解情况,有关实验数据如下
|
|
雾化后废硫酸液滴直径 |
废硫酸完全裂解所需时间 |
|
普通雾化器 |
800-1200/μm |
10 s以上 |
|
旋转式雾化器 |
600-850 μm |
8-10 s |
|
压缩风雾化器 |
400-650 μm |
6-7 s |
|
超声波雾化器 |
100-300μm |
3.5-5 s |
(1)由上表数据可得出的结论是 ;
(2)废硫酸裂解成SO2总反应的热化学方程式为 ;
(3)在催化氧化室中发生反应:
 2SO2(g)+O2(g)
2SO3(g)△H=-196 kJ·mol-1
2SO2(g)+O2(g)
2SO3(g)△H=-196 kJ·mol-1
①某温度时,该反应的平衡常数K=3.5,平衡后再充人一定量气体测得。100 L的恒容密闭容器中含有3.0molSO2,16.0 mol O2和3.0 mol SO3(g),此时平衡 移动;(填“向正反应方向”、“向逆反应方向”或“不”)
②上述反应达到平衡后,改变下列条件,能使SO:平衡浓度比原来减小的是 ;(填字母)
A.保持温度和容器体积不变,充人1.0molO2
B.保持温度和容器内压强不变,充人3.0molN2
 C.降低温度
C.降低温度
D.在其他条件不变时,缩小容器的容积
(4)尾气SO2用饱和Na2SO3溶液吸收可得到
一种化工原料,反应的化学方程式为
(5)科学家研究出以右图所示装置用电化学原
理生产硫酸的新工艺,其阳极的电极反应
式为 ,总反应的化学方程式
为 。
23.(15分)
甲、乙、丙三种物质都含有A元素,只有甲是单质,其转化关系如下:

(1)若乙是目前世界倡导需减少排放的温室
气体,丁也含有A元素。则含有7个中
子的核素A可用符号表示为 ,丙溶液呈碱性的原因用离子方程式表示为 ;
(2)若A是非金属元素,其次外层电子是最外层电子数的2倍,则乙在现代通讯中可用于制造 写出一个有丙参加的、能证明碳的非金属性强于A的化学方程式 ;
(3)若甲是生活中最常用的过渡金属单质,其在点燃条件下与氧气反应生成乙。若丁是稀硝酸,则乙一丙的化学方程式为 ;
(4)若A元素是第三周期元素,其最高正化合价与负价的绝对值差为4,则乙的化学式为 ,当丁是Ca(OH)2时,往丙中加人碳酸钠溶液,当碳酸钠溶液浓度大于 mol·L1时,丙可转化为碳酸钙。(已知此温度下,丙物质Ksp=1×10-6,CaCO3的Ksp=1×10-8)
21.(19分)
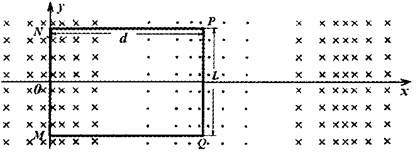
如图所示,在y≥0的区域内存在垂直于坐标平面向里的匀强磁场,磁感应强度大小为B;水平虚线MN、PQ区域内有水平向右电场强度的大小的匀强电场。半径为R的光滑绝缘空心半圆细管AD0固定在竖直平面内,圆心O,在MN上,直径AO垂直于MN。一质量为m、电荷量为q的带正电小球(可视为质点)从半圆管的A点由静止滑人管内,重力加速度为g。求:
(1)小球从A到0点的过程中,电场力对带正电小球所做的功。
(2)小球到达0点时,对半圆管的作用力大小。
(3)若小球从D点射出后,能穿过电场区域再次经过y轴,则电场区域的高度H应大于多少。

 22.(20分)
22.(20分)
磁悬浮铁路系统是一种新型的交通运输系统,它是利
用电磁系统产生的吸引力或排斥力将车辆托起,使整个列
车悬浮在导轨上。同时利用电磁力进行驱动。采用直线电
机模式获得驱动力的列车可简化为如下情景:固定在列车
下端的矩形金属框随车平移;轨道区域内存在垂直于金属
框平面的磁场,磁感应强度沿Ox方向按正弦规律分布,
最大值为B0,其空间变化周期为2d,整个磁场以速度v1沿ox方向向前高速平移,由于列车沿Ox方向匀速行驶速度v2与磁场平移速度不同,而且v1>v2,列车相对磁场以v1- v2的速度向后移动切割磁感线,金属框中会产生感应电流,该电流受到的向前安培力即为列车向前行驶的驱动力。设金属框电阻为R,长PQ=L,宽NP=d,求:
 (1)如图为列车匀速行驶时的某一时刻,MN、
(1)如图为列车匀速行驶时的某一时刻,MN、
PQ均处于磁感应强度最大值处,此时金
属框内感应电流的大小和方向。
(2)列车匀速行驶s距离的过程中,矩形金属
线框产生的焦耳热。
(3)列车匀速行驶时所获得的最大驱动力的大
小,并定性四出驱动力功率随时间变化在 时间内的关系图线。
时间内的关系图线。
20.(15分)
研究性学习小组在探究某球竖直向上运动过程中,通过位移传感器测得该球运动的高度与时间关系(从抛出时开始计时)如图所示。设运动过程所受的空气阻力大小保持不变,为简化计算g取l0m/s。,求:
(1)小球抛出的初速度。
(2)小球下落的加速度。
(3)从最高处落回到抛出点的时间。

19.(18分)
为了探究能量转化和守恒规律,某学习研究小组设计如图1所示装置进行实验。
(1)为了测定整个过程电路产生的焦耳热,需要知道螺线管线圈的电阻。用替代法测线圈电阻Rx的阻值可用如图2所示电路,图中R5为电阻箱(R5的最大阻值大于待测电阻尺Rx的阻值),S2为单刀双掷开关,R0为滑动变阻器。为了电路安全,测量前应将滑动变阻器的滑片P调至 ,电阻箱R5阻值应调至 (选填“最大”或“最小”)。闭合S1开始实验,接下来有如下一些操作,合理的次序是 (选填字母代号):
A.慢慢移动滑片P使电流表指针变化至某一适当位置
B.将S2闭合在1端
C.将S2闭合在2端
D.记下电阻箱上电阻读数
E.调节电阻箱R5的值,使电流表指针指在与上一次指针位置相同
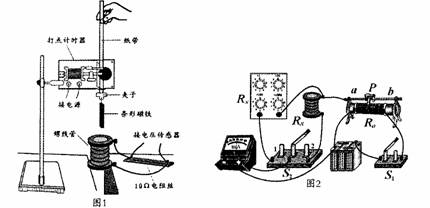
(2)按图l所示装置安装实验器材后,将质量为0.50kg蝇的条形磁铁拖一条纸带由静止释放,利用打点计时器打出如图3所示的纸带。磁铁下落过程中穿过空心的螺线管,螺线管与10Ω的电阻丝接成闭合电路,用电压传感器采集数据得到电阻两端电压与时间的U – t 图,并转换为U 2– t,如图4所示。

①经分析纸带在打第14点时,条形磁铁已经离线圈较远了,打第14点时磁铁速度为 米/秒。0-14点过程中,磁铁的机械能损失为 焦耳。
②若螺线管线圈的电阻是90fl,又从图4中扩一‘图线与时间轴所围的面积约为103格,可以计算磁铁穿过螺线管过程中,在回路中产生的总电热是 焦耳。

③实验结果机械能损失与回路中电流产生的热量相差较大,试分析其原因可能有
16.如图所示,将截面为正方形的真空腔abcd放置在一匀强磁场中,磁场方 向垂直纸面向里.若有一束具有不同速率的电子由小孔a沿ab方向射入磁场,打在腔壁上的被吸收,则关于由小孔c和小孔 d射出的电子的时间比值和运动速率比值正确的是 ( )
 A.
A. B.
B.
C. D.
D.
 17.如图所示,A、B两点各放有电量为+Q和+2Q的点电荷,
17.如图所示,A、B两点各放有电量为+Q和+2Q的点电荷,
A、B、C、D四点在同一直线上,且 。
。
将一正电荷从c点沿直线移到D点,则 ( )
A.电势能始终增加 B.电势能始终减少
C.电场力先做正功再做负功 D.电场力先做负功再做正功
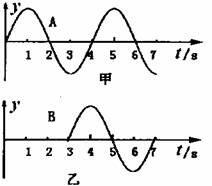 18.在置轴上有A、B两质点,其坐标分别是
18.在置轴上有A、B两质点,其坐标分别是
 ,有一简谐波沿X正
,有一简谐波沿X正
方向传播,若以波传到A点开始计时,A,
B的振动分别如图甲、乙所示。则10秒末,
有关质点振动情况以下说法正确的是( )
A.质点B经过平衡位置
B.质点A速度方向为正方向
C.X=55m的质点在负最大位移处
D.X=30m的质点经平衡位置向上运动
第Ⅱ卷
必考部分
第Ⅱ卷必考部分共9题.157分。
15.如图所示,A、B两球完全相同,质量为m,用两根等长
的细线悬挂在O点,两球之间夹着一根劲度系数为月的
轻弹簧,静止不动时,弹簧位于水平方向,两根细线之
间的夹角为 。则弹簧的长度被压缩了
( )
。则弹簧的长度被压缩了
( )
A. B.
B. C.
C. D.
D.
12.为探究NaHCO3、Na2CO3和盐酸(以下盐酸浓度均为1 mol·L-1)反应过程中的热效应,进行实验并测得如下数据:
|
序号 |
35 mL试剂 |
固体 |
混合前温度℃ |
混合后温度℃ |
|
① |
水 |
2.5gNaHCO3 |
20.0 |
18.5 |
|
② |
水 |
3.2gNa2CO3 |
20.0 |
24.3 |
|
③ |
盐酸 |
2.5gNaHCO3 |
20.0 |
16.2 |
|
④ |
盐酸 |
3.2gNa2CO3 |
20.0 |
25.1 |
由此得出的结论正确的是 ( )
A.Na2CO3与盐酸的反应是吸热反应
B.NaHCO3与盐酸的反应是放热反应
C.20.0℃时,含3.2 g Na2CO3的饱和溶液和35 mL盐酸混合后的温度将低于25.1℃
D.20.0℃时,含2.5 g NaHCO3的饱和溶液和35 mL盐酸混合后的温度将低于16.2℃
 13.如图所示,一束红光从空气垂直射到直角玻璃三棱
13.如图所示,一束红光从空气垂直射到直角玻璃三棱
镜的界面AB上,棱镜材料对红光的折射率为 。
。
关于这束光的传播以下说法正确的是 ( )
A.红光第一次到达Ac界面时,有一部分光从AC
界面折射出
B.红光从BC边射出棱镜后的光线与界面BC的夹角为45。
C.红光从Bc边射出棱镜后的光线与界面BC的夹角为60。
D.若换成绿光,从BC边射出棱镜后的光线与界面BC的夹角比红光的大
 14.我国未来将建立月球基地,并在绕月轨道上建造空间
14.我国未来将建立月球基地,并在绕月轨道上建造空间
站.如图所示,关闭动力的航天飞机在月球引力作用
下经椭圆轨道向月球靠近,并将与空间站在B处对
接.已知空间站绕月轨道半径为r,周B期为T,万
有引力常量为c,下列说法中正确的是 ( )
A.图中航天飞机在飞向B处的过程中,速率恒定
 B.航天飞机在B处由椭圆轨道可直接进入空间站轨道
B.航天飞机在B处由椭圆轨道可直接进入空间站轨道
C.根据题中条件可以算出月球质量
D.根据题中条件可以算出空间站受到月球引力的大小
11.欲使0.1mol·L-1的NaHCO3溶液中c(H+)、c(HCO3-)、c(CO2-3)都减少,其方法是
( )
A.加入饱和石灰水溶液 B.加入氢氧化钠固体
C.通人氯化氢气体 D.通人二氧化碳气体
10.制取新型水处理剂ClO2的化学方程式为:
2KClO3+H2C2O4+H2SO4 2C1O2↑+KSO+2CO2↑+2H2O。下列说法不正确的是( )
2C1O2↑+KSO+2CO2↑+2H2O。下列说法不正确的是( )
A.KClO3在反应中得到电子
B.ClO2是还原产物
C.H2C2O4在反应中被氧化
D.1 mol KClO3参加反应有2 mol电子转移
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com